Prinivil 2.5mg, 5mg, 10mg Lisinopril 使用法、副作用および投与量。 オンライン薬局の価格。 処方箋不要のジェネリック医薬品。
Prinivil 2.5mg とは何ですか? どのように使用されますか?
Prinivil は、心臓発作または心不全後の高血圧 (高血圧) の症状を治療するために使用される処方薬です。プリニビルは、単独で使用することも、他の薬と併用することもできます。
- Prinivil は、ACE 阻害剤と呼ばれる薬物のクラスに属します。
- Prinivil が 6 歳未満の子供に安全で効果的であるかどうかはわかっていません。
プリニビルの副作用にはどのようなものがありますか?
Prinivil は、次のような重大な副作用を引き起こす可能性があります。
- 立ちくらみ、
- 熱、
- 喉の痛み、
- 吐き気、
- 弱点、
- ピリピリ感、
- 胸痛、
- 不規則な心拍、
- 動きの喪失、
- 排尿がほとんどまたはまったくない、
- 足や足首のむくみ、
- 疲労感、
- 息を切らして、
- 上腹部の痛み、
- かゆみ、
- 疲労感、
- 食欲減少、
- 暗い尿、
- 粘土色の便、および
- 皮膚や目の黄変(黄疸)
上記の症状がある場合は、すぐに医療機関を受診してください。
Prinivil 5mg の最も一般的な副作用は次のとおりです。
- 頭痛、
- めまい、
- 咳、そして
- 胸痛
気になる副作用や治らない副作用がある場合は、医師に相談してください。
これらは、プリニビルの考えられるすべての副作用ではありません。詳細については、医師または薬剤師にお尋ねください。
副作用に関する医学的アドバイスについては、医師に連絡してください。 1-800-FDA-1088 で副作用を FDA に報告できます。
警告
胎児毒性
- 妊娠が検出されたら、できるだけ早く PRINIVIL を中止してください [警告と注意事項を参照]。
- レニン-アンギオテンシン系に直接作用する薬は、発育中の胎児に傷害や死亡を引き起こす可能性があります[警告と注意事項を参照]。
説明
PRINIVILには、合成ペプチド誘導体であるリシノプリルと、経口の長時間作用型アンギオテンシン変換酵素阻害剤が含まれています。リシノプリルは化学的に (S)-1-[N2-(1-カルボキシ-3-フェニルプロピル)-リシル]-L-プロリン二水和物と表されます。その実験式は C21H31N3O5•2H2O であり、その構造式は次のとおりです。
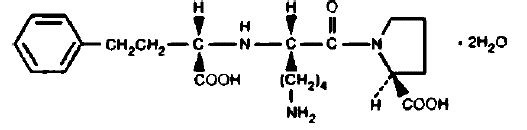
リシノプリルは白色からオフホワイトの結晶性粉末で、分子量は 441.52 です。水に溶けにくく、メタノールにやや溶けにくく、エタノールにほとんど溶けない。
PRINIVIL 10mg は、経口投与用の 5mg、10mg、および 20mg の錠剤として提供されます。有効成分であるリシノプリルに加えて、各錠剤には次の不活性成分が含まれています: リン酸カルシウム、マンニトール、ステアリン酸マグネシウム、デンプン。 10 mg と 20 mg の錠剤には、酸化鉄も含まれています。
適応症
高血圧症
PRINIVIL は、血圧を下げるために 6 歳以上の成人患者および小児患者の高血圧の治療に適応されます。血圧を下げると、致命的および非致命的な心血管イベント、主に脳卒中や心筋梗塞のリスクが低下します。これらの利点は、さまざまな薬理学的クラスの降圧薬の対照試験で見られました。
高血圧の管理は、必要に応じて、脂質管理、糖尿病管理、抗血栓療法、禁煙、運動、およびナトリウム摂取制限を含む包括的な心血管リスク管理の一部であるべきです。多くの患者は、血圧目標を達成するために複数の薬を必要とします。目標と管理に関する具体的なアドバイスについては、国立高血圧教育プログラムの高血圧の予防、検出、評価、および治療に関する合同全国委員会 (JNC) などの公開されたガイドラインを参照してください。
さまざまな薬理学的クラスから、作用機序の異なる多数の降圧薬が無作為対照試験で示され、心血管疾患の罹患率と死亡率を低下させることが示されています。これらの利点の大部分を担っているのは薬です。最大かつ最も一貫した心血管転帰の利点は、脳卒中のリスクの低下ですが、心筋梗塞と心血管死亡率の低下も定期的に見られています.
収縮期圧または拡張期圧の上昇は心血管リスクの増加を引き起こし、mmHg あたりの絶対リスク増加は血圧が高いほど大きくなるため、重度の高血圧をわずかに低下させるだけでもかなりの利益が得られます。血圧低下による相対リスク低下は、絶対リスクが異なる集団全体で類似しているため、高血圧とは無関係にリスクが高い患者 (たとえば、糖尿病や高脂血症の患者) では絶対的利益が大きくなり、そのような患者は、より積極的な治療により、より低い血圧の目標を達成することができます。
一部の降圧薬は、黒人患者では(単剤療法として)血圧への影響が小さく、多くの降圧薬には追加の承認された適応症と効果があります(例、狭心症、心不全、または糖尿病性腎疾患)。これらの考慮事項は、治療法の選択の指針となる場合があります。
PRINIVIL は、単独で投与することも、他の降圧薬と併用することもできます。 臨床研究 ]。
心不全
PRINIVIL は、利尿薬およびジギタリスに十分に反応しない患者の心不全の徴候および症状を軽減することが示されています。 臨床研究 ]。
急性心筋梗塞
PRINIVIL は、急性心筋梗塞から 24 時間以内に血行動態が安定している患者の治療における死亡率の低下を目的としています。患者は、必要に応じて、血栓溶解薬、アスピリン、ベータ遮断薬などの標準的な推奨治療を受けるべきです[参照 臨床研究 ]。
投薬と管理
高血圧症
成人の初期治療: 推奨される初期用量は、1 日 1 回 10 mg です。血圧反応に応じて投与量を調整してください。通常、1 日 20~40mg を 1 日 1 回投与します。 80 mg までの用量が使用されていますが、それ以上の効果が得られるようには見えません。
成人の利尿薬との併用
PRINIVIL 10mg単独で血圧がコントロールされない場合は、低用量の利尿薬を追加することができます(例、ヒドロクロロチアジド12.5mg)。
利尿薬を服用している高血圧の成人患者の推奨開始用量は、1 日 1 回 5 mg です。 薬物相互作用 ]。
6歳以上の高血圧の小児患者
糸球体濾過率が 30 mL/min/1.73 m² を超える小児患者の場合、推奨開始用量は 0.07 mg/kg を 1 日 1 回 (合計 5 mg まで) です。 1日1回0.61mg/kg(40mgまで)を限度として、血圧反応に応じて適宜増減されます。 0.61 mg/kg を超える (または 40 mg を超える) 用量は、小児患者では研究されていません [ 臨床薬理学 ]。
PRINIVIL 2.5mg は、6 歳未満の小児患者、または糸球体濾過量が 30 mL/min/1.73 m² 未満の小児患者には推奨されません [参照 特定の集団での使用 と 臨床研究 ]。
心不全
PRINIVIL 2.5mg の推奨開始用量は、補助療法として利尿剤および (通常は) ジギタリスと併用する場合、1 日 1 回 5mg です。これらの低ナトリウム血症患者 (血清ナトリウム
低血圧の一因となる可能性がある循環血液量減少を最小限に抑えるために、利尿薬の投与量を調整する必要がある場合があります。 警告と注意事項 と 薬物相互作用 ]。 PRINIVIL の初回投与後の低血圧の出現は、低血圧の効果的な管理に続いて、薬剤によるその後の慎重な用量調整を妨げるものではありません。
急性心筋梗塞
急性心筋梗塞の症状が現れてから 24 時間以内に血行動態が安定している患者には、PRINIVIL を 5 mg 経口投与し、続いて 24 時間後に 5 mg、48 時間後に 10 mg、その後 10 mg を 1 日 1 回投与します。投与は少なくとも 6 週間継続する必要があります。
収縮期血圧が低い患者(100~120 mmHg)では、梗塞後の最初の 3 日間に 2.5 mg で治療を開始する [参照 警告と注意事項 ]。低血圧が発生した場合 (収縮期血圧 ≤100 mmHg)、2.5 または 5 mg の用量を検討してください。低血圧が長引く場合 (収縮期血圧
腎障害のある患者における用量
クレアチニンクリアランスが 30 mL/min を超える患者では、PRINIVIL 2.5 mg の用量調整は必要ありません。クレアチニンクリアランスが 10 ~ 30 mL/min の患者では、PRINIVIL の初回投与量を通常の推奨投与量の半分に減らします (すなわち、高血圧症では 5 mg、心不全または急性 MI では 2.5 mg)。血液透析を受けている患者、またはクレアチニンクリアランスが 10 mL/分未満の患者の場合、推奨される初期用量は 2.5 mg を 1 日 1 回です [ 特定の集団での使用 と 臨床薬理学 ]。
サスペンションの準備
1.0 mg/mL の懸濁液 200 mL を調製するには、PRINIVIL 5 mg の 20 mg 錠剤が 10 個入っているポリエチレン テレフタレート (PET) ボトルに USP 精製水 10 mL を加え、少なくとも 1 分間振とうします。クエン酸ナトリウムとクエン酸の内服液または Cytra-2 希釈液 30 mL と Ora-Sweet SF™ 160 mL を PET ボトルの濃縮液に加え、数秒間穏やかに振って成分を分散させます。懸濁液は 25°C (77°F) 以下で保存する必要があり、最大 4 週間保存できます。使用前に毎回懸濁液を振ってください。
供給方法
剤形と強度
錠剤 PRINIVIL 5 mg は白色の楕円形の圧縮錠剤で、片面にコード MSD 19 があり、もう片面に刻み目が入っています。
錠剤 PRINIVIL 10 mg は、片面にコード MSD 106 があり、もう一方の面に刻み目が入った薄黄色の楕円形の圧縮錠剤です。
錠剤 PRINIVIL 20 mg は、桃色の楕円形の圧縮錠剤で、片面にコード MSD 207 があり、もう一方の面に刻み目が付けられています。
保管と取り扱い
PRINIVIL 10mg は、楕円形の圧縮された錠剤として供給され、片側に切り込みが入っています。
保管所
制御された室温、15 ~ 30°C (59 ~ 86°F) で保管し、湿気から保護してください。
製品パッケージが小分けされている場合は、密閉容器に分配してください。
販売元: MERCK & CO., INC., Whitehouse Station, NJ 08889, USA の子会社である Merck Sharp & Dohme Corp.。改訂: 2021 年 11 月
副作用
臨床試験の経験
臨床試験はさまざまな条件下で実施されるため、ある医薬品の臨床試験で観察された副作用の発生率を別の医薬品の臨床試験で観察された発生率と直接比較することはできず、実際に観察された発生率を反映していない可能性があります。
高血圧症
次の有害反応(プラセボよりもプリニビル 5mg で 2% 大きいイベント)が、プラセボと比較してプリニビル 2.5mg で観察されました: 頭痛 (5.7% 対 1.9%)、めまい (5.4% 対 1.9%)、咳 (3.5% 対 1.0%) )。
心不全
心不全患者を対象とした対照研究では、プラセボで12週間治療した患者の7.7%と比較して、PRINIVIL 10mgで12週間治療した患者の8.1%で治療が中止されました。
PRINIVIL vs プラセボ群では、以下の有害反応(プラセボ群よりPRINIVIL 2.5mg群で2%多いイベント)が観察されました:低血圧(4.4% vs 0.6%)、胸痛(3.4% vs 1.3%)。
ATLAS 試験では [参照 臨床研究 心不全患者では、副作用による中止は低用量群と高用量群で同様でした。主に ACE 阻害に関連する次の副作用は、高用量群でより一般的に報告されました。
急性心筋梗塞
PRINIVIL 10mgで治療されたGISSI-3研究の患者は、PRINIVILを服用していない患者と比較して、低血圧(9.0%対3.7%)および腎機能障害(2.4%対1.1%)の発生率が高かった.
対照臨床試験でPRINIVIL 2.5mgで治療された高血圧または心不全の患者の1%以上で発生し、ラベル表示の他のセクションには表示されないその他の臨床的有害反応を以下に示します。
ボディ全体: 疲労、無力症、起立効果。
消化器: 膵炎、便秘、鼓腸、口渇、下痢。
血液学: 骨髄抑制、溶血性貧血、白血球減少症/好中球減少症、血小板減少症のまれなケース。
内分泌: 糖尿病、不適切な抗利尿ホルモン分泌。
代謝: 痛風
肌: 蕁麻疹、脱毛症、光線過敏症、紅斑、潮紅、発汗、皮膚偽リンパ腫、中毒性表皮壊死融解症、スティーブンス・ジョンソン症候群、およびそう痒症。
特別な感覚: 視覚障害、複視、かすみ目、耳鳴り、羞明、味覚障害、嗅覚障害。
泌尿生殖器: インポテンス
その他: 陽性のANA、赤血球沈降速度の上昇、関節痛/関節炎、筋肉痛、発熱、血管炎、好酸球増加症、白血球増加症、感覚異常およびめまいを含む可能性のある複合症状が報告されています。発疹、光線過敏症、またはその他の皮膚症状が単独で、またはこれらの症状と組み合わさって発生することがあります。
臨床検査結果
血清カリウム
臨床試験では、高カリウム血症 (血清カリウム >5.7 mEq/L) が、PRINIVIL 治療を受けた高血圧患者と心不全患者のそれぞれ 2.2% と 4.8% で発生しました [ 警告と注意事項 ]。
クレアチニン、血中尿素窒素
PRINIVIL 5mg単独で治療された高血圧患者の約2%で、血中尿素窒素と血清クレアチニンのわずかな増加が観察されました。利尿薬を併用している患者や腎動脈狭窄のある患者では、増加がより一般的であった[参照 警告と注意事項 ]。血中尿素窒素と血清クレアチニンの可逆的なわずかな増加が、利尿薬併用療法を受けている心不全患者の 11.6% で観察されました。多くの場合、これらの異常は利尿薬の投与量を減らすと解消されました。
PRINIVILで治療されたGISSI-3試験の急性心筋梗塞患者は、病院内および6週間で腎機能障害の発生率が高かった(プラセボで1.1%に対して2.4%)(クレアチニン濃度が3 mg / dL以上または2倍に増加)。ベースラインの血清クレアチニン濃度以上)。
ヘモグロビンとヘマトクリット
ヘモグロビン (平均 0.4 mg/dL) とヘマトクリット (平均 1.3%) のわずかな減少は、PRINIVIL 5 mg で治療された患者で頻繁に発生しましたが、貧血の他の原因がない患者ではめったに臨床的に重要ではありませんでした。臨床試験では、貧血のために治療を中止した患者は 0.1% 未満でした。
肝酵素
まれに、肝酵素および/または血清ビリルビンの上昇が起こる[ 警告と注意事項 ]。
市販後の経験
以下の副作用は、リシノプリルの承認後の使用中に確認されており、他のラベル表示には含まれていません。これらの反応は不確かな規模の集団から自発的に報告されるため、その頻度を確実に推定したり、薬物曝露との因果関係を確立したりすることは常に可能ではありません.その他の反応には次のものがあります。
代謝と栄養障害
低ナトリウム血症 [参照 警告と注意事項 ]、経口抗糖尿病薬またはインスリンを使用している糖尿病患者の低血糖の症例[参照 薬物相互作用 ]
神経系と精神障害
気分の変化(抑うつ症状を含む)、精神錯乱
薬物相互作用
利尿薬
利尿薬を服用している患者が PRINIVIL を開始すると、血圧が過度に低下する可能性があります。 PRINIVILによる降圧効果の可能性は、PRINIVILによる治療の開始前に利尿薬を減らすか中止するか、塩分摂取量を増やすことで最小限に抑えることができます.これが不可能な場合は、PRINIVIL の開始用量を減らします [ 投薬と管理 と 警告と注意事項 ]。
PRINIVIL 2.5mg は、サイアザイド系利尿薬によるカリウム損失を軽減します。カリウム保持性利尿薬(スピロノラクトン、アミロライド、トリアムテレンなど)または血清カリウムを上昇させる可能性のある他の薬は、高カリウム血症のリスクを高める可能性があります。したがって、そのような薬剤の併用が必要な場合は、患者の血清カリウムを頻繁に監視してください。
糖尿病治療薬
プリニビル10mgと糖尿病治療薬(インスリン、経口血糖降下薬)を併用すると、血糖降下作用が強まり、低血糖を起こすおそれがあります。
選択的シクロオキシゲナーゼ-2阻害剤(COX-2阻害剤)を含む非ステロイド性抗炎症剤
高齢者、体液量が減少している患者(利尿薬治療中の患者を含む)、または腎機能が低下している患者では、選択的 COX-2 阻害剤を含む NSAID とリシノプリルを含む ACE 阻害剤を併用すると、以下を含む腎機能が悪化する可能性があります。急性腎不全の可能性があります。これらの影響は通常可逆的です。リシノプリルと NSAID 療法を受けている患者では、腎機能を定期的に監視します。
リシノプリルを含む ACE 阻害剤の降圧効果は、NSAID によって弱まる可能性があります。
レニン-アンジオテンシン系 (RAS) の二重遮断
アンジオテンシン受容体遮断薬、ACE 阻害薬、または直接レニン阻害薬 (アリスキレンなど) による RAS の二重遮断は、単剤療法と比較して、低血圧、失神、高カリウム血症、および腎機能の変化 (急性腎不全を含む) のリスクの増加と関連しています。
Veterans Affairs Nephropathy in Diabetes (VA NEPHRON-D) 試験では、2 型糖尿病患者 1448 人が登録され、尿アルブミン対クレアチニン比が上昇し、推定糸球体濾過率が低下し (GFR 30 から 89.9 ml/分)、ロサルタン療法のバックグラウンドでリシノプリルまたはプラセボを追跡し、中央値で2.2年間追跡しました.ロサルタンとリシノプリルの併用療法を受けた患者は、GFR の低下、末期腎疾患、または死亡という複合エンドポイントについて、単剤療法と比較して追加の利益を得ることはありませんでしたが、単剤療法群と比較して高カリウム血症および急性腎障害の発生率が増加しました。 .
RAS阻害剤との併用は原則として避けてください。 PRINIVIL 5mgおよびRASに影響を与える他の薬剤を服用している患者の血圧、腎機能、および電解質を監視します。
糖尿病患者にはアリスキレンとプリニビルを併用しないでください。腎機能障害のある患者(GFR
リチウム
リチウム毒性は、ACE阻害薬を含むナトリウムの除去を引き起こす薬剤と同時にリチウムを投与されている患者で報告されています。リチウム中毒は通常、リチウムと ACE 阻害剤を中止すると元に戻りました。同時使用中は血清リチウムレベルを監視してください。
金
ニトリトイド反応(顔面紅潮、吐き気、嘔吐、低血圧などの症状)は、注射可能な金(金チオリンゴ酸ナトリウム)による治療と、PRINIVIL を含む併用 ACE 阻害薬治療を受けている患者でまれに報告されています。
哺乳類のラパマイシン標的 (mTOR) 阻害剤
mTOR阻害薬(例、テムシロリムス、シロリムス、エベロリムス)療法を併用している患者は、血管性浮腫のリスクが高くなる可能性がある[参照 警告と注意事項 ]。
ネプリライシン阻害剤
併用ネプリライシン阻害剤(例、サクビトリル)を服用している患者は、血管性浮腫のリスクが高くなる可能性があります[参照 禁忌 と 警告と注意事項 ]。
警告
の一部として含まれています 予防 セクション。
予防
胎児毒性
PRINIVIL を妊婦に投与すると、胎児に害を及ぼす可能性があります。妊娠第 2 期および第 3 期にレニンアンギオテンシン系に作用する薬物を使用すると、胎児の腎機能が低下し、胎児および新生児の罹患率と死亡率が増加します。結果として生じる羊水過少症は、胎児の肺形成不全および骨格の変形に関連している可能性があります。潜在的な新生児の副作用には、頭蓋形成不全、無尿症、低血圧、腎不全、および死亡が含まれます。妊娠が判明したら、できるだけ早く PRINIVIL を中止してください [ 特定の集団での使用 ]。
血管性浮腫およびアナフィラキシー様反応
血管性浮腫
頭頸部血管性浮腫
PRINIVIL を含むアンギオテンシン変換酵素阻害剤で治療された患者では、治療中の任意の時点で、顔面、四肢、唇、舌、声門および/または喉頭の血管性浮腫が発生しており、いくつかの致命的な反応も含まれています。舌、声門、または喉頭に病変がある患者、特に気道手術の既往がある患者は、気道閉塞を経験する可能性があります。 PRINIVIL 5mg は速やかに中止し、血管性浮腫の徴候と症状が完全かつ持続的に消失するまで、適切な治療とモニタリングを行う必要があります。
ACE阻害薬療法とは無関係の血管性浮腫の既往歴のある患者は、ACE阻害薬の投与中に血管性浮腫のリスクが高くなる可能性があります[参照 禁忌 ]。 ACE阻害薬は、黒人以外の患者よりも黒人の血管性浮腫の発生率が高いことに関連しています。
ACE阻害薬とmTOR(ラパマイシンの哺乳類標的)阻害薬(例、テムシロリムス、シロリムス、エベロリムス)の併用療法を受けている患者は、血管性浮腫のリスクが高くなる可能性がある[参照 薬物相互作用 ]。
ACE阻害薬とネプリライシン阻害薬の併用療法を受けている患者は、血管性浮腫のリスクが高くなる可能性があります[参照 禁忌 と 薬物相互作用 ]。
腸血管性浮腫
ACE阻害薬で治療された患者では、腸の血管性浮腫が発生しています。これらの患者は、腹痛(吐き気や嘔吐の有無にかかわらず)を呈しました。場合によっては、顔面血管浮腫の既往がなく、C-1エステラーゼレベルが正常でした.場合によっては、血管性浮腫は、腹部 CT スキャンや超音波などの手順、または手術で診断され、ACE 阻害薬を中止した後に症状が解消されました。
アナフィラキシー様反応
脱感作中のアナフィラキシー様反応
膜翅目毒による脱感作治療を受けている 2 人の患者は、ACE 阻害剤を受けながら、生命を脅かすアナフィラキシー反応を持続しました。
透析中のアナフィラキシー様反応
高流束膜で透析され、ACE阻害剤を併用して治療された一部の患者で、突然の、生命を脅かす可能性のあるアナフィラキシー反応が発生しました。そのような患者では、透析を直ちに中止し、アナフィラキシー様反応に対する積極的な治療を開始する必要があります。これらの状況では、抗ヒスタミン薬によって症状が緩和されません。これらの患者では、異なるタイプの透析膜または異なるクラスの降圧剤の使用を考慮する必要があります。アナフィラキシー反応は、デキストラン硫酸吸収を伴う低密度リポタンパク質アフェレーシスを受けている患者でも報告されています。
腎機能障害
PRINIVIL で治療された患者の腎機能を定期的に監視します。急性腎不全を含む腎機能の変化は、レニン-アンギオテンシン系を阻害する薬剤によって引き起こされる可能性があります。腎機能がレニン-アンギオテンシン系の活性に部分的に依存している可能性がある患者(例、腎動脈狭窄、慢性腎臓病、重度のうっ血性心不全、心筋梗塞後または容量枯渇の患者)は、発症のリスクが特に高い可能性があります。 PRINIVILの急性腎不全。 PRINIVIL 投与中に臨床的に重大な腎機能の低下がみられた患者では、治療の保留または中止を検討する [参照 有害反応 と 薬物相互作用 ]。
低血圧
PRINIVIL は症候性低血圧を引き起こす可能性があり、時には乏尿、進行性高窒素血症、急性腎不全または死亡を合併することがあります。過度の低血圧のリスクがある患者には、次の状態または特徴を持つ患者が含まれます: 収縮期血圧が 100 mmHg 未満の心不全、虚血性心疾患、脳血管疾患、低ナトリウム血症、高用量利尿薬療法、腎透析、または重度の体液量および/または塩分の枯渇あらゆる病因の。
これらの患者では、医師の監督下で PRINIVIL を開始し、治療の最初の 2 週間、および PRINIVIL および/または利尿薬の用量が増加するたびに、そのような患者を追跡します。急性心筋梗塞後に血行動態が不安定な患者では、PRINIVIL 2.5mg の使用を避けてください。
症候性低血圧は、重度の大動脈弁狭窄症または肥大型心筋症の患者でも発生する可能性があります。
手術・麻酔
大手術を受けている患者、または低血圧を引き起こす薬剤による麻酔中の患者では、PRINIVIL は、代償性レニン放出に続発するアンギオテンシン II 形成をブロックする可能性があります。低血圧が発生し、このメカニズムによるものと考えられる場合は、ボリューム拡張によって修正できます。
高カリウム血症
PRINIVIL を投与されている患者では、定期的に血清カリウムをモニターしてください。レニンアンギオテンシン系を阻害する薬は、高カリウム血症を引き起こす可能性があります。高カリウム血症を発症する危険因子には、腎不全、真性糖尿病、およびカリウム保持性利尿薬、カリウムサプリメント、カリウム含有塩代替物、または血清カリウムを上昇させる可能性のある他の薬物の併用が含まれます[ 薬物相互作用 ]。
肝不全
ACE阻害薬は、胆汁うっ滞性黄疸または肝炎から始まり、劇症肝壊死に進行し、時には死に至る症候群と関連しています。この症候群のメカニズムは理解されていません。黄疸または肝酵素の著しい上昇を発症するACE阻害薬を投与されている患者は、ACE阻害薬を中止し、適切な治療を受けるべきです。
非臨床毒性学
発がん、突然変異誘発、生殖能力の障害
リシノプリルを雌雄ラットに 1 日 1 kg あたり 90 mg までの用量で 105 週間、雌雄マウスに 1 日 1 kg あたり 135 mg までの用量で 92 週間投与した場合、腫瘍形成効果の証拠はありませんでした。これらの線量は、体表面積ベースで比較すると、それぞれ MRHDD の 10 倍と 7 倍です。
リシノプリルは、代謝活性化の有無にかかわらず、Ames 微生物変異原試験で変異原性を示さなかった。また、チャイニーズハムスターの肺細胞を用いた前方突然変異試験でも陰性でした。リシノプリルは、in vitro アルカリ溶出ラット肝細胞アッセイで一本鎖 DNA 切断を生じませんでした。さらに、リシノプリルは、チャイニーズハムスター卵巣細胞の in vitro 試験またはマウス骨髄の in vivo 試験で、染色体異常を増加させませんでした。
300 mg/kg/日までのリシノプリル (体表面積ベースで比較すると MRHDD の 33 倍) で処理された雄および雌のラットにおいて、生殖能力に悪影響はありませんでした。
ラットでの研究は、リシノプリルが血液脳関門をほとんど通過しないことを示しています。ラットにリシノプリルを複数回投与しても、どの組織にも蓄積しません。 14C リシノプリル投与後の授乳中のラットの乳汁には放射能が含まれている。標識薬剤を妊娠ラットに投与したところ、全身オートラジオグラフィーにより胎盤に放射能が認められたが、胎児には放射能が認められなかった。
特定の集団での使用
妊娠
リスクの概要
PRINIVIL を妊婦に投与すると、胎児に害を及ぼす可能性があります。妊娠第 2 期および第 3 期にレニンアンギオテンシン系に作用する薬物を使用すると、胎児の腎機能が低下し、胎児および新生児の罹患率と死亡率が増加します。妊娠初期に降圧薬の使用にさらされた後の胎児の異常を調べるほとんどの疫学研究では、レニンアンギオテンシン系に影響を与える薬物を他の降圧薬と区別していません。妊娠が判明したら、できるだけ早くPRINIVIL 5mgを中止してください。
示された集団の主要な先天性欠損症および流産の推定背景リスクは不明です。すべての妊娠には、先天性欠損症、喪失、またはその他の有害な転帰の背景リスクがあります。米国の一般集団では、臨床的に認識された妊娠における主要な先天性欠損症および流産の推定背景リスクは、それぞれ 2 ~ 4% および 15 ~ 20% です。
臨床上の考慮事項
病気に関連する母体および/または胚/胎児のリスク
妊娠中の高血圧は、子癇前症、妊娠糖尿病、早産、分娩合併症(帝王切開の必要性、分娩後出血など)のリスクを高めます。高血圧は、胎児の子宮内発育制限および子宮内死亡のリスクを高めます。高血圧症の妊婦は注意深く監視し、それに応じて管理する必要があります。
胎児/新生児の副作用
妊娠第 2 期および第 3 期にレニン-アンギオテンシン系に影響を与える薬剤を使用している妊婦の羊水過少症は、次のような結果をもたらす可能性があります。 、そして死。特定の患者のレニン-アンギオテンシン系に影響を与える薬物に代わる適切な治療法がないという異常なケースでは、胎児への潜在的なリスクについて母親に知らせてください。
妊娠中に PRINIVIL を服用している患者では、一連の超音波検査を行って羊膜内環境を評価します。妊娠週に基づいて、胎児検査が適切な場合があります。羊水過少症が観察された場合は、母親の命を救うと考えられる場合を除き、PRINIVIL 10mg を中止してください。ただし、患者と医師は、胎児が不可逆的な損傷を受けるまで羊水過少症が現れない可能性があることに注意する必要があります。
低血圧、乏尿、および高カリウム血症のためにプリニビルに子宮内で暴露したことのある乳児を注意深く観察してください。 PRINIVIL への子宮内曝露歴のある新生児で、乏尿または低血圧が発生した場合は、血圧および腎灌流をサポートします。交換輸血または透析は、低血圧の逆転および/または障害のある腎機能の代替手段として必要になる場合があります。
授乳
リスクの概要
母乳中のリシノプリルの存在、または母乳で育てられた乳児または乳生産に対するリシノプリルの影響に関するデータは入手できません。リシノプリルはラットミルクに含まれています。多くの薬物が母乳中に分泌され、母乳育児中の乳児に ACE 阻害剤による重篤な副作用が生じる可能性があるため、母乳育児を中止するか、PRINIVIL を中止してください。
小児用
PRINIVIL の降圧効果と安全性は、6 歳から 16 歳の小児患者で確立されている [参照 投薬と管理 と 臨床研究 ]。小児患者と成人患者の有害反応プロファイルの間に関連する違いは確認されませんでした。
PRINIVIL の安全性と有効性は、6 歳未満の小児患者、または糸球体濾過率が 30 mL/min/1.73 m² 未満の小児患者では確立されていません [ 臨床薬理学 と 臨床研究 ]。
高齢者の使用
高齢者においては、プリニビル 2.5mg による用量調整は必要ありません。心筋梗塞患者を対象としたPRINIVIL 10mgの臨床試験(GISSI-3試験)では、4,413人(47%)が65歳以上、1,656人(18%)が75歳以上でした。この研究では、75 歳以上の患者の 4.8% が腎機能障害のために PRINIVIL 5mg の治療を中止したのに対し、75 歳未満の患者の 1.3% が中止しました。高齢者と若年者の間で安全性または有効性に他の違いは観察されませんでしたが、一部の高齢者の感度が高いことは除外できません.
人種
PRINIVIL を含む ACE 阻害剤の血圧への影響は、黒人以外の患者よりも黒人患者の方が小さくなっています。
腎障害
血液透析を受けている患者、またはクレアチニンクリアランスが 30 mL/min 以下の患者では、PRINIVIL の用量調整が必要です。クレアチニンクリアランスが 30 mL/min を超える患者では、PRINIVIL 5 mg の用量調整は必要ありません。 投薬と管理 と 臨床薬理学 ]。
過剰摂取
20 g/kg の単回経口投与後、ラットで致死は発生せず、同じ用量を投与された 20 匹のマウスのうちの 1 匹で死亡が発生しました。過剰摂取の最も可能性の高い徴候は低血圧であり、通常の治療は通常の生理食塩水の静脈内注入です.
リシノプリルは、血液透析によって除去できます[参照 警告と注意事項 ]。
禁忌
PRINIVIL 10mg は、以下の患者には禁忌です。
- -アンギオテンシン変換酵素阻害剤による以前の治療に関連する血管性浮腫または過敏症の病歴
- 遺伝性または特発性の血管性浮腫。
糖尿病患者には、アリスキレンとプリニビル 5mg を併用してはならない [参照 薬物相互作用 ]。 PRINIVIL は、ネプリライシン阻害剤(例、サクビトリル)との併用は禁忌です。ネプリライシン阻害剤を含む製品であるサクビトリル/バルサルタンに切り替えてから 36 時間以内に PRINIVIL 2.5mg を投与しないでください [ 警告と注意事項 と 薬物相互作用 ]。
臨床薬理学
作用機序
リシノプリルは、ヒトおよび動物のアンギオテンシン変換酵素 (ACE) を阻害します。 ACE は、アンギオテンシン I から血管収縮物質であるアンギオテンシン II への変換を触媒するペプチジルジペプチダーゼです。アンジオテンシン II は、副腎皮質によるアルドステロン分泌も刺激します。高血圧および心不全におけるリシノプリルの有益な効果は、主にレニン-アンジオテンシナルドステロン系の抑制によるものと思われます。 ACEの阻害は血漿アンギオテンシンIIの減少をもたらし、血管収縮活性の減少およびアルドステロン分泌の減少をもたらす。後者の減少は、血清カリウムのわずかな増加をもたらす可能性があります。 PRINIVIL 10mg単独で最大24週間治療された、腎機能が正常な高血圧患者では、血清カリウム値の平均上昇は約0.1mEq/Lでした。しかし、患者の約 15% は 0.5 mEq/L を超える増加を示し、約 6% は 0.5 mEq/L を超える減少を示しました。同じ研究で、PRINIVIL 2.5mg とヒドロクロロチアジドで最長 24 週間治療を受けた患者では、血清カリウムが平均 0.1 mEq/L 減少しました。患者の約 4% は 0.5 mEq/L を超える増加を示し、約 12% は 0.5 mEq/L を超える減少を示しました [参照 警告と注意事項 ]。レニン分泌に対するアンギオテンシン II の負のフィードバックを除去すると、血漿レニン活性が増加します。
ACEは、ブラジキニンを分解する酵素であるキニナーゼと同一です。強力な血管抑制ペプチドであるブラジキニンレベルの上昇が、PRINIVIL 5mgの治療効果に関与しているかどうかは、まだ解明されていません。
PRINIVIL 2.5mg が血圧を下げるメカニズムは、主にレニン-アンギオテンシン-アルドステロン系の抑制であると考えられていますが、PRINIVIL は低レニン高血圧症の患者でも降圧効果があります。 PRINIVIL 10mg は調査したすべての人種で降圧効果がありましたが、黒人高血圧患者 (通常は低レニン高血圧集団) は、非黒人患者よりも単剤療法に対する平均反応が小さかった.
PRINIVIL 5mg とヒドロクロロチアジドの同時投与は、黒人患者と非黒人患者の血圧をさらに低下させ、血圧反応の人種差はもはや明らかではありませんでした。
薬力学
高血圧症
成人患者
PRINIVIL を高血圧患者に投与すると、代償性頻脈を伴わずに、仰臥位と立位の血圧がほぼ同程度に低下します。症候性体位性低血圧は通常は観察されないが、それは起こる可能性があり、体量および/または塩分が枯渇している患者では予想されるべきである[参照 警告と注意事項 ]。サイアザイド系利尿薬と一緒に投与すると、2 つの薬の血圧降下効果はほぼ相加的になります。
調査したほとんどの患者では、PRINIVIL の個別用量の経口投与の 1 時間後に降圧活性の開始が見られ、血圧のピーク低下は 6 時間までに達成されました。降圧効果は、1 日 1 回の推奨投与量で投与後 24 時間で観察されましたが、効果はより一貫しており、平均効果は 20 mg 以上の投与量のいくつかの研究では、低用量よりもかなり大きかった.しかし、調査したすべての用量で、平均降圧効果は、投与後 6 時間よりも投与後 24 時間で大幅に小さくなりました。
PRINIVIL の降圧効果は、長期治療中も維持されます。 PRINIVIL 10mgの突然の中止は、治療前のレベルと比較して、血圧の急激な上昇や血圧の有意な上昇とは関連していません.
薬物動態
成人患者
PRINIVIL の経口投与後、リシノプリルのピーク血清濃度は約 7 時間以内に発生しますが、急性心筋梗塞患者ではピーク血清濃度に到達するまでの時間がわずかに遅れる傾向がありました。血清濃度の低下は、薬物の蓄積に寄与しない延長された終末期を示します。この終末期はおそらく ACE への可飽和結合を表し、用量に比例しません。複数回投与すると、リシノプリルは 12 時間の有効半減期を示します。
リシノプリルは、他の血清タンパク質に結合していないようです。リシノプリルは代謝を受けず、尿中に完全に変化せずに排泄されます。尿中回復に基づくと、リシノプリルの平均吸収範囲は約 25% であり、試験したすべての用量 (5 ~ 80 mg) で大きな被験者間変動 (6 ~ 60%) があります。リシノプリルの吸収は、消化管内の食物の存在によって影響を受けません。リシノプリルの絶対バイオアベイラビリティは、安定した NYHA クラス II ~ IV のうっ血性心不全患者では約 16% に減少し、分布量は正常な被験者よりわずかに小さいようです。
急性心筋梗塞患者におけるリシノプリルの経口バイオアベイラビリティーは、健康なボランティアと同様です。
腎機能障害は、主に腎臓から排泄されるリシノプリルの排泄を減少させますが、この減少が臨床的に重要になるのは、糸球体濾過速度が 30 mL/分未満の場合のみです。この糸球体濾過速度を超えると、排泄半減期はほとんど変化しません。しかし、障害が大きくなると、リシノプリルのピークおよびトラフレベルが上昇し、濃度がピークに達するまでの時間が長くなり、定常状態に達するまでの時間が長くなります。年配の患者は、平均して、若い患者よりも血中濃度と血漿濃度時間曲線下面積 (AUC) が (約 2 倍) 高い [参照 投薬と管理 ]。リシノプリルは血液透析で除去できます。
ラットでの研究は、リシノプリルが血液脳関門をほとんど通過しないことを示しています。ラットにリシノプリルを複数回投与しても、どの組織にも蓄積しません。 14C リシノプリル投与後の授乳中のラットの乳汁には放射能が含まれている。標識薬剤を妊娠ラットに投与したところ、全身オートラジオグラフィーにより胎盤に放射能が認められたが、胎児には放射能が認められなかった。
小児患者
リシノプリルの薬物動態は、糸球体濾過率が 30 mL/min/1.73 m² を超える 6 歳から 16 歳までの 29 人の小児高血圧患者で研究されました。 0.1から0.2mg/kgの投与後、リシノプリルの定常状態ピーク血漿濃度は6時間以内に生じ、尿中回復に基づく吸収の程度は約28%であった。これらの値は、以前に成人で得られた値と同様です。体重 30 kg の小児におけるリシノプリルの経口クリアランス (全身クリアランス/絶対バイオアベイラビリティ) の典型的な値は 10 L/h であり、これは腎機能に比例して増加します。
臨床研究
高血圧症
成人患者
利尿薬を服用していない軽度から中等度の高血圧患者 438 人を対象に、1 日 1 回のレジメンを利用した 2 つの用量反応研究が実施されました。投与後24時間に血圧を測定した。 PRINIVIL の降圧効果は、一部の患者で 5 mg で見られました。しかし、どちらの研究でも、10、20、または 80 mg の PRINIVIL で治療された患者の方が血圧低下が早く、より大きかった。軽度から中等度の高血圧患者を対象とした対照臨床研究では、PRINIVIL 20-80 mg をヒドロクロロチアジド 12.5-50 mg およびアテノロール 50-500 mg と比較し、中等度から重度の高血圧患者ではメトプロロール 100-200 mg と比較しました。 75%が白人である人口において、収縮期血圧および拡張期血圧に対する効果は、ヒドロクロロチアジドよりも優れていました。 PRINIVIL 10mg は、拡張期血圧への影響においてアテノロールおよびメトプロロールとほぼ同等であり、収縮期血圧への影響はやや大きかった.
PRINIVIL は、若年および高齢 (>65 歳) の患者で同様の有効性と有害作用を示しました。黒人では白人よりも効果が低かった.
本態性高血圧患者を対象としたPRINIVIL 5mgの血行動態研究では、心拍出量と心拍数にほとんどまたはまったく変化がなく、血圧低下に伴って末梢動脈抵抗が低下しました。 9 人の高血圧患者を対象とした研究では、PRINIVIL 5mg の投与後に平均腎血流量が増加しましたが、有意ではありませんでした。腎機能が正常な高血圧患者の糸球体濾過率に対するリシノプリルの効果に関しては、いくつかの小規模な研究のデータに一貫性がありませんが、変化があったとしても大きくないことを示唆しています。
腎血管性高血圧症の患者では、PRINIVIL は忍容性が高く、血圧を下げるのに効果的であることが示されています。 警告と注意事項 ]。
小児患者
歳から 16 歳の高血圧の小児患者 115 人を対象とした臨床研究では、体重が 50 kg 未満の患者には毎日 0.625、2.5、または 20 mg のリシノプリルが投与され、体重が 50 kg 以上の患者には 1.25、5、または 40 mg のいずれかが投与されました。毎日リシノプリルの。 2 週間の終わりに、リシノプリルを 1 日 1 回投与すると、トラフ血圧が用量依存的に低下し、一貫した降圧効果が 1.25 mg (0.02 mg/kg) を超える用量で示されました。この効果は離脱段階で確認され、プラセボに無作為に割り付けられた患者では、中用量および高用量のリシノプリルを継続するように無作為に割り付けられた患者よりも拡張期血圧が約 9 mmHg 上昇しました。リシノプリルの用量依存的な降圧効果は、いくつかの人口統計学的サブグループ(年齢、タナー期、性別、および人種)にわたって一貫していました。この研究では、リシノプリルは一般的に忍容性が良好でした。
上記の小児科の研究では、リシノプリルは、錠剤を飲み込むことができない、または錠剤の形よりも低用量を必要とする子供や乳児のために、錠剤または懸濁液として投与されました。 投薬と管理 ]。
心不全
つのプラセボ対照の 12 週間の臨床研究では、PRINIVIL 2.5mg を毎日 20mg まで追加した場合と、ジギタリスおよび利尿薬のみを追加した場合とを比較しました。 PRINIVIL、ジギタリス、および利尿薬の組み合わせは、心不全の次の徴候および症状を軽減しました:浮腫、ラ音、発作性夜間呼吸困難および頸静脈拡張。ある研究では、PRINIVIL 2.5mg、ジギタリス、利尿薬の組み合わせにより、起座呼吸、第 3 心音の存在、および NYHA クラス III および IV に分類される患者の数が減少し、運動耐性が改善されました。大規模な (3000 人以上の患者) 生存研究である ATLAS 試験では、収縮性心不全患者における 2.5 mg と 35 mg のリシノプリルを比較し、リシノプリルの高用量が低用量と少なくとも同じくらい良好な結果をもたらすことを示しました。ベースラインで管理された臨床試験では、ジギタリスと利尿薬を投与されている患者に PRINIVIL 5mg を単回投与すると、肺毛細血管楔入圧、体血管抵抗、血圧が低下し、心拍出量が増加し、心拍数は変化しませんでした。
急性心筋梗塞
Gruppo Italiano per lo Studio della Sopravvienza nell’Infarto Miocardico (GISSI-3) 研究は、冠動脈治療室に入院した急性心筋梗塞 (MI) 患者 19,394 人を対象に実施された、多施設共同、無作為化、非盲検の臨床試験でした。これは、リシノプリル、硝酸塩、それらの組み合わせによる短期 (6 週間) 治療、または治療なしの短期 (6 週間) 死亡率および長期死亡率、ならびに心機能の著しい障害に対する効果を調べるために設計されました。症状の発症から 24 時間以内に現れる血行動態が安定している患者を、2 x 2 要因計画で、1) PRINIVIL 単独 (n=4841)、2) 硝酸塩単独 (n=4869)、3 のいずれかに 6 週間ランダムに割り付けました。 ) PRINIVIL 2.5mg と硝酸塩 (n=4841)、または 4) オープンコントロール (n=4843)。すべての患者は、血栓溶解薬(72%)、アスピリン(84%)、およびベータ遮断薬(31%)を含む通常の治療を受け、通常は急性心筋梗塞(MI)患者に使用されます。
プロトコルは、低血圧 (収縮期血圧 ≤100 mmHg)、重度の心不全、心原性ショック、および腎機能障害 (血清クレアチニン > 2 mg/dL および/またはタンパク尿 > 500 mg/24 時間) の患者を除外しました。 PRINIVIL 5 mg に無作為に割り付けられた患者は、症状の発症から 24 時間以内に 5 mg、24 時間後に 5 mg、その後は毎日 10 mg を投与されました。ベースラインで収縮期血圧が 120 mmHg 未満の患者には、2.5 mg の PRINIVIL が投与されました。低血圧が発生した場合、PRINIVIL 10mg の用量を減らすか、重度の低血圧が発生した場合、PRINIVIL を中止した [参照 投薬と管理 ]。
試験の主要アウトカムは、6 週間での全死亡率と、心筋梗塞後 6 か月で死亡した患者数、晩期 (4 日目) 臨床的うっ血性心不全を発症した患者数、または広範囲の左心室を有していた患者数からなる複合エンドポイントでした。駆出率 ≤35% として定義される損傷、または無動 - ジスキネティック [AD] スコア ≥45%。 PRINIVIL を単独または硝酸塩と一緒に投与された患者 (n=9646) は、PRINIVIL を投与されなかった患者 (n=9672) と比較して、死亡リスクが 11% 低かった (p = 0.04) (それぞれ 6.4% 対 7.2%)。 6週間で。 PRINIVIL を最大 6 週間投与するように無作為に割り付けられた患者は、6 か月での複合エンドポイントでも数値的に良好でしたが、心不全の評価のオープンな性質、追跡心エコー検査の実質的な損失、および PRINIVIL 10mg の実質的な過剰使用により、 6 週間のリシノプリルに無作為に割り付けられたグループの 6 週間と 6 か月は、このエンドポイントに関する結論を排除します。
PRINIVIL 10mgで治療された急性心筋梗塞患者は、持続性低血圧(1時間以上収縮期血圧 有害反応 ]。
患者情報
注: この情報は、この薬の安全で効果的な使用を支援することを目的としています。考えられるすべての悪影響または意図された影響を開示するものではありません。
妊娠
妊娠可能な年齢の女性患者に、妊娠中のプリニビル 10mg への曝露の影響について伝えてください。妊娠を計画している女性と治療の選択肢について話し合います。できるだけ早く医師に妊娠を報告するように患者に伝えてください。
血管性浮腫
喉頭浮腫を含む血管性浮腫は、PRINIVIL を含むアンギオテンシン変換酵素阻害剤による治療中にいつでも発生する可能性があります。血管性浮腫を示唆する徴候や症状(顔、四肢、目、唇、舌の腫れ、嚥下や呼吸の困難)を直ちに報告し、処方医に相談するまで薬を服用しないよう患者に伝えてください.
症候性低血圧
特に治療の最初の数日間は、めまいを報告するように患者に伝えてください。実際に失神が起こった場合は、処方医に相談するまで薬を中止するよう患者に伝えてください。
過度の発汗と脱水は、体液量の減少により血圧が過度に低下する可能性があることを患者に伝えます。嘔吐や下痢などの体液量減少の他の原因も、血圧の低下につながる可能性があります。それに応じて患者にアドバイスします。
高カリウム血症
医師に相談せずにカリウムを含む代替塩を使用しないように患者に伝えてください。
低血糖症
経口抗糖尿病薬またはインスリンで治療を受けている糖尿病患者には、特に併用の最初の 1 か月間は、低血糖を注意深く監視するように ACE 阻害薬を開始するよう伝えてください [ 薬物相互作用 ]。
白血球減少症/好中球減少症
白血球減少症/好中球減少症の徴候である可能性がある感染の徴候(例、喉の痛み、発熱)を速やかに報告するよう患者に伝えます。
