Minipress 1mg, 2mg Prazosin 使用法、副作用および投与量。 オンライン薬局の価格。 処方箋不要のジェネリック医薬品。
ミニプレスとは何ですか?
ミニプレス(塩酸プラゾシン)は、高血圧(高血圧)の治療に使用されるαアドレナリン遮断薬です。
ミニプレス 2mg の副作用は何ですか?
Minipress 1mg の一般的な副作用は次のとおりです。
- 頭痛、
- 眠気、
- 疲れ、
- 弱点、
- ぼやけた視界、
- 吐き気、
- 嘔吐、
- 下痢、または
- あなたの体が薬に順応するための便秘
Minipress 2mg の他の副作用は次のとおりです。
- 立ちくらみや立ちくらみ、特に最初の投与後、および治療の最初の週に薬を服用した直後。
Minipress 1mg の深刻な副作用が発生した場合は、医師に相談してください。心臓の鼓動が速くなったり、ドキドキしたり、胸がドキドキしたり、気絶しそうな気分になったり、呼吸が困難になったり、手や足が腫れたり、勃起が 4 時間続く場合や痛みを伴う場合は、医師に相談してください。またはそれ以上。
説明
キナゾリン誘導体である MINIPRESS® (プラゾシン塩酸塩) は、降圧剤の新しい化学クラスの最初のものです。これは、1-(4-アミノ-6,7-ジメトキシ-2-キナゾリニル)-4-(2-フロイル) ピペラジンの塩酸塩であり、その構造式は次のとおりです。
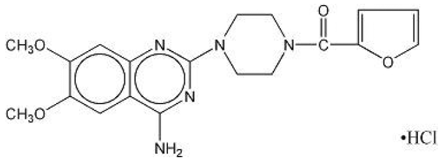
分子式 C19H21N5O4・HCl
白色の結晶性物質で、水と等張食塩水にわずかに溶け、分子量は 419.87 です。経口用のミニプレスの各 1 mg カプセルには、1 mg の遊離塩基に相当する薬物が含まれています。
製剤中の不活性成分は次のとおりです。ハード ゼラチン カプセル (青 1、赤 3、赤 28、赤 40、およびその他の不活性成分を含む場合があります)。ステアリン酸マグネシウム;ラウリル硫酸ナトリウム;スターチ;スクロース。
適応症
ミニプレス 1mg は、血圧を下げるために高血圧の治療に適応されます。血圧を下げると、主に脳卒中や心筋梗塞などの致命的および非致命的な心血管イベントのリスクが低下します。これらの利点は、この薬を含むさまざまな薬理学的クラスの降圧薬の対照試験で見られました。
高血圧の管理は、必要に応じて、脂質管理、糖尿病管理、抗血栓療法、禁煙、運動、およびナトリウム摂取制限を含む包括的な心血管リスク管理の一部であるべきです。多くの患者は、血圧目標を達成するために複数の薬を必要とします。目標と管理に関する具体的なアドバイスについては、国立高血圧教育プログラムの高血圧の予防、検出、評価、および治療に関する合同全国委員会 (JNC) のガイドラインなど、公開されているガイドラインを参照してください。
さまざまな薬理学的クラスから、作用機序の異なる多数の降圧薬が無作為対照試験で示され、心血管疾患の罹患率と死亡率を低下させることが示されています。これらの利点の大部分を担っているのは薬です。最大かつ最も一貫した心血管転帰の利点は、脳卒中のリスクの低下ですが、心筋梗塞と心血管死亡率の低下も定期的に見られています.
収縮期圧または拡張期圧の上昇は心血管リスクの増加を引き起こし、mmHg あたりの絶対リスク増加は血圧が高いほど大きくなるため、重度の高血圧をわずかに低下させるだけでもかなりの利益が得られます。血圧低下による相対リスク低下は、絶対リスクが異なる集団全体で類似しているため、高血圧とは無関係にリスクが高い患者 (たとえば、糖尿病や高脂血症の患者) では絶対的利益が大きくなり、そのような患者は、より積極的な治療により、より低い血圧の目標を達成することができます。
一部の降圧薬は、黒人患者では(単剤療法として)血圧への影響が小さく、多くの降圧薬には追加の承認された適応症と効果があります(例、狭心症、心不全、または糖尿病性腎疾患)。これらの考慮事項は、治療法の選択の指針となる場合があります。
MINIPRESS は、単独で使用することも、利尿薬やベータアドレナリン遮断薬などの他の降圧薬と組み合わせて使用することもできます。
投薬と管理
ミニプレス 1mg の投与量は、患者の個々の血圧反応に応じて調整する必要があります。以下は、その管理のガイドです。
初回投与量
1mgを1日2~3回( 警告 .)
維持量
用量は、分割用量で与えられる 20 mg の合計 1 日用量までゆっくりと増加させることができます。最も一般的に使用される治療用量は、分割用量で与えられた 1 日 6 mg から 15 mg の範囲です。通常、20 mg を超える用量では有効性が向上しませんが、数回に分けて 1 日 40 mg までさらに増量することで効果が得られる患者もいます。最初の滴定後、一部の患者は 1 日 2 回の投与計画で適切に維持できます。
他の薬との併用
利尿剤などの降圧剤を追加する場合は、ミニプレス 1mg を 1 日 3 回 1mg または 2mg に減量してから漸増してください。
MINIPRESS 1mg と PDE-5 阻害剤を併用すると、相加的な血圧降下効果と症候性低血圧が生じる可能性があります。したがって、MINIPRESS を服用している患者では、PDE-5 阻害剤療法を最低用量で開始する必要があります。
供給方法
配布元: Pfizer Labs, Divsion of Pfizer Inc., NY, NY 10017. 改訂: 2015 年 2 月
副作用
臨床試験は 900 人以上の患者に対して実施されました。これらの試験およびその後のマーケティング経験において、MINIPRESS 療法に関連する最も頻繁な反応は、めまい 10.3%、頭痛 7.8%、眠気 7.6%、エネルギー不足 6.9%、衰弱 6.5%、動悸 5.3%、吐き気 4.9% でした。ほとんどの場合、副作用は治療を継続することで消失するか、薬剤の投与量を減らさなくても耐えられます。
患者の 1 ~ 4% で発生すると報告されている頻度の低い副作用は次のとおりです。
胃腸: 嘔吐、下痢、便秘。
心臓血管: 浮腫、起立性低血圧、呼吸困難、失神。
中枢神経系: めまい、うつ病、神経質。
皮膚科: 発疹。
泌尿生殖器: 頻尿。
EENT: かすみ目、赤くなった強膜、鼻出血、口渇、鼻づまり。
さらに、患者の 1% 未満が次のことを報告しています (場合によっては、正確な因果関係が確立されていません)。
胃腸: 腹部不快感および/または痛み、肝機能異常、膵炎。
心臓血管: 頻脈。
中枢神経系: 感覚異常、幻覚。
皮膚科: そう痒症、脱毛症、扁平苔癬。
泌尿生殖器: 失禁、インポテンス、持続勃起症。
EENT: 耳鳴り。
他の: 発汗、発熱、陽性ANA力価、関節痛。
色素斑と漿液性網膜症の単一の報告、および白内障の発生または消失のいくつかの報告が報告されています.これらの例では、ベースラインの観察が不十分であることが多いため、正確な因果関係は確立されていません。
適切なベースライン検査を含む、より具体的なスリットランプおよび眼底検査の研究では、薬物に関連した異常な眼科的所見は報告されていません。
MINIPRESS 1mg療法を既存のナルコレプシーの悪化と関連付ける文献報告が存在します。これらの場合、因果関係は定かではありません。
市販後の経験では、次の有害事象が報告されています。
自律神経系: フラッシング。
全身: アレルギー反応、無力症、倦怠感、痛み。
循環器、一般: 狭心症、低血圧。
内分泌: 女性化乳房。
心拍数/リズム: 徐脈。
精神的: 不眠症。
スキン/付属物: 蕁麻疹。
血管(心臓外): 血管炎。
ヴィジョン: 眼の痛み。
特別な感覚: 白内障手術中、術中フロッピー虹彩症候群 (IFIS) として知られる小さな瞳孔症候群の変種が、α-1 遮断薬療法に関連して報告されています (以下を参照)。 予防 )。
薬物相互作用
MINIPRESS 2mg は、これまでの限られた臨床経験の中で、次の薬物との有害な相互作用なしに投与されています。 (2) 血糖降下薬 - インスリン、クロルプロパミド、フェンホルミン、トラザミド、およびトルブタミド。 (3) 精神安定剤および鎮静剤 - クロルジアゼポキシド、ジアゼパム、およびフェノバルビタール。 (4) 抗痛風アロプリノール、コルヒチン、およびプロベネシド。 (5) 抗不整脈薬 - プロカインアミド、プロプラノロール (参照 警告 ただし)、およびキニジン; (6)鎮痛剤、解熱剤、および抗炎症剤 - プロポキシフェン、アスピリン、インドメタシン、およびフェニルブタゾン。
MINIPRESS 2mgに利尿剤または他の降圧剤を追加すると、相加的な降圧効果が生じることが示されています。この影響は、MINIPRESS の用量を 1 日 3 回 1 ~ 2 mg に減らし、追加の降圧薬を慎重に導入し、その後、臨床反応に基づいて MINIPRESS を再調整することによって最小限に抑えることができます。 MINIPRESS とホスホジエステラーゼ-5 (PDE-5) 阻害剤の併用投与は、相加的な血圧降下効果と症候性低血圧をもたらす可能性があります ( 投薬と管理 )。
薬物/実験室試験の相互作用
日あたり 12 ~ 24 mg のプラゾシンを 10 ~ 14 日間投与された 5 人の患者に関する研究では、ノルエピネフリンの尿中代謝物が平均 42% 増加し、尿中 VMA が平均 17% 増加しました。したがって、プラゾシンで治療されている患者の褐色細胞腫のスクリーニング検査で、偽陽性の結果が生じる可能性があります。 VMA の上昇が見つかった場合は、プラゾシンを中止し、1 か月後に患者を再検査する必要があります。
臨床検査
脂質プロファイルが追跡された臨床研究では、一般に、治療前と治療後の脂質レベルの間に有害な変化は見られませんでした.
警告
すべてのアルファ遮断薬と同様に、MINIPRESS は突然の意識喪失を伴う失神を引き起こす可能性があります。ほとんどの場合、これは過度の姿勢性低血圧効果によるものと考えられていますが、シンコパレピス頌歌の前に、心拍数が毎分 120 ~ 160 回の重度の頻脈の発作が起こることもあります。失神は、通常、薬物の初回投与から 30 ~ 90 分以内に発生します。時折、それらは急激な用量の年齢の増加、または高用量のMINIPRESSを服用している患者のレジメンへの別の降圧薬の導入に関連して報告されています. Syncopalepis odes の発生率は、2 mg 以上の初期用量を投与された患者で約 1% です。この薬剤の治験段階で実施された臨床試験では、薬剤の初回投与量を 1 mg に制限し、その後投与量をゆっくりと増やし、追加の降圧薬を患者のレジメンに導入することにより、失神のエピソードを最小限に抑えることができることが示唆されています。注意してください(用法・用量を参照)。プロプラノロールなどのベータ遮断薬も投与されている MINIPRESS を投与された患者では、低血圧が発生する可能性があります。
失神が発生した場合は、患者を横臥位にし、必要に応じて支持療法を行う必要があります。この悪影響は自己制限的であり、ほとんどの場合、治療の初期期間後またはその後の用量漸増中に再発しません。
患者は常に MINIPRESS の 1 mg カプセルから開始する必要があります。 2 および 5 mg のカプセルは、初回治療には適応されません。
意識の喪失よりも一般的なのは、しばしば血圧の低下に関連する症状、すなわちめまいや立ちくらみです。患者は、これらの副作用の可能性について警告し、どのような対策を講じるべきかをアドバイスする必要があります。また、MINIPRESS 2mg 治療の開始中に失神が発生した場合、怪我をする可能性がある状況を避けるように患者に注意する必要があります。
持続勃起症
延長された勃起と持続勃起症は、マーケティング後の経験で、プラゾシンを含むアルファ-1 ブロッカーで報告されています。勃起が 4 時間以上続く場合は、直ちに医師の診察を受けてください。持続勃起症をすぐに治療しないと、陰茎組織が損傷し、効力が永久に失われる可能性があります。
予防
全般的
術中フロッピー虹彩症候群 (IFIS) は、α-1 遮断薬で治療された一部の患者の白内障手術中に観察されています。この小瞳孔症候群の変種は、術中の灌流に反応してうねる弛緩した虹彩、標準的な散瞳薬による術前の拡張にもかかわらず進行性の術中の縮瞳、水晶体超音波乳化吸引術の切開部に向かって虹彩が脱出する可能性の組み合わせによって特徴付けられます。患者の眼科医は、アイリス フック、アイリス ダイレーター リング、または粘弾性物質の利用など、手術手技の変更に備える必要があります。白内障手術の前にα-1ブロッカー療法を中止しても、利益はないようです。
発がん、突然変異誘発、生殖能力の障害
MINIPRESS 1mg をラットに 18 か月間投与した試験では、人間の通常の最大推奨用量である 1 日あたり 20mg の 225 倍以上の用量で発がん性の可能性は示されませんでした。 MINIPRESS 2mg は、in vivo 遺伝毒性試験で変異原性を示さなかった。受精能および一般的な生殖能力に関するラットの研究では、75 mg/kg (通常の最大推奨ヒト用量の 225 倍) で処理された雄と雌の両方で受胎能の低下が示されましたが、25 mg/kg (通常の最大推奨用量の 75 倍) で処理されたラットは受胎能の低下を示しました。人への最大推奨用量)はありませんでした。
ミニプレスのラットおよびイヌにおける慢性試験(1年以上)では、萎縮および壊死からなる精巣の変化が25mg/kg/日(通常の最大推奨ヒト用量の75倍)で発生した. 10 mg/kg/日 (通常の最大推奨ヒト用量の 30 倍) では、ラットまたはイヌで精巣の変化は見られませんでした。動物で観察された精巣の変化を考慮して、長期MINIPRESS療法を受けている105人の患者を17-ケトステロイド排泄についてモニターしたが、薬物効果を示す変化は観察されなかった.さらに、MINIPRESS 1mg を最長 51 か月間服用した 27 人の男性は、薬物効果を示唆する精子の形態に変化がありませんでした。
妊娠中の使用
妊娠カテゴリーC。 MINIPRESS 1mg は、通常の最大推奨用量の 225 倍を超える用量をラットに投与した場合、出生時、生後 1、4、および 21 日齢の同腹仔数の減少に関連することが示されています。薬物関連の外部、内臓、または骨格の胎児異常の証拠は観察されませんでした。妊娠したウサギの胎児および妊娠したサルの胎児において、通常の最大推奨最大用量の 225 倍および 12 倍を超える用量で、薬物に関連する外部、内臓、または骨格の異常はそれぞれ観察されませんでした。
44人の妊娠中の女性の重度の高血圧を制御するためのプラゾシンとベータ遮断薬の使用は、薬物に関連した胎児の異常や悪影響を明らかにしませんでした.プラゾシンによる治療は 14 週間も継続されました。
プラゾシンはまた、他の研究者によって重度の妊娠高血圧症において、単独で、または他の降圧薬と組み合わせて使用されています.プラゾシンの使用による胎児または新生児の異常は報告されていません.2
妊娠中の女性における MINIPRESS の安全性を確立する、十分に管理された研究はありません。ミニプレスは、潜在的な利益が母親と胎児への潜在的なリスクを正当化する場合にのみ、妊娠中に使用する必要があります。
授乳中の母親
MINIPRESS 1mg は、母乳中に少量排泄されることが示されています。ミニプレス2mgを授乳中の女性に投与する場合は注意が必要です。
子供の使用法
小児における安全性と有効性は確立されていません。
参考文献
1. Lubbe, WF, and Hodge, JV: New Zealand Med J, 94 (691) 169-172, 1981.
2. Davey、DA、および Dommisse、J: SA Med J、1980 年 10 月 4 日 (551-556)。
過剰摂取
2 歳の子供が MINIPRESS を 50 mg 以上誤って摂取すると、深刻な眠気と反射神経の低下が起こりました。血圧の低下は認められなかった。回復は順調でした。
過剰摂取が低血圧につながる場合は、心臓血管系のサポートが最も重要です.血圧の回復と心拍数の正常化は、患者を仰臥位に保つことで達成できます。この対策が不十分な場合は、まずショックをボリューム エキスパンダーで処理する必要があります。必要に応じて、昇圧剤を使用する必要があります。腎機能を監視し、必要に応じてサポートする必要があります。検査データは、MINIPRESS がタンパク質に結合しているため透析できないことを示しています。
禁忌
MINIPRESS は、キナゾリン、プラゾシン、またはいずれかの不活性成分に過敏であることがわかっている患者には禁忌です。
臨床薬理学
プラゾシンの降圧作用の正確なメカニズムは不明です。プラゾシンは総末梢抵抗の減少を引き起こし、当初は血管平滑筋に対する直接的な弛緩作用があると考えられていました。しかし、最近の動物研究は、プラゾシンの血管拡張効果がシナプス後アルファアドレナリン受容体の遮断にも関連していることを示唆しています.イヌの前肢実験の結果は、プラゾシンの末梢血管拡張効果が主に抵抗血管 (細動脈) のレベルに限定されることを示しています。従来のα遮断薬とは異なり、プラゾシンの降圧作用は通常、反射性頻脈を伴いません。寛容は、長期治療で発達することは観察されていません。
急性単回投与後および長期維持療法の過程で、血行動態研究がヒトで実施された。結果は、治療効果が心拍出量、心拍数、腎血流および糸球体濾過率の臨床的に有意な変化を伴わない血圧の低下であることを確認しています。測定可能な負の変時効果はありません。
これまでの臨床研究では、塩酸プラゾシンは血漿レニン活性を増加させませんでした。
男性では、仰臥位と立位の両方で血圧が低下します。この効果は、拡張期血圧で最も顕著です。
経口投与後、ヒトの血漿濃度は約 3 時間でピークに達し、血漿半減期は 2 ~ 3 時間です。この薬は、血漿タンパク質と強く結合しています。バイオアベイラビリティ研究では、20% アルコール溶液中の薬物に対する総吸収は 90% であり、溶液中の薬物のピークレベルの約 65% になることが実証されています。動物研究は、プラゾシン塩酸塩が主に脱メチル化と抱合によって広範囲に代謝され、主に胆汁と糞便を介して排泄されることを示しています。あまり広範囲ではない人間の研究は、人間の同様の代謝と排泄を示唆しています。
脂質プロファイルが追跡された臨床研究では、一般に、治療前と治療後の脂質レベルの間に有害な変化は見られませんでした.
患者情報
この薬の最初の服用後に、めまいや眠気が起こることがあります。この薬を服用してから最初の 24 時間、または用量を増やした後は、運転や危険を伴う作業を避けてください。めまい、立ちくらみ、または失神が起こることがあり、特に横になったり座ったりした状態から立ち上がるときに起こります。ゆっくり起き上がると、問題が軽減される場合があります。これらの影響は、アルコールを飲んだり、長時間立ったり、運動したり、天気が暑い場合にも発生する可能性があります.ミニプレスを服用中は、飲酒量に注意してください。また、運動時や炎天下、長時間立ちっぱなしの場合は特にご注意ください。ご不明な点がございましたら、医師にご確認ください。
