Sumycin 250mg, 500mg Tetracycline 使用法、副作用および投与量。 オンライン薬局の価格。 処方箋不要のジェネリック医薬品。
スマイシンとは何ですか?
スマイシン (塩酸テトラサイクリン) は、尿路感染症、にきび、淋病、クラミジアなど、さまざまな細菌感染症の治療に使用される抗生物質です。スマイシンは一般的な形で入手できます。
Sumycin 250mgの副作用は何ですか?
スマイシンの一般的な副作用は次のとおりです。
- 吐き気、
- 嘔吐、
- 下痢、
- 胃の不調、
- 食欲減少、
- 口の中や唇に白い斑点やただれがある
- 舌の腫れ、
- 黒い毛むくじゃらの舌、
- 喉の痛み、
- 嚥下障害、
- めまい、
- 頭痛、
- 直腸または生殖器領域のただれまたは腫れ、または
- 膣のかゆみまたは分泌物。
薬剤耐性菌の発生を抑え、スマイシン'250'の有効性を維持します。およびスマイシン「500」錠剤(塩酸テトラサイクリン錠)などの抗菌薬、スマイシン「250」およびスマイシン「500」錠剤(テトラサイクリン塩酸塩錠剤)は、細菌が原因であることが証明されている、または強く疑われる感染症の治療または予防にのみ使用してください。
説明
経口投与用のスマイシンには、Streptomyces aureofaciens から分離された抗生物質であるテトラサイクリンが含まれています。テトラサイクリンは化学的に 4-(ジメチルアミノ)-1, 4, 4a, 5, 5a, 6, 11, 12a-オクタ-ヒドロ-3, 6, 10, 12, 12a-ペンタヒドロキシ-6-メチル-1, 11 と表されます。 -ジオキソ-2-ナフタセンカルボキサミド;その構造式は次のとおりです。
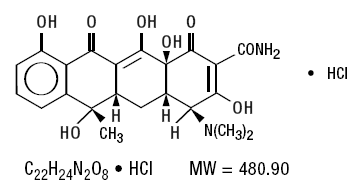
スマイシン '250'およびスマイシン「500」錠剤 (テトラサイクリン塩酸塩錠剤) は、それぞれ 250 mg および 500 mg のテトラサイクリン塩酸塩を提供する錠剤として、経口投与に利用できます。不活性成分: 着色料 (D&C Red No. 30 アルミニウムレーキ、二酸化チタン)、ヒプロメロース、無水ラクトース、ステアリン酸マグネシウム、微結晶性セルロース、ポビドン、アルファ化デンプン、ステアリン酸。また、250mgには塩化メチレンヒドロキシプロピルセルロース、トリアセチン、500mgにはポリエチレングリコール、ポリパラベン、メチルパラベン、クエン酸ナトリウム、ソルビン酸カリウム、プロピルパラベン、キサンタンガムが含まれています。
適応症
スマイシン '250' 錠、スマイシン '500' 錠(テトラサイクリン塩酸塩錠)などの抗菌薬の耐性菌の発生を抑制し、その効果を維持するために、スマイシン '250' 錠、スマイシン '500' 錠(テトラサイクリン塩酸塩錠) )は、感受性のある細菌によって引き起こされることが証明されているか、強く疑われる感染症を治療または予防するためにのみ使用する必要があります.培養および感受性の情報が利用可能である場合、それらは抗菌療法の選択または変更において考慮されるべきです。そのようなデータがない場合、地域の疫学および感受性パターンが治療の経験的選択に寄与する可能性があります。
テトラサイクリン塩酸塩は、次の感染症の治療に適応されます。
ロッキー山紅斑熱、チフス熱およびチフス群、Q熱、リケッチア痘およびリケッチアによるダニ熱。
肺炎マイコプラズマによる気道感染症
クラミジア・トラコマチスによるリンパ肉芽腫
Chlamydia psittaci によるオウム病および鳥類症
Chlamydia trachomatis によって引き起こされるトラコーマ。ただし、免疫蛍光によって判断されるように、感染性病原体は常に排除されるわけではありません。
クラミジア・トラコマチスによる封入体結膜炎
塩酸テトラサイクリンは、クラミジア・トラコマチスによって引き起こされる成人の合併症のない尿道、子宮頸部または直腸の感染症の治療に適応されます。
ウレアプラズマ・ウレアリチカムによる非淋菌性尿道炎 再発性ボレリアによる回帰熱
テトラサイクリン塩酸塩は、次のグラム陰性微生物によって引き起こされる感染症の治療にも適応されます。
Haemophilus ducreyi による下疳
エルシニア・ペスティス(以前のパスツレラ・ペスティス)によるペスト
Francisella tularensis (旧 Pasteurella tularensis) による野兎病
Vibrio cholerae (以前の Vibrio comma) によって引き起こされるコレラ
カンピロバクター胎児(旧ビブリオ胎児)によるカンピロバクター胎児感染症
ブルセラ種によるブルセラ症(ストレプトマイシンと併用)
バルトネラ菌によるバルトネラ症
カリマトバクテリウム・グラニュロマティスによる鼠径肉芽腫
以下の微生物群の多くの菌株はテトラサイクリン塩酸塩に耐性があることが示されているため、培養および感受性試験が推奨されます。
テトラサイクリン塩酸塩は、細菌学的検査で薬剤に対する適切な感受性が示された場合に、以下のグラム陰性微生物によって引き起こされる感染症の治療に適応されます。
大腸菌
エンテロバクター・エアロゲネス(以前のエアロバクター・エアロゲネス)
赤痢菌種
Acinetobacter 種 [旧 Mima 種および Herellea 種]
インフルエンザ菌による気道感染症
クレブシエラ菌による気道および尿路感染症
テトラサイクリン塩酸塩は、細菌学的検査で薬剤に対する適切な感受性が示された場合に、次のグラム陽性微生物によって引き起こされる感染症の治療に適応されます。
Streptococcus pneumoniae(以前の Diplococcus pneumoniae)による上気道感染症
黄色ブドウ球菌によって引き起こされる皮膚および皮膚構造の感染症。テトラサイクリン系薬剤は、あらゆる種類のブドウ球菌感染症の治療に最適な薬剤ではありません
ペニシリンが禁忌である場合、テトラサイクリン塩酸塩は、以下の感染症の治療における代替薬です。
Neisseria gonorrhoeae による合併症のない淋病
梅毒トレポネーマによる梅毒
Treponema pertenue によるヨーズ
リステリア・モノサイトゲネスによるリステリア症
炭疽菌による炭疽菌
Fusobacterium fusiforme による Vincent の感染症
Actinomyces israelii による放線菌症
クロストリジウム種による感染症
急性腸アメーバ症では、テトラサイクリン塩酸塩がアメーバ駆除剤の有用な補助療法となる可能性があります。
重度のにきびでは、テトラサイクリン塩酸塩が有用な補助療法となる場合があります。
投薬と管理
成人: 通常の 1 日量は 1 ~ 2 g です。重度の感染症には、500 mg qid などの高用量が必要になる場合があります。
8 歳以上の子供の場合:通常の 1 日量は、体重 1 ポンドあたり 10 ~ 20 mg (25 ~ 50 mg) を 4 等分します。
治療は、症状と発熱が治まってから少なくとも 24 ~ 48 時間継続する必要があります。
ブルセラ症の治療では、テトラサイクリン 500 mg を 1 日 4 回、3 週間投与するとともに、ストレプトマイシン 1 g を 1 日 2 回、最初の週は 1 日 2 回、2 週目は 1 日 1 回筋肉内投与する必要があります。
合併症のない淋病の治療には、500 mg を 6 時間ごとに 7 日間。
梅毒の治療では、10~15 日間にわたって、合計 30~40 g を均等に分割して投与する必要があります。臨床検査を含む綿密なフォローアップが推奨されます。
クラミジア・トラコマチスによる成人の合併症のない尿道、子宮頸部、または直腸の感染症: 経口で 500 mg、1 日 4 回、少なくとも 7 日間。
臨床医の判断で長期治療が必要な重度のにきびの場合、推奨される初回投与量は、1 日 1 g の分割投与です。通常 1 週間以内に改善が認められたら、1 日 125 ~ 500 mg の範囲の維持レベルまで、用量を徐々に減らしてください。一部の患者では、隔日または断続的な治療で病変の十分な寛解を維持できる場合があります。にきびのテトラサイクリン療法は、価値があることが知られている他の標準的な手段を強化する必要があります。
腎機能障害のある患者( 警告 総投与量は、推奨される個々の投与量を減らすか、および/または投与間の時間間隔を延ばして減らす必要があります。
レンサ球菌感染症の治療では、治療用量のテトラサイクリンを少なくとも 10 日間投与する必要があります。
併用療法: テトラサイクリンの吸収は、アルミニウム、カルシウム、またはマグネシウムを含む制酸剤、および鉄を含む製剤によって損なわれます。
食品や一部の乳製品も吸収を妨げます。
テトラサイクリンの錠剤、特にカプセル製剤で十分な量の液体を投与することは、薬を洗い流し、食道の刺激と潰瘍形成のリスクを減らすために推奨されます。 有害反応 )
供給方法
スマイシン®錠(テトラサイクリン塩酸塩錠USP)
保管所
錠剤は室温で保管してください。過度の熱を避ける。遮光性の密閉容器に分注してください。
製造元: Bristol-Myers Squibb Company、Princeton、NJ 08543 USA。製造元: Par Pharmaceutical, Inc. Spring Valley, NY 10977. USA。 03/04 改訂。 FDA 改訂日: 1997 年 7 月 22 日
副作用
胃腸: 食欲不振、上腹部痛、吐き気、嘔吐、下痢、かさばる軟便、口内炎、喉の痛み、舌炎、黒い毛むくじゃらの舌、嚥下障害、嗄声、腸炎、直腸炎や肛門そう痒症を含む肛門生殖器領域の炎症性病変(カンジダ過成長を伴う) .食道炎および食道潰瘍のまれな例は、特にカプセルおよびテトラサイクリンの錠剤形態を投与された患者で報告されています.ほとんどの患者は、就寝直前に薬を服用していると報告されています( 投薬と管理 )。これらの反応は、テトラサイクリンの経口および非経口投与の両方によって引き起こされていますが、非経口使用後は頻度が低くなります.
皮膚と皮膚の構造: 黄斑丘疹および紅斑性発疹。剥脱性皮膚炎が報告されていますが、一般的ではありません。爪の爪剥離および変色はまれに報告されています。光過敏症が発生しました。 (見る 警告 )。
腎毒性: BUN の増加が報告されており、明らかに用量に関連しています。 (見る 警告。 )
肝胆汁うっ滞: めったに報告されておらず、通常はテトラサイクリンの高用量レベルに関連しています。

過敏反応: アナフィラキシー;発熱、発疹、関節痛などの血清病様反応;蕁麻疹、血管神経性浮腫、アナフィラキシー様紫斑病、心膜炎、全身性エリテマトーデスの増悪。
血液学: 血液: 貧血、溶血性貧血、血小板減少症、血小板減少性紫斑病、好中球減少症、好酸球増加症が報告されています。
その他: めまいや頭痛が報告されています。
長期間にわたって投与された場合、テトラサイクリンは、甲状腺の黒褐色の顕微鏡的変色を引き起こすことが報告されています.甲状腺機能の異常が発生することは知られていません。乳児の泉門の隆起および成人の頭蓋内圧亢進が報告されています。 (見る 注意事項 - 一般。 )
薬物相互作用
ペニシリン -テトラサイクリンのような静菌薬はペニシリンの殺菌作用を妨げる可能性があるため、ペニシリンと一緒にテトラサイクリンを投与することは避けることをお勧めします.
抗凝固薬 -テトラサイクリンは血漿プロトロンビン活性を低下させることが示されているため、抗凝固療法を受けている患者は、抗凝固剤の投与量を下方調整する必要がある場合があります.
制酸剤と鉄含有製品 テトラサイクリンの吸収は、アルミニウム、カルシウム、またはマグネシウムを含む制酸剤、および鉄を含む製剤によって損なわれます。
経口避妊薬 -テトラサイクリンの同時使用は、経口避妊薬の効果を低下させる可能性があります。
メトキシフルラン -テトラサイクリンとメトキシフルランの同時使用は、致命的な腎毒性をもたらすと報告されています。
警告
テトラサイクリン系の抗生物質は、妊婦に投与すると胎児に害を及ぼす可能性があります。妊娠中にテトラサイクリンを使用する場合、またはこれらの薬を服用中に患者が妊娠した場合、患者は胎児への潜在的な危険性について知らされるべきです。
歯の発達期(妊娠後期、乳児期および8歳までの小児期)にテトラサイクリン系の薬剤を使用すると、永久的な歯の変色(黄色がかった灰色の茶色)を引き起こす可能性があります。
この有害反応は、薬物の長期使用中により一般的ですが、短期間の経過を繰り返した後に観察されています.エナメル質形成不全も報告されています。 したがって、テトラサイクリン系薬剤は、他の薬剤が効果的である可能性が低いか、または禁忌でない限り、歯の発達中に使用すべきではありません.
すべてのテトラサイクリンは、骨形成組織で安定したカルシウム複合体を形成します。 6 時間ごとに 25 mg/kg の用量で経口テトラサイクリンを与えられた若い動物 (ラットおよびウサギ) で、腓骨の成長速度の低下が観察されています。この反応は、薬を中止すると元に戻ることが示されました。
動物研究の結果は、テトラサイクリンが胎盤を通過し、胎児組織に見られ、発達中の胎児に毒性作用を及ぼす可能性があることを示しています(多くの場合、骨格発達の遅延に関連しています).胚毒性の証拠は、妊娠初期に治療された動物にも見られます。
テトラサイクリンの抗アナボリック作用により、BUN が増加する可能性があります。これは腎機能が正常な人には問題ありませんが、腎機能が著しく低下している患者では、テトラサイクリンの血清レベルが高いと、高窒素血症、高リン血症、およびアシドーシスにつながる可能性があります。腎障害が存在する場合、通常の経口または非経口投与でも、薬物の過剰な全身蓄積および肝臓毒性の可能性につながる可能性があります。このような条件下では、通常よりも低い用量が指示され、治療が長引く場合は、薬物の血清レベルの測定が推奨される場合があります.
誇張された日焼け反応によって明らかにされる光過敏症は、テトラサイクリンを服用している一部の個人で観察されています.直射日光や紫外線にさらされる傾向のある患者は、テトラサイクリン系薬剤でこの反応が起こる可能性があることを知らされ、皮膚の紅斑の最初の兆候が見られたら治療を中止する必要があります。
注: 光増感反応は、デメクロサイクリンで最も頻繁に発生し、クロルテトラサイクリンでは少なく、オキシテトラサイクリンとテトラサイクリンではほとんど発生しません。
予防
全般的
証明された、または強く疑われる細菌感染がない場合、または予防適応症がない場合に、スマイシン '250' およびスマイシン '500' 錠剤 (テトラサイクリン塩酸塩錠剤) を処方することは、患者に利益をもたらす可能性が低く、薬剤耐性の発生のリスクを高めます。バクテリア。
他の抗生物質と同様に、この薬を使用すると、真菌を含む非感受性生物の異常増殖を引き起こす可能性があります.重複感染が発生した場合は、抗生物質の使用を中止し、適切な治療を開始する必要があります。注: ブドウ球菌による腸の重複感染は生命を脅かす可能性があります。
成人における偽大脳腫瘍(良性頭蓋内圧亢進症)は、テトラサイクリンの使用に関連しています。通常の臨床症状は、頭痛とかすみ目です。膨らんだフォンタネルは、乳児におけるテトラサイクリンの使用に関連しています。これらの状態と関連する症状は通常、テトラサイクリンの中止後に解決しますが、永久的な後遺症の可能性が存在します.
アレルギー、ぜんそく、花粉症、蕁麻疹などの既往歴のある人は過敏症を起こしやすいので、慎重に使用すること。
さまざまなテトラサイクリン間の交差感作は非常に一般的です。
必要に応じて、切開排膿またはその他の外科的処置を抗生物質療法と併用して実施する必要があります。
テトラサイクリンの分解は非常に腎毒性があり、場合によってはファンコニー様症候群を引き起こすため、どのような状況においても時代遅れのテトラサイクリンを投与すべきではありません.
臨床検査
長期治療中は、腎臓、肝臓、および造血系を含む臓器系機能の定期的な臨床検査を実施する必要があります。
淋病のすべての患者は、診断時に梅毒の血清学的検査を受ける必要があります。テトラサイクリンで治療された患者は、3 か月後に梅毒のフォローアップ血清学的検査を受ける必要があります。
発がん、突然変異誘発、生殖能力の障害
テトラサイクリン塩酸塩に発がん性があるかどうかを判断するためにラットとマウスで実施された長期研究は陰性でした。いくつかの関連する抗生物質 (オキシテトラサイクリン、ミノサイクリン) は、ラットにおける発癌活性の証拠を示しています。 2 つの in vitro 哺乳動物細胞アッセイ系 (L51784y マウスリンパ腫およびチャイニーズハムスター肺細胞) では、それぞれ 60 および 10 μg/mL のテトラサイクリン塩酸塩濃度で変異原性の証拠がありました。
テトラサイクリン塩酸塩は、ヒト用量の 25 倍の 1 日摂取量で雌雄ラットに混餌投与した場合、生殖能力に影響を与えませんでした。
妊娠: 催奇形性効果: 妊娠カテゴリーD(参照 警告。 )
妊娠: 非催奇形性の影響: (見る 警告。 )
労働と配達
陣痛および分娩に対するテトラサイクリンの影響は不明です。
授乳中の母親
テトラサイクリンは、このクラスの薬を服用している授乳中の女性の母乳に含まれています.授乳中の乳児にテトラサイクリンによる重篤な副作用が生じる可能性があるため、母親にとっての薬剤の重要性を考慮して、授乳を中止するか薬剤を中止するかを決定する必要があります。 警告 .)
小児用
見る 警告 と 投薬と管理。
過剰摂取
過剰摂取の場合は、対症療法を行い、補助措置を講じてください。
禁忌
この薬は、テトラサイクリンのいずれかに過敏症を示した人には禁忌です。
臨床薬理学
テトラサイクリンは胃腸管から十分に吸収されますが、完全には吸収されません。短時間作用型テトラサイクリンの約 65% が血漿タンパク質に結合します。中間作用型および長時間作用型類似体の血漿タンパク質結合は、通常、より大きくなります。
ほとんどの体液および組織へのテトラサイクリンの浸透は優れています。テトラサイクリンは、胆汁、肝臓、肺、腎臓、前立腺、尿、脳脊髄液、滑液、上顎洞の粘膜、脳、喀痰、および骨にさまざまな程度で分布しています。テトラサイクリンは胎盤を通過し、胎児循環と羊水に入ります。
1 回の経口投与後、2 ~ 4 時間で最高の血漿中濃度に達します。
テトラサイクリンは肝臓で胆汁に濃縮されます。それらは、生物学的に活性な形で高濃度で尿と糞の両方に排泄されます。テトラサイクリンの腎クリアランスは糸球体濾過によるものであるため、排泄は腎機能の状態に大きく影響されます。 (見る 警告。 )
微生物学
テトラサイクリンは主に静菌性であり、タンパク質合成の阻害によって抗菌効果を発揮すると考えられています。テトラサイクリンは、広範囲のグラム陽性菌およびグラム陰性菌に対して同様の抗菌スペクトルを持っています。これらの生物のテトラサイクリンに対する交差耐性は一般的です。さらに、テトラサイクリン耐性にされたグラム陰性桿菌は、クロラムフェニコールに対しても交差耐性を示す可能性があります。
グラム陰性菌:
バルトネラ・バチルス・ブルセラ種 カリマトバクテリウム・グラニュロマチス カンピロバクター・フェタス フランシセラ・ツラレンシス ヘモフィルス・デュクレイイ ヘモフィルス・インフルエンザ リステリア・モノサイトゲネス ナイセリア・ゴノロエエ ビブリオ・コレラエ エルシニア・ペスティス
以下のグラム陰性微生物グループの多くの菌株がテトラサイクリン耐性であることが示されているため、培養および感受性試験が特に推奨されます。
Acinetobacter 種 Bacteroides 種 Enterobacter aerogenes Escherichia coli Klebsiella 種 Shigella 種
グラム陽性菌:
エンテロコッカスグループ [Enterococcus faecalis (以前の Streptococcus faecalis) および Enterococcus faecium (以前の Streptococcus faecium)
Streptococci viridans グループ Streptococcus pneumoniae Streptococcus pyogenes
これらのグラム陽性微生物の多くの菌株はテトラサイクリンに耐性があることが示されているため、培養および感受性試験が推奨されます。 Streptococcus pyogenes の最大 44% の菌株と、Enterococcus faecalis (以前の Streptococcus faecalis) の最大 74% が、テトラサイクリン系薬剤に耐性があることがわかっています。したがって、テトラサイクリンは、その微生物が感受性であることがわかっていない限り、レンサ球菌疾患の治療に使用すべきではありません.
その他の微生物:
Actinomyces 種 Bacillus anthracis Balantidium coli Balantidium coli Borrelia recurrentis Chlamydia psittaci Chlamydia trachomatis Clostridium 種 Entamoeba 種 Fusobacterium fusiforme Mycoplasma pneumoniae Rickettsiae プロピオニバクテリウム アクネス Treponema pallidum Treponema pertenue Ureaplasma urealyticum
感受性試験
拡散テクニック
ゾーンの直径の測定を必要とする定量的方法は、抗菌剤に対する細菌の感受性を最も正確に推定します。
テトラサイクリンに対する微生物の感受性をテストするためにディスクを使用することが推奨されている標準手順の 1 つは、30 mcg のテトラサイクリン ディスクを使用します。解釈には、ディスク試験で得られたゾーン直径とテトラサイクリンの最小発育阻止濃度 (MIC) との相関関係が含まれます。
30 mcg テトラサイクリン ディスクを使用した標準的な単一ディスク感受性試験の結果を示す検査室からのレポートは、次の基準に従って解釈する必要があります。
「感受性」のレポートは、病原体が一般的に達成可能な血中濃度によって抑制される可能性が高いことを示します。 「中間」の報告は、高用量が使用された場合、または感染が高い抗生物質 (または抗菌剤) レベルに達した組織または体液に限定されている場合、生物が感受性になることを示唆しています。 「耐性」のレポートは、達成可能な濃度が阻害される可能性が低く、他の治療法を選択する必要があることを示しています。
標準化された手順では、実験室の制御生物を使用する必要があります。 30 mcg テトラサイクリン ディスクは、次のゾーン直径を与える必要があります。
希釈法
標準化された希釈法 2 (培養液、寒天、微量希釈) またはテトラサイクリン粉末と同等のものを使用します。得られた MIC 値は、次の基準に従って解釈する必要があります。
標準的な拡散技術と同様に、希釈法では実験室の制御生物を使用する必要があります。標準的なテトラサイクリン粉末は、次の MIC 値を提供する必要があります。
動物薬理学・動物毒物学
甲状腺の色素沈着過剰は、次の種のテトラサイクリン クラスのメンバーによって生成されています。ドキシサイクリン、ミノサイクリン、テトラサイクリン PO4 およびメタサイクリンによるミニブタ。犬ではドキシサイクリンとミノサイクリンによる。ミノサイクリンによるサル。
ミノサイクリン、テトラサイクリン PO4、メタサイクリン、ドキシサイクリン、テトラサイクリン塩基、オキシテトラサイクリン HCl、およびテトラサイクリン HCl は、低ヨウ素食を与えられたラットで甲状腺腫誘発性でした。このゴイトロジェニック効果は、高い放射性ヨウ素の取り込みを伴いました。ミノサイクリンの投与はまた、比較的高いヨウ素食を与えられたラットに放射性ヨウ素の取り込みが高い大きな甲状腺腫を生じさせた.
このクラスの薬物でさまざまな動物種を治療すると、ラットとイヌ (ミノサイクリン)、ニワトリ (クロルテトラサイクリン)、ラットとマウス (オキシテトラサイクリン) で甲状腺過形成が誘発されます。副腎過形成は、オキシテトラサイクリンで治療されたヤギおよびラットで観察されています。
参照
1. National Committee for Clinical Laboratory Standards、抗菌ディスク感受性試験の性能基準 - 第 4 版。承認済み標準 NCCLS ドキュメント M2-A4、Vol. 10、No. 7 NCCLS、ペンシルベニア州ヴィラノバ、1990 年 4 月。
2. 全米臨床検査基準委員会、好気的に増殖する細菌の希釈抗菌剤感受性試験方法 - 第 2 版。承認済み標準 NCCLS ドキュメント M7-A2、Vol. 10、No. 8 NCCLS、ペンシルベニア州ヴィラノバ、1990 年 4 月。
患者情報
スマイシン '250' およびスマイシン '500' タブレット (テトラサイクリン塩酸塩タブレット) を含む抗菌薬は、細菌感染症の治療にのみ使用する必要があることを患者に説明する必要があります。ウイルス感染症(風邪など)は治療しません。スマイシン '250' およびスマイシン '500' タブレット (テトラサイクリン塩酸塩タブレット) が細菌感染症の治療に処方される場合、患者は、治療過程の早い段階で気分が良くなるのが一般的ですが、薬は正確に服用する必要があることを伝えなければなりません。監督。投与をスキップしたり、治療の完全なコースを完了しないと、(1) 即時治療の有効性が低下し、(2) 細菌が耐性を獲得し、スマイシン '250' およびスマイシン '500' 錠剤で治療できなくなる可能性が高くなります (テトラサイクリン塩酸塩錠)またはその他の抗菌薬を将来的に使用する予定です。
