Keflex 250mg, 500mg Cephalexin 使用法、副作用および投与量。 オンライン薬局の価格。 処方箋不要のジェネリック医薬品。
Keflex 250mg とは何ですか?
Keflex は、細菌の増殖を止めることによって、さまざまな細菌感染症の症状を治療するために使用される処方薬です。 Keflex 500mg は、単独で使用することも、他の薬と併用することもできます。
Keflex は、セファロスポリン系抗生物質として知られています。
ケフレックスの副作用は何ですか?
Keflex は、次のような重大な副作用を引き起こす可能性があります。
- 激しい胃痛、
- 水様または血様の下痢、
- 異常な疲労感
- ふらつきや息切れを感じたり、
- あざができやすい、
- 不正出血、
- 皮膚の下の紫または赤の斑点、
- 発作、
- 薄い肌、
- 手足の冷え、
- 皮膚の黄ばみ、尿の色の濃さ、
- 熱、
- 弱点 ,
- 脇腹や腰の痛み、
- 排尿痛、
上記の症状がある場合は、すぐに医療機関を受診してください。
Keflex 500mg の最も一般的な副作用は次のとおりです。
- 下痢、
- 吐き気、
- 嘔吐、
- 消化不良、
- 胃痛、
- 膣のかゆみや分泌物、
気になる副作用や治らない副作用がある場合は、医師に相談してください。
これらは、Keflex の考えられるすべての副作用ではありません。詳細については、医師または薬剤師にお尋ねください。
副作用に関する医学的アドバイスについては、医師に連絡してください。 1-800-FDA-1088 で副作用を FDA に報告できます。
説明
KEFLEX® (セファレキシン) カプセル、USP は、経口投与を目的とした半合成セファロスポリン抗菌薬です。 7-(D-α-アミノ-α-フェニルアセトアミド)-3-メチル-3-セフェム-4-カルボン酸一水和物です。セファレキシンの分子式は C16H17N3O4S•H2O で、分子量は 365.41 です。
セファレキシンの構造式は次のとおりです。
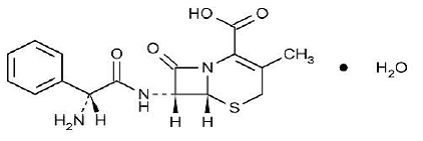
各カプセルには、250 mg、500 mg、または 750 mg のセファレキシンに相当するセファレキシン一水和物が含まれています。カプセルには、カルボキシメチルセルロース ナトリウム、D&C 黄色 10 号、ジメチコン、FD&C 青色 1 号、FD&C 黄色 6 号、ゼラチン、ステアリン酸マグネシウム、微結晶性セルロース、および二酸化チタンも含まれています。
適応症
気道感染症
KEFLEX は、肺炎連鎖球菌および化膿性連鎖球菌の感受性分離株によって引き起こされる気道感染症の治療に適応されます。
中耳炎
KEFLEX は、肺炎連鎖球菌、インフルエンザ菌、黄色ブドウ球菌、化膿連鎖球菌、およびモラクセラ・カタラーリスの感受性分離株によって引き起こされる中耳炎の治療に適応されます。
皮膚および皮膚構造の感染症
KEFLEX 250mg は、以下のグラム陽性菌の感受性分離株によって引き起こされる皮膚および皮膚構造の感染症の治療に適応されます: 黄色ブドウ球菌および化膿連鎖球菌。
骨の感染症
KEFLEX 250mg は、黄色ブドウ球菌およびプロテウス ミラビリスの感受性分離株によって引き起こされる骨感染症の治療に適応されます。
泌尿生殖器感染症
KEFLEX は、大腸菌、プロテウス・ミラビリス、およびクレブシエラ・ニューモニエの感受性分離株によって引き起こされる、急性前立腺炎を含む泌尿生殖器感染症の治療に適応されます。
使用法
薬剤耐性菌の発生を減らし、ケフレックス 250mg および他の抗菌薬の有効性を維持するために、ケフレックス 500mg は、感受性のある細菌によって引き起こされることが証明されている、または強く疑われる感染症の治療にのみ使用する必要があります。培養と感受性の情報が利用可能である場合、この情報は抗菌療法を選択または修正する際に考慮されるべきです。そのようなデータがない場合、地域の疫学および感受性パターンが治療の経験的選択に寄与する可能性があります。
投薬と管理
15歳以上の成人および小児患者
経口ケフレックス 250mg の通常の投与量は 6 時間ごとに 250mg ですが、12 時間ごとに 500mg を投与することもできます。治療は7〜14日間行われます。
より重篤な感染症の場合は、2 回から 4 回に分けて 1 日最大 4 グラムの経口 KEFLEX を大量に服用する必要があります。
小児患者(1歳以上)
小児患者に推奨される経口 KEFLEX 500mg の 1 日総投与量は、25 ~ 50 mg/kg を 7 ~ 14 日間均等に分割して投与します。 β溶血性レンサ球菌感染症の治療では、少なくとも10日間の継続が推奨されています。重度の感染症では、1 日あたり 50 ~ 100 mg/kg の総量を均等に分割して投与できます。
中耳炎の治療の場合、1 日あたりの推奨用量は 75 ~ 100 mg/kg を均等に分割して投与します。
腎障害のある少なくとも15歳の成人および小児患者における用量調整
腎機能障害のある患者には、以下の KEFLEX の投与レジメンを投与する [参照 警告と注意事項 と 特定の集団での使用 ]。
供給方法
剤形と強度
250mgカプセル: 白色から淡黄色の粉末で、白色の本体に食用黒色インクで KEFLEX 250 mg が刻印された不透明な白色および不透明な濃い緑色のカプセルに充填されています。
500mgカプセル: 白色から淡黄色の粉末が不透明な薄緑色および不透明な暗緑色のカプセルに充填されており、薄緑色の本体に食用黒色インクで KEFLEX 500 mg が刻印されています。
750 mg カプセル: 白色から淡黄色の粉末が細長い不透明な濃い緑色と不透明な濃い緑色のカプセルに充填されており、濃い緑色の本体に食用の白色インクで KEFLEX 750 mg と刻印されています。
保管と取り扱い
ケフレックス(セファレキシン)カプセル 、USP は、次のように提供されます。
250mgカプセル、100本入りボトル NDC 59630-112-10 500mgカプセル、100本入りボトル – NDC 59630-113-10 750 mg カプセル、50 個入りボトル – NDC 59630-115-05
KEFLEX は 25°C (77°F) で保管してください。 15° から 30°C (59° から 86°F) まで許容されるエクスカーション [参照 USP制御の室温 ]。
遮光性の密閉容器に分注してください。
製造元: Shionogi Inc. Florham Park, NJ 07932. 製造元: Sandoz GmbH Kundl, Austria.改訂: 2015 年 10 月。
副作用
次の重大なイベントについては、「警告と予防措置」セクションで詳しく説明しています。
- 過敏反応 [参照 警告と注意事項 ]
- クロストリジウム・ディフィシル関連の下痢[参照 警告と注意事項 ]
- Direct Coombs' Test Seroconversion [参照 警告と注意事項 ]
- 発作の可能性 [参照 警告と注意事項 ]
- プロトロンビン活性への影響 [参照 警告と注意事項 ]
- 薬剤耐性菌の発生 [参照 警告と注意事項 ]
臨床試験の経験
臨床試験はさまざまな条件下で実施されるため、ある医薬品の臨床試験で観察された副作用率を別の医薬品の臨床試験で観察された率と直接比較することはできず、実際に観察された率を反映していない可能性があります。
臨床試験では、最も頻繁に見られた副作用は下痢でした。吐き気と嘔吐、消化不良、胃炎、腹痛も発生しています。ペニシリンや他のセファロスポリンと同様に、一過性肝炎や胆汁うっ滞性黄疸が報告されています。
その他の反応には、過敏症反応、性器および肛門の掻痒、性器カンジダ症、膣炎および膣分泌物、めまい、疲労、頭痛、動揺、錯乱、幻覚、関節痛、関節炎、および関節障害が含まれます.可逆性間質性腎炎が報告されています。好酸球増加症、好中球減少症、血小板減少症、溶血性貧血、およびアスパラギン酸トランスアミナーゼ (AST) およびアラニントランスアミナーゼ (ALT) のわずかな上昇が報告されています。
KEFLEX 500mgで治療された患者で観察された上記の副作用に加えて、セファロスポリンクラスの抗菌薬について、次の副作用およびその他の実験室試験の変更が報告されています。
その他の有害反応
発熱、大腸炎、再生不良性貧血、出血、腎機能障害、中毒性腎症。
実験室試験の変更
プロトロンビン時間の延長、血中尿素窒素 (BUN) の増加、クレアチニンの増加、アルカリホスファターゼの上昇、ビリルビンの上昇、乳酸脱水素酵素 (LDH) の上昇、汎血球減少症、白血球減少症、および無顆粒球症。
薬物相互作用
メトホルミン
メトホルミンと一緒に KEFLEX 250mg を投与すると、血漿メトホルミン濃度が上昇し、メトホルミンの腎クリアランスが減少します。
KEFLEX とメトホルミンを併用している患者では、慎重な患者モニタリングとメトホルミンの用量調整が推奨される [ 臨床薬理学 ]。
プロベネシド
KEFLEX の腎排泄は、プロベネシドによって阻害されます。プロベネシドと KEFLEX 500mg の併用は推奨されません。
臨床検査または診断検査との相互作用
ベネディクト液またはフェーリング液を使用して尿中のブドウ糖の存在を検査すると、偽陽性反応が発生することがあります。
警告
の一部として含まれています 予防 セクション。
予防
過敏反応
発疹、蕁麻疹、血管性浮腫、アナフィラキシー、多形紅斑、スティーブンス・ジョンソン症候群、中毒性表皮壊死症などのアレルギー反応が KEFLEX の使用により報告されています。 KEFLEX 500mg による治療を開始する前に、患者にセファレキシン、セファロスポリン、ペニシリン、またはその他の薬物に対する過敏反応の既往があるかどうかを尋ねてください。ペニシリンアレルギーの病歴を持つ患者の最大 10% で、β-ラクタム系抗菌薬間の交差過敏症が発生する可能性があります。
KEFLEX 500mg に対するアレルギー反応が発生した場合は、薬剤の使用を中止し、適切な治療を受けてください。
クロストリジウム・ディフィシル関連下痢症
クロストリジウム・ディフィシル関連下痢症 (CDAD) は、KEFLEX 500mg を含むほぼすべての抗菌薬の使用で報告されており、軽度の下痢から致命的な大腸炎までの重症度に及ぶ可能性があります。抗菌剤による治療は、結腸の正常な細菌叢を変化させ、C. difficile の異常増殖を引き起こします。
C. difficile は、CDAD の発症に寄与する毒素 A および B を産生します。 C. difficile の高毒素産生株は、これらの感染症が抗菌療法に抵抗性であり、結腸切除術を必要とする可能性があるため、罹患率と死亡率の増加を引き起こします。抗生物質の使用後に下痢を呈するすべての患者で、CDAD を考慮する必要があります。 CDADは抗菌薬投与後2か月以上経過すると報告されているため、病歴には注意が必要です。
CDAD が疑われるか確認された場合、C. difficile に対するものではない継続的な抗生物質の使用を中止する必要があるかもしれません。適切な体液と電解質の管理、タンパク質の補給、C. difficile の抗生物質治療、および外科的評価を、臨床的に必要な場合に開始する必要があります。
Direct Coombs' Test Seroconversion
セファレキシンを含むセファロスポリン抗菌薬による治療中に、陽性の直接クームス試験が報告されています。セファレキシン療法によって誘発される急性血管内溶血が報告されています。セファレキシン治療中または治療後に貧血が発症した場合は、薬剤性溶血性貧血の診断的精密検査を行い、セファレキシンを中止し、適切な治療を開始してください。
発作の可能性
いくつかのセファロスポリンは、特に投与量が減らされなかった場合に腎障害のある患者で発作を引き起こすことに関与しています.発作が起きた場合は、KEFLEX を中止してください。臨床的に必要な場合は、抗けいれん療法を行うことができます。
プロトロンビン時間の延長
セファロスポリンは、延長されたプロトロンビン時間と関連している可能性があります。危険にさらされている患者には、腎臓または肝臓の機能障害、または栄養状態の悪い患者、長期にわたる抗菌療法を受けている患者、および抗凝固療法を受けている患者が含まれます。リスクのある患者のプロトロンビン時間を監視し、指示に従って管理します。
薬剤耐性菌の発生
証明された、または強く疑われる細菌感染がない場合に KEFLEX を処方すると、患者に利益がもたらされる可能性は低く、薬剤耐性菌が発生するリスクが高まります。
KEFLEX を長期間使用すると、感受性のない微生物が増殖する可能性があります。患者の注意深い観察が不可欠です。治療中に重複感染が発生した場合は、適切な対策を講じる必要があります。
非臨床毒性学
発がん、突然変異誘発、生殖能力の障害
セファレキシンの発がん性を評価するための動物での生涯試験は実施されていません。セファレキシンの変異原性を決定するための試験は実施されていません。オスとメスのラットでは、体表面積に基づいた最高推奨用量の 1.5 倍までのセファレキシンの経口用量によって、繁殖力と生殖能に影響はありませんでした。
特定の集団での使用
妊娠
妊娠カテゴリーB
妊娠中の女性を対象とした、十分に管理された研究はありません。動物の繁殖研究は常に人間の反応を予測できるわけではないため、この薬は明らかに必要な場合にのみ妊娠中に使用する必要があります.
生殖研究は、体表面積に基づいて、人間の 1 日最大用量 (66 mg/kg/日) の 0.6 倍および 1.5 倍の経口用量のセファレキシン一水和物を使用して、マウスおよびラットで実施されました。胎児。
授乳中の母親
セファレキシンは母乳中に排泄されます。 KEFLEX を授乳中の女性に投与する場合は注意が必要です。
小児用
小児患者における KEFLEX 500mg の安全性と有効性は、用法・用量のセクションに記載されている用量の臨床試験で確立されています。 投薬と管理 ]。
高齢者の使用
セファレキシンの 3 つの公開された臨床研究の 701 人の被験者のうち、433 人 (62%) が 65 歳以上でした。これらの被験者と若い被験者の間で安全性または有効性の全体的な違いは観察されず、他の報告された臨床経験では、高齢者と若い患者の間の反応の違いは確認されていません.
この薬は実質的に腎臓から排泄され、この薬に対する毒性反応のリスクは、腎機能が低下している患者で大きくなる可能性があります。高齢者は腎機能が低下している可能性が高いため、用量選択には注意が必要です。 警告と注意事項 ]。
腎障害
KEFLEX は、腎機能障害がある場合 (クレアチニンクリアランス 投薬と管理 ]。
参考文献
1. Clinical and Laboratory Standards Institute (CLSI)。好気的に増殖する細菌の希釈抗菌薬感受性試験の方法;承認された標準 - 第 10 版。 CLSI ドキュメント M07-A10、Clinical and Laboratory Standards Institute、950 West Valley Road、Suite 2500、Wayne、Pennsylvania 19087、USA、2015。
2. Clinical and Laboratory Standards Institute (CLSI)。抗菌薬感受性試験の性能基準;第 25 情報補足。 CLSI ドキュメント M100-S25、Clinical and Laboratory Standards Institute、950 West Valley Road、Suite 2500、Wayne、Pennsylvania 19087、USA、2015。
3. Clinical and Laboratory Standards Institute (CLSI)。抗菌性ディスク感受性試験の性能基準;承認された標準 - 第 12 版。 CLSI ドキュメント M02-A12、Clinical and Laboratory Standards Institute、950 West Valley Road、Suite 2500、Wayne、Pennsylvania 19087、USA、2015。
過剰摂取
経口過剰摂取の症状には、吐き気、嘔吐、上腹部痛、下痢、血尿などがあります。過剰摂取の場合は、一般的な支援策を講じてください。
強制利尿、腹膜透析、血液透析、またはチャコール血液灌流は、セファレキシンの過剰摂取に有益であると確立されていません。
禁忌
KEFLEX は、セファレキシンまたは抗菌薬のセファロスポリン クラスの他のメンバーに対して既知の過敏症を持つ患者には禁忌です。
臨床薬理学
作用機序
セファレキシンはセファロスポリン系抗菌薬です。 微生物学 ]。
薬物動態
吸収
セファレキシンは酸に安定しており、食事に関係なく投与できます。 250 mg、500 mg、および 1 g の用量で、それぞれ約 9、18、および 32 mcg/mL の平均ピーク血清レベルが 1 時間で得られました。血清レベルは、投与後 6 時間で検出可能でした (0.2 mcg/mL の検出レベル)。
分布
セファレキシンは、約 10% から 15% が血漿タンパク質に結合しています。
排泄
セファレキシンは、糸球体濾過と尿細管分泌によって尿中に排泄されます。研究によると、薬物の 90% 以上が 8 時間以内に変化せずに尿中に排泄されました。この期間中、250 mg、500 mg、および 1 g の投与後のピーク尿中濃度は、それぞれ約 1000、2200、および 5000 mcg/mL でした。
薬物相互作用
セファレキシンとメトホルミンを 500 mg 単回投与した健康な被験者では、血漿メトホルミン平均 Cmax と AUC がそれぞれ平均 34% と 24% 増加し、メトホルミン平均腎クリアランスは 14% 減少しました。いずれかの薬物を複数回投与した後のセファレキシンとメトホルミンの相互作用に関する情報は入手できません。
微生物学
作用機序
セファレキシンは、細菌の細胞壁合成を阻害することによって作用する殺菌剤です。
抵抗
メチシリン耐性ブドウ球菌および腸球菌のほとんどの分離株は、セファレキシンに耐性があります。 Cephalexin は、Enterobacter spp.、Morganella morganii、および Proteus vulgaris のほとんどの分離株に対して活性がありません。セファレキシンは、シュードモナス種またはアシネトバクター・カルコアセチカスに対して活性を有しません。ペニシリン耐性肺炎連鎖球菌は、通常、ベータラクタム系抗菌薬に対して交差耐性があります。
抗菌活性
セファレキシンは、in vitro および臨床感染の両方で、以下の細菌のほとんどの分離株に対して活性があることが示されています [参照 適応症と使用法 ]。
グラム陽性菌
黄色ブドウ球菌 (メチシリン感受性分離株のみ) 肺炎連鎖球菌 (ペニシリン感受性分離株) 化膿連鎖球菌
グラム陰性菌
大腸菌 インフルエンザ菌 肺炎桿菌 モラクセラ・カタラーリス プロテウス・ミラビリス
感受性試験方法
利用可能な場合、臨床微生物検査室は、院内および市中感染病原体の感受性プロファイルを説明する定期報告として、常駐病院で使用される抗菌薬製品の in vitro 感受性試験の結果を医師に提供する必要があります。これらのレポートは、医師が治療用の抗菌薬を選択するのに役立つはずです。
合併症のない尿路感染症のみの場合、大腸菌、肺炎桿菌、ミラビリス菌のセファレキシンに対する感受性は、セファゾリンを検査することで推測できます2。
希釈法
定量的方法は、抗菌剤の最小発育阻止濃度 (MIC) を決定するために使用されます。これらの MIC は、抗菌化合物に対する細菌の感受性の推定値を提供します。 MIC は、標準化された試験方法 (培養液または寒天) を使用して決定する必要があります 1,2。
拡散テクニック
ゾーンの直径の測定を必要とする定量的方法も、抗菌化合物に対する細菌の感受性の再現可能な推定値を提供します。ゾーンのサイズは、抗菌化合物に対する細菌の感受性の推定値を提供します。ゾーンのサイズは、標準化されたテスト方法を使用して決定する必要があります2,3。
Susceptible (S) のレポートは、抗菌薬が感染部位で通常達成可能な濃度に達すると、抗菌薬が病原体の増殖を阻害する可能性が高いことを示しています。中間 (I) のレポートは、結果が曖昧であると見なされるべきであることを示しており、微生物が代替の臨床的に実現可能な薬剤に完全に感受性でない場合、試験を繰り返す必要があります。このカテゴリーは、薬物が生理学的に集中している身体部位、または高用量の薬物を使用できる状況での臨床応用の可能性を示唆しています。このカテゴリは、制御されていない小さな技術的要因が解釈に大きな矛盾を引き起こすのを防ぐ緩衝地帯も提供します。 Resistant (R) のレポートは、抗菌薬が感染部位で通常達成可能な濃度に達した場合、抗菌薬が病原体の増殖を阻害する可能性が低いことを示しています。他の治療法を選択する必要があります。
品質管理
標準化された感受性試験手順では、実験室での管理を使用して、アッセイで使用される消耗品と試薬の精度と精度、および試験を実施する個人の技術を監視および確認する必要があります1,2,3。
患者情報
- 深刻なアレルギー反応を含むアレルギー反応が発生する可能性があり、深刻な反応には直ちに治療が必要であることを患者に伝えてください。 KEFLEX、他のベータラクタム(セファロスポリンを含む)または他のアレルゲンに対する以前の過敏症反応について患者に尋ねる
- 下痢は抗菌薬によって引き起こされる一般的な問題であり、通常は薬を中止すると解決することを患者にアドバイスします。時々、水様または血様の下痢が頻繁に発生することがあり、より深刻な腸感染症の徴候である可能性があります.重度の水様性または血性下痢が発生した場合は、医療提供者に連絡するよう患者にアドバイスしてください。
- KEFLEX を含む抗菌薬は、細菌感染症の治療にのみ使用するよう患者に助言してください。ウイルス感染症(風邪など)は治療しません。細菌感染症の治療に KEFLEX 500mg を処方する場合は、治療の初期に気分が良くなるのが一般的ですが、指示どおりに服用する必要があることを患者に伝えてください。投与をスキップしたり、治療の全コースを完了しないと、(1) 当面の治療の有効性が低下し、(2) 細菌が耐性を獲得し、将来的に KEFLEX や他の抗菌薬で治療できなくなる可能性が高くなる可能性があります。
