Flagyl 200mg, 400mg Metronidazole 使用法、副作用および投与量。 オンライン薬局の価格。 処方箋不要のジェネリック医薬品。
フラジールとは何ですか?
フラジールは、膣、胃、肝臓、皮膚、関節、脳、気道の細菌感染の症状を治療するために使用される処方薬です。フラジールは、単独で使用することも、他の薬と併用することもできます。
フラジールは、中程度のニトロイミダゾール、CYP3A4 阻害剤です。
フラジール 200mg の副作用の可能性は何ですか?
フラジール 400mg は、次のような重大な副作用を引き起こす可能性があります。
- 下痢、
- 痛みや排尿困難、
- 寝られない、
- うつ、
- 過敏症、
- 頭痛、
- めまい
- 弱点、
- 立ちくらみ、
- 口の中の水ぶくれや潰瘍、
- 歯ぐきが赤くなったり、腫れたり、
- 嚥下障害
次のようなフラジールの重大な副作用が発生した場合は、医師に相談してください。
- しびれ、
- チクチクする、
- 手や足の焼けるような痛み、
- 視力の問題、
- 目の奥の痛み、
- 閃光や光を見て、
- 筋力低下、
- 調整の難しさ、
- あなたに言われたことを話したり理解したりするのに苦労する、
- 発作、
- 熱、
- 首の凝りと、
- 光に対する感度の向上
上記の症状がある場合は、すぐに医療機関を受診してください。
これらは、フラジールの考えられるすべての副作用ではありません。詳細については、医師または薬剤師にお尋ねください。
副作用に関する医学的アドバイスについては、医師に連絡してください。 1-800-FDA-1088 で副作用を FDA に報告できます。
薬剤耐性菌の発生を抑え、FLAGYL® やその他の抗菌薬の有効性を維持するために、FLAGYL® は、細菌が原因であることが証明されている、または強く疑われる感染症の治療または予防にのみ使用してください。
警告
メトロニダゾールは、マウスとラットで発がん性があることが示されています ( 予防 )。薬の不必要な使用は避けるべきです。その使用は、 適応症と使用法 以下のセクション。
説明
FLAGYL (メトロニダゾール) 錠剤、250 mg または 500 mg は、合成ニトロイミダゾール抗菌剤、2-メチル-5-ニトロ-1H-イミダゾール-1-エタノールの経口製剤であり、次の構造式を持っています。
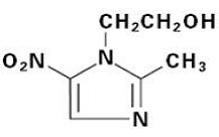
FLAGYL (メトロニダゾール) 錠剤には、250 mg または 500 mg のメトロニダゾールが含まれています。不活性成分には、セルロース、FD&C Blue No. 2 Lake、ヒドロキシプロピルセルロース、ヒプロメロース、ポリエチレングリコール、ステアリン酸、および二酸化チタンが含まれます。
適応症
症候性トリコモナス症。 FLAGYL は、トリコモナスの存在が適切な検査手順 (湿潤塗抹標本および/または培養) によって確認された場合に、女性および男性の膣 T. 感染症の治療に適応されます。
無症候性トリコモナス症。 FLAGYL 400mg は、女性の無症候性 T. vaginalis 感染症の治療に適応され、生物が子宮頸管内炎、子宮頸管炎、または子宮頸部びらんに関連している場合に適応となります。トリコモナスの存在が異常な細胞学的塗抹標本の正確な評価を妨げる可能性があるという証拠があるため、寄生虫の根絶後に追加の塗抹標本を実施する必要があります。
無症候性の性的パートナーの治療。 T. vaginalis 感染症は性病です。したがって、パートナーの再感染を防ぐために、治療を受けた患者の無症候性の性的パートナーは、微生物が存在することが判明した場合は同時に治療する必要があります.否定的な文化を持っている無症候性の男性パートナーを治療するか、文化を試みていない男性パートナーを治療するかについての決定は、個々のものです.この決定を下す際には、性的パートナーが治療されない場合、女性が再感染する可能性があるという証拠があることに注意する必要があります.また、無症候性の男性保因者から微生物を分離することはかなり困難である可能性があるため、この点に関して塗抹標本や培養が陰性であることに依存することはできません。いずれにせよ、性的パートナーは、再感染の場合には FLAGYL で治療する必要があります。
アメーバ症。 FLAGYL は、急性腸アメーバ症(アメーバ赤痢)およびアメーバ性肝膿瘍の治療に適応されます。
アメーバ性肝膿瘍では、FLAGYL 療法によって膿の吸引や排出が不要になるわけではありません。
嫌気性細菌感染症。 FLAGYL 200mg は、感受性嫌気性細菌によって引き起こされる重篤な感染症の治療に適応されます。指示された外科的処置は、FLAGYL 療法と組み合わせて実施する必要があります。好気性と嫌気性の混合感染症では、FLAGYL に加えて、好気性感染症の治療に適した抗菌薬を使用する必要があります。
B. fragilis グループ (B. fragilis、B. distasonis、B. ovatus、B. thetaiotaomicron、B. vulgatus)、Clostridium を含む Bacteroides 種によって引き起こされる、腹膜炎、腹腔内膿瘍、および肝膿瘍を含む腹腔内感染症種、ユーバクテリウム種、ペプトコッカス種、およびペプトストレプトコッカス種。
B. fragilis グループ、Clostridium 種、Peptococcus 種、Peptostreptococcus 種、および Fusobacterium 種を含む Bacteroides 種によって引き起こされる皮膚および皮膚構造感染症。
B. fragilis グループを含む Bacteroides 種、Clostridium 種、Peptococcus 種、Peptostreptococcus 種、および Fusobacterium 種によって引き起こされる、子宮内膜炎、子宮内膜炎、卵管卵巣膿瘍、および術後の膣カフ感染を含む婦人科感染症。
B. fragilis グループおよび Clostridium 種を含む Bacteroides 種によって引き起こされる細菌性敗血症。
B. fragilis グループを含む Bacteroides 種によって引き起こされる骨および関節の感染症 (補助療法として)。
B. fragilis グループを含む Bacteroides 種によって引き起こされる、髄膜炎および脳膿瘍を含む中枢神経系 (CNS) 感染症。
B. fragilis グループを含む Bacteroides 種によって引き起こされる、肺炎、蓄膿症、および肺膿瘍を含む下気道感染症。
B. fragilis グループを含む Bacteroides 種によって引き起こされる心内膜炎。
薬剤耐性菌の発生を減らし、フラジール 400mg および他の抗菌薬の有効性を維持するために、フラジールは、感受性菌によることが証明されているか、または強く疑われる感染症の治療または予防にのみ使用する必要があります。培養および感受性の情報が利用可能である場合、それらは抗菌療法の選択または変更において考慮されるべきです。そのようなデータがない場合、地域の疫学および感受性パターンが治療の経験的選択に寄与する可能性があります。
投薬と管理
トリコモナス症
女性で
日治療 - 2 グラムの FLAGYL を 1 回または 1 グラムずつ 2 回に分けて、同じ日に投与します。
日間の治療コース - 250 mg を 1 日 3 回、連続 7 日間。対照比較研究から、膣スメアおよび徴候と症状によって決定される治癒率は、1 日治療レジメンよりも 7 日間治療コースの方が高い可能性があるといういくつかの兆候があります。
投与計画は個別化する必要があります。単回投与治療は、7 日間のレジメンを継続することに頼ることができない患者において、特に監督下で投与された場合、コンプライアンスを保証することができます。 7日間の治療コースは、性的接触が適切な治療を受けるのに十分な期間患者を保護することにより、再感染を最小限に抑えることができます.さらに、一部の患者は、一方の治療レジメンが他方よりも良好に許容される場合があります。
妊娠中の患者は、妊娠初期に治療を受けるべきではありません( 禁忌 )。代替治療が不十分な妊娠中の患者では、胎児循環に到達する可能性のある血清レベルが高くなるため、1日コースの治療は使用しないでください。 予防 、 妊娠 )。
薬の繰り返しコースが必要な場合は、コース間に 4 ~ 6 週間の間隔を置き、適切な検査手段によってトリコモナスの存在を再確認することをお勧めします。再治療の前後に白血球の総計数と分画数を測定する必要があります。
男性の場合:女性の場合と同様に、治療は個別化する必要があります。
アメーバ症
大人
急性腸アメーバ症 (急性アメーバ赤痢) の場合: 750 mg を 1 日 3 回、5 ~ 10 日間経口投与します。
アメーバ性肝膿瘍の場合:500 mg または 750 mg を 1 日 3 回、5 ~ 10 日間経口投与します。
小児患者: 35 ~ 50 mg/kg/24 時間、3 回に分けて 10 日間経口投与。
嫌気性細菌感染症
最も深刻な嫌気性感染症の治療では、通常、静脈内メトロニダゾールが最初に投与されます。
通常、成人には1回7.5mg/kgを6時間おきに経口投与します(体重70kgの成人で約500mg)。 24 時間で最大 4 g を超えてはなりません。
通常の治療期間は 7 ~ 10 日です。ただし、骨や関節、下気道、心内膜の感染症には、より長い治療が必要になる場合があります。
投与量の調整
重度の肝障害のある患者
重度の肝障害のある患者 (Child-Pugh C) の場合、FLAGYL の用量を 50% 減らす必要があります (以下を参照)。 臨床薬理学 と 予防 )。
血液透析を受けている患者
血液透析は、全身循環からかなりの量のメトロニダゾールとその代謝物を除去します。メトロニダゾールのクリアランスは、使用する透析膜の種類、透析期間、およびその他の要因によって異なります。メトロニダゾールの投与を血液透析セッションから切り離すことができない場合、患者の臨床状況に応じて、血液透析セッション後にメトロニダゾールの投与量を追加することを検討する必要があります。 臨床薬理学 )。
供給方法
フラジール 250mg 錠剤は円形、青色、フィルムコーティングされており、片面に SEARLE と 1831 の型押し、反対面に FLAGYL と 250 の型押しが施されています。 50本入りと100本入りのボトルでお届けします。
フラジール 500mg 錠剤は長方形、青色、フィルムコーティングされており、片面にFLAGYLが型押しされ、もう片面には500が型押しされています。 50と100のボトル。
ストレージと安定性
25°C (77°F) 以下で保管し、遮光してください。
配布元: Pfizer Labs, Division of Pfizre Inc., NY, NY 10017. 改訂: 2021 年 12 月
副作用
メトロニダゾールによる治療中に、以下の反応が報告されています。
中枢神経系
メトロニダゾールで治療された患者で報告された最も深刻な副作用は、けいれん発作、脳症、無菌性髄膜炎、視神経および末梢神経障害であり、後者は主に四肢のしびれまたは感覚異常を特徴としています。メトロニダゾールの長期投与を受けている一部の患者で永続的な末梢神経障害が報告されているため、患者はこれらの反応について特に警告する必要があり、神経学的症状が発生した場合は薬を中止し、すぐに医師に報告するように指示する必要があります.さらに、患者は、頭痛、失神、めまい、めまい、協調運動失調、運動失調、錯乱、構音障害、過敏症、うつ病、脱力感、および不眠症を報告しています( 警告 )。
胃腸
報告された最も一般的な有害反応は、胃腸管に関連するもので、特に吐き気で、時には頭痛、食欲不振、時には嘔吐を伴います。下痢;みぞおちの苦痛;腹部のけいれんと便秘。
口
辛く不快な金属味は珍しくありません。毛むくじゃらの舌、舌炎、口内炎が発生しました。これらは、治療中に発生する可能性のあるカンジダの突然の過増殖に関連している可能性があります.
皮膚科
紅斑性発疹およびかゆみ。
造血
可逆性好中球減少症 (白血球減少症);まれに、可逆性血小板減少症。
心臓血管
特にメトロニダゾールがQT間隔を延長する可能性のある薬物と一緒に投与された場合、QT延長が報告されています。 T 波の平坦化は、心電図トレースで見られる場合があります。
過敏症
蕁麻疹、紅斑性発疹、スティーブンス・ジョンソン症候群、中毒性表皮壊死融解症、潮紅、鼻づまり、口(または膣または外陰部)の乾燥、および発熱。
腎臓
排尿困難、膀胱炎、多尿、失禁、骨盤圧迫感。黒ずんだ尿の例は、約 100,000 人に 1 人の患者によって報告されています。この現象の原因と思われる色素は特定されていませんが、ほぼ確実にメトロニダゾールの代謝産物であり、臨床的意義はないようです.
肝臓
コケイン症候群の患者では、メトロニダゾールの全身使用の開始後に非常に急速に発症し、致命的な転帰を伴う症例を含む、重度の不可逆的な肝毒性/急性肝不全の症例が報告されています(投薬開始から肝不全の徴候までの潜伏期間はわずか2日です) (見る 禁忌 )。
他の
膣内のカンジダの増殖、性交疼痛、性欲減退、直腸炎、時には「血清病」に似た一時的な関節痛。膵炎のまれなケースが報告されていますが、これは通常、薬物の中止で和らぎました。
クローン病の患者は、消化管および特定の腸管外のがんの発生率が高いことが知られています。高用量のメトロニダゾールで長期間治療されたクローン病患者の乳癌および結腸癌の医学文献には、いくつかの報告があります。因果関係は確立されていません。クローン病は、FLAGYL 200mg 錠の適応症として承認されていません。
薬物相互作用
ジスルフィラム
精神病反応は、メトロニダゾールとジスルフィラムを同時に使用しているアルコール依存症患者で報告されています.メトロニダゾールは、過去 2 週間以内にジスルフィラムを服用した患者には投与しないでください ( 禁忌 )。
アルコール飲料
メトロニダゾール治療中または治療後にアルコール飲料またはプロピレングリコールを含む製品を摂取すると、腹部のけいれん、吐き気、嘔吐、頭痛、潮紅が起こることがあります。 禁忌 )。
ワルファリンおよびその他の経口抗凝固薬
メトロニダゾールは、ワルファリンやその他の経口クマリン抗凝固剤の抗凝固効果を増強し、プロトロンビン時間を延長させることが報告されています。このタイプの抗凝固療法を受けている患者に FLAGYL を処方する場合は、プロトロンビン時間と INR を注意深く監視する必要があります。

リチウム
比較的高用量のリチウムで安定した患者では、短期間のメトロニダゾール療法は血清リチウムの上昇と、少数のケースではリチウム毒性の徴候と関連しています。血清リチウムおよび血清クレアチニンレベルは、リチウム中毒の臨床症状に先行する可能性のある上昇を検出するために、メトロニダゾールを開始してから数日後に取得する必要があります.
ブスルファン
メトロニダゾールは、ブスルファンの血漿濃度を上昇させることが報告されており、その結果、深刻なブスルファン毒性のリスクが高まる可能性があります。ベネフィットがリスクを上回らない限り、メトロニダゾールをブスルファンと同時に投与すべきではありません。メトロニダゾールに代わる治療法がなく、ブスルファンとの併用投与が医学的に必要な場合は、ブスルファンの血漿濃度を頻繁にモニタリングし、それに応じてブスルファンの用量を調整する必要があります。
CYP450酵素を阻害する薬剤
シメチジンなどのミクロソーム肝酵素活性を低下させる薬物の同時投与は、半減期を延長し、メトロニダゾールの血漿クリアランスを低下させる可能性があります。
CYP450酵素を誘導する薬剤
フェニトインやフェノバルビタールなどのミクロソーム肝酵素を誘導する薬物の同時投与は、メトロニダゾールの排出を促進し、血漿レベルの低下をもたらす可能性があります。フェニトインのクリアランス障害も報告されています。
QT間隔を延長する薬
特にメトロニダゾールがQT間隔を延長する可能性のある薬物と一緒に投与された場合、QT延長が報告されています。
警告
中枢および末梢神経系への影響
脳症および末梢神経障害:脳障害および末梢神経障害(視神経障害を含む)の症例がメトロニダゾールで報告されています。
脳症は、運動失調、めまい、および構音障害を特徴とする小脳毒性に関連して報告されています。 MRI で見られる CNS 病変は、脳症の報告に記載されています。中枢神経系の症状は、メトロニダゾールを中止すると、通常、数日から数週間で元に戻ります。 MRI で見られる CNS 病変も可逆的であると説明されています。
主に感覚型の末梢神経障害が報告されており、四肢のしびれまたは感覚異常を特徴としています。
メトロニダゾールで治療された患者では、けいれん発作が報告されています。
無菌性髄膜炎:無菌性髄膜炎の症例がメトロニダゾールで報告されています。症状は投与後数時間以内に発生する可能性があり、一般的にメトロニダゾール療法を中止すると解消します。
異常な神経学的徴候および症状の出現は、治療継続の利益/リスク比の迅速な評価を必要とします (以下を参照)。 有害反応 )。
予防
全般的
肝障害
肝機能障害のある患者は、メトロニダゾールの代謝が遅く、その結果、血漿中にメトロニダゾールが蓄積します。重度の肝機能障害(Child-Pugh C)の患者には、FLAGYL 400mg の減量が推奨されます。軽度から中等度の肝障害のある患者の場合、用量調整は必要ありませんが、これらの患者はメトロニダゾール関連の有害事象について監視する必要があります( 臨床薬理学 と 投薬と管理 )。
腎障害
末期腎不全の患者は、メトロニダゾールと代謝物をゆっくりと尿中に排泄し、メトロニダゾール代謝物が著しく蓄積する可能性があります。メトロニダゾール関連の有害事象のモニタリングが推奨されます( 臨床薬理学 )。
真菌重複感染
既知または以前に認識されていないカンジダ症は、FLAGYL による治療中により顕著な症状を示す可能性があり、カンジダ駆除剤による治療が必要です。
血液疾患のある患者への使用
メトロニダゾールはニトロイミダゾールの一種であり、血液疾患の証拠または病歴のある患者には注意して使用する必要があります。投与中に軽度の白血球減少が観察されました。ただし、メトロニダゾールに起因する持続的な血液学的異常は、臨床研究では観察されていません。治療の前後に白血球の総計数と分画数を測定することをお勧めします。
薬剤耐性菌と寄生虫
細菌感染または寄生虫感染が証明されている、または強く疑われる場合、または予防的適応がない場合に FLAGYL を処方すると、患者に利益がもたらされる可能性は低く、薬剤耐性菌および寄生虫が発生するリスクが高まります。
薬物/実験室試験の相互作用
メトロニダゾールは、アスパラギン酸アミノトランスフェラーゼ (AST、SGOT)、アラニンアミノトランスフェラーゼ (ALT、SGPT)、乳酸脱水素酵素 (LDH)、トリグリセリド、およびグルコースヘキソキナーゼなど、特定の種類の血清化学値の決定を妨げる可能性があります。ゼロの値が観察される場合があります。干渉が報告されているすべてのアッセイには、ニコチンアミドアデニンジヌクレオチド (NAD+ NADH) の酸化還元へのアッセイの酵素的カップリングが含まれます。干渉は、pH 7 での NADH (340 nm) とメトロニダゾール (322 nm) の吸光度ピークの類似性によるものです。
非臨床毒性学
発がん、突然変異誘発、生殖能力の障害
肝臓、肺、乳腺、およびリンパ組織に影響を与える腫瘍は、ラットおよびマウスにおけるメトロニダゾールのいくつかの研究で検出されましたが、ハムスターでは検出されませんでした.
肺腫瘍は、マウスで報告された 6 つの研究すべてで観察されており、その中には動物に断続的なスケジュールで投与された 1 つの研究 (4 週ごとにのみ投与) が含まれていました。悪性肝腫瘍は、約 1500 mg/m² で処理された雄マウスで増加しました (体表面積の比較に基づく、1 日最大推奨用量と同様)。悪性リンパ腫と肺新生物も、マウスへの薬物の生涯給餌で増加しました。経口メトロニダゾールを投与された雌ラットでは、同時対照群と比較して、乳腺および肝臓の腫瘍が増加した。ハムスターで 2 つの生涯腫瘍原性試験が実施され、陰性であると報告されています。
メトロニダゾールは、エイムズ試験を含む in vitro アッセイ系で変異原性を示しています。哺乳動物の in vivo 研究では、遺伝的損傷の可能性を示すことができませんでした。
メトロニダゾールは、28 日間、400 mg/kg/日 (体表面積の比較に基づく最大推奨臨床用量と同様) の用量で雄ラットの受胎能または精巣機能に悪影響を与えることはありませんでした。しかし、同じ用量で 6 週間以上投与されたラットは不妊であり、精巣の精細上皮の重度の変性と、精巣精子細胞数および精巣上体精子数の顕著な減少を示しました。 8 週間の薬物を使用しない回復期間の後、ほとんどのラットで生殖能力が回復しました。
妊娠
催奇形性効果
妊娠中の女性を対象とした FLAGYL の十分に管理された研究はありません。ケースコントロール研究、コホート研究、および妊娠中にメトロニダゾールを使用した 5000 人以上の妊婦を含む 2 つのメタ分析からのデータが公開されています。多くの研究には、妊娠初期の曝露が含まれていました。ある研究では、子宮内でメトロニダゾールに曝露された乳児において、口蓋裂の有無にかかわらず、口唇裂のリスクが増加することが示されました。ただし、これらの調査結果は確認されませんでした。さらに、早産の発生率に対する細菌性膣炎に対する抗生物質治療(メトロニダゾールを含む)の使用を評価するために、5000 人以上の妊婦を登録した 10 以上のランダム化プラセボ対照臨床試験が実施されました。ほとんどの研究では、妊娠中のメトロニダゾール曝露後の先天性異常またはその他の有害な胎児転帰のリスク増加は示されませんでした。妊娠中のメトロニダゾール曝露後の乳児がんのリスクを評価するために実施された 3 つの研究では、リスクの増加は示されませんでした。ただし、このような信号を検出するこれらの研究の能力は限られていました。
メトロニダゾールは胎盤関門を通過し、ヒト胎児器官形成への影響は知られていません。体表面積の比較に基づくヒトの最大推奨用量と同様の用量で、ラット、ウサギ、およびマウスで生殖研究が実施されています。メトロニダゾールによる胎児への害の証拠はありませんでした。
授乳中の母親
メトロニダゾールは、母親の血清レベルと同様の濃度で母乳中に存在し、乳児の血清レベルは、乳児の治療レベルに近いか、同等である可能性があります。マウスおよびラットでメトロニダゾールに示された腫瘍原性の可能性のため
研究に基づいて、母親にとっての薬物の重要性を考慮して、看護を中止するか薬物を中止するかを決定する必要があります。別の方法として、授乳中の母親は、メトロニダゾール治療中は母乳を搾乳して廃棄し、治療終了後 24 時間は乳児に保存した母乳または粉ミルクを与えることを選択する場合があります。
高齢者の使用
高齢の高齢患者では、メトロニダゾール関連の有害事象のモニタリングが推奨されます( 臨床薬理学 、 予防 )。高齢患者の肝機能の低下により、メトロニダゾールの濃度が上昇する可能性があり、メトロニダゾールの投与量の調整が必要になる場合があります。 投薬と管理 )。
小児用
アメーバ症の治療を除いて、小児患者における安全性と有効性は確立されていません。
過剰摂取
15gまでのメトロニダゾールの単回経口投与は、自殺未遂や偶発的な過剰摂取で報告されています.報告されている症状には、吐き気、嘔吐、および運動失調が含まれます。
経口メトロニダゾールは、悪性腫瘍の治療における放射線増感剤として研究されています。発作および末梢神経障害を含む神経毒性作用は、6~10.4gの用量を隔日で5~7日間服用した後に報告されています。
過剰摂取の治療
メトロニダゾールの過剰摂取に対する特定の解毒剤はありません。したがって、患者の管理は、対症療法と支持療法で構成する必要があります。
禁忌
過敏症
FLAGYL 錠は、メトロニダゾールまたは他のニトロイミダゾール誘導体に対する過敏症の既往歴のある患者には禁忌です。
トリコモナス症の患者では、フラジール 200mg 錠は妊娠の最初の三半期には禁忌です( 予防 )。
ジスルフィラムによる精神病反応
経口メトロニダゾールの使用は、ジスルフィラムを同時に使用していたアルコール依存症患者の精神病反応と関連しています。過去 2 週間以内にジスルフィラムを服用した患者には、メトロニダゾールを投与しないでください。 予防 、 薬物相互作用 )。
アルコールとの相互作用
経口メトロニダゾールの使用は、腹部痙攣、吐き気、嘔吐、頭痛、紅潮など、アルコールに対するジスルフィラム様反応と関連しています。メトロニダゾールによる治療中および治療後少なくとも 3 日間は、アルコールまたはプロピレングリコールを含む製品の摂取を中止してください (以下を参照)。 予防 、 薬物相互作用 )。
コケイン症候群
FLAGYL 400mg 錠は、コケイン症候群の患者には禁忌です。コケイン症候群の患者でメトロニダゾールの開始後に、致命的な転帰を伴う重度の不可逆的な肝毒性/急性肝不全が報告されています。 有害反応 )。
臨床薬理学
吸収
体内でのメトロニダゾールの配置は、経口剤形と静脈内剤形の両方で類似しています。経口投与後、メトロニダゾールはよく吸収され、投与後 1 ~ 2 時間でピーク血漿濃度が発生します。
メトロニダゾールの血漿中濃度は投与量に比例します。 250 mg、500 mg、または 2,000 mg の経口投与により、それぞれ 6 mcg/mL、12 mcg/mL、および 40 mcg/mL のピーク血漿濃度が得られました。研究によると、男性と女性の間でバイオアベイラビリティーに大きな違いはありません。ただし、体重の違いにより、男性の血漿中濃度は一般的に低くなります。
分布
メトロニダゾールは血漿中に出現する主要成分であり、少量の代謝物も存在します。循環するメトロニダゾールの 20% 未満が血漿タンパク質に結合しています。メトロニダゾールは、脳脊髄液、唾液、および母乳中に、血漿中と同様の濃度で存在します。メトロニダゾールの殺菌濃度は、肝膿瘍からの膿でも検出されています。
代謝・排泄
メトロニダゾールとその代謝物の主な排泄経路は尿 (投与量の 60% ~ 80%) であり、糞便排泄は投与量の 6% ~ 15% を占めます。尿中に現れる代謝物は、主に側鎖の酸化 [1-(βヒドロキシエチル)- 2-ヒドロキシメチル-5-ニトロイミダゾールおよび 2-メチル-5-ニトロイミダゾール-1-イル酢酸] とグルクロニド抱合から生じ、メトロニダゾールは変化しません。全体の約20%。親化合物とヒドロキシル代謝物の両方が in vitro 抗菌活性を持っています。
メトロニダゾールの腎クリアランスは、約 10 mL/分/1.73 m² です。健康な被験者におけるメトロニダゾールの平均排出半減期は 8 時間です。
腎障害
腎機能の低下は、メトロニダゾールの単回投与の薬物動態を変化させません。
末期腎疾患 (ESRD; CLCR= 8.1±9.1 mL/分) を持ち、メトロニダゾール 500 mg の単回静脈内注入を受けた被験者では、メトロニダゾールの薬物動態に有意な変化はありませんでしたが、ヒドロキシメトロニダゾールの Cmax は 2 倍高く、5腎機能が正常な健康な被験者と比較して、酢酸メトロニダゾールの Cmax が倍高い (CLCR= 126±16 mL/min)。したがって、ESRD 患者ではメトロニダゾール代謝産物が蓄積する可能性があるため、メトロニダゾール関連の有害事象をモニタリングすることが推奨されます (以下を参照)。 予防 )。
透析の効果
メトロニダゾール 500 mg の単回静脈内注入または経口投与後、メトロニダゾールのクリアランスは、血液透析または連続外来腹膜透析 (CAPD) を受けている ESRD 被験者で調査されました。使用する透析膜の種類と透析期間に応じて、4 ~ 8 時間続く血液透析セッションでは、投与されたメトロニダゾール用量の 40% ~ 65% が除去されました。メトロニダゾールの投与を透析セッションから切り離すことができない場合は、血液透析後のメトロニダゾール用量の補充を検討する必要があります。 投薬と管理 )。 7.5 時間続く腹膜透析セッションでは、投与されたメトロニダゾール用量の約 10% が除去されました。 CAPDを受けているESRD患者では、メトロニダゾールの用量を調整する必要はありません。
肝障害
メトロニダゾール 500 mg の単回静脈内注入後、メトロニダゾールの平均 AUC24 は、重度 (Child-Pugh C) 肝障害患者で 114%、軽度 (Child-Pugh A) 患者で 54% および 53% 高くなった。健康な対照被験者と比較して、それぞれ中等度(Child-Pugh B)の肝障害。これらの肝障害患者では、ヒドロキシメトロニダゾールの AUC24 に有意な変化はありませんでした。重度の(Child-Pugh C)肝障害のある患者には、メトロニダゾールの投与量を 50% 減らすことが推奨されます。 投薬と管理 )。軽度から中等度の肝障害のある患者には、用量調整は必要ありません。軽度から中等度の肝障害のある患者は、メトロニダゾール関連の有害事象について監視する必要があります( 予防 と 投薬と管理 )。
高齢患者
メトロニダゾール 500 mg の単回経口または IV 投与後、明らかな腎機能障害または肝機能障害のない 70 歳以上の被験者は、ヒドロキシメトロニダゾール (活性代謝物) の平均 AUC が 40% から 80% 高く、平均値の明らかな増加はありませんでした。メトロニダゾール (親化合物) の AUC (40 歳未満の若い健康な対照と比較)。高齢患者では、メトロニダゾール関連の有害事象のモニタリングが推奨されます( 予防 )。
小児患者
ある研究では、新生児はメトロニダゾールを排泄する能力が低下しているように見えました.人生の最初の 3 日間に測定された排泄半減期は、妊娠期間と反比例の関係にありました。妊娠期間が 28 ~ 40 週の乳児では、対応する排泄半減期は 109 ~ 22.5 時間の範囲でした。
微生物学
作用機序
ニトロイミダゾールであるメトロニダゾールは、ほとんどの偏性嫌気性菌に対して嫌気性環境で抗菌効果を発揮します。メトロニダゾールが受動拡散によって生体内に入り、感受性嫌気性細菌の細胞質で活性化されると、メトロニダゾールは減少します。このプロセスには、フェレドキシンなどの細胞内電子伝達タンパク質、メトロニダゾールのニトロ基への電子の移動、および短命のニトロソ フリーラジカルの形成が含まれます。このメトロニダゾール分子の変化により、濃度勾配が作られ維持され、薬物の細胞内輸送が促進されます。還元型のメトロニダゾールとフリーラジカルは DNA と相互作用し、DNA 合成を阻害し、DNA 分解を引き起こし、細菌を死滅させます。メトロニダゾールの正確な作用機序は不明です。
抵抗
メトロニダゾールに対する耐性が発生する可能性があります。
耐性は、薬物の取り込みの減少、還元効率の変化、排出ポンプの過剰発現、薬物の不活性化、および/または DNA 損傷修復の増加など、複数のメカニズムによる可能性があります。
メトロニダゾールは、通性嫌気性菌または偏性好気性菌に対して臨床的に関連する活性を持ちません。
抗菌活性
メトロニダゾールは、適応症と使用法セクションで説明されているように、in vitro および臨床感染症の両方で、以下の細菌のほとんどの分離株に対して活性があることが示されています。
グラム陽性嫌気性菌
クロストリジウム種 ユーバクテリア種 ペプトコッカス種 ペプトストレプトコッカス種
グラム陰性菌
Bacteroides fragilis グループ (B. fragilis、B. distasonis、B. ovatus、B. thetaiotaomicron、B.vulgatus) Fusobacterium 種
原虫寄生虫
Entamoeba histolytica Trichomonas vaginalis
以下の in vitro データが利用可能ですが、それらの臨床的意義は不明です。
メトロニダゾールは、次の細菌のほとんどの分離株 (90% 以上) に対して 8 mcg/mL 以下の in vitro 最小発育阻止濃度 (MIC’s) を示します。しかし、これらの細菌による臨床感染症の治療におけるメトロニダゾールの安全性と有効性は、十分に管理された臨床試験では確立されていません。
グラム陰性嫌気性菌
Bacteroides fragilis グループ (B. caccae、B. uniformis) Prevotella 種 (P. bivia、P. buccae、P. disiens)
感受性試験
感受性試験の解釈基準、関連する試験方法、およびこの薬剤について FDA によって認められた品質管理基準に関する具体的な情報については、https://www.fda.gov/STIC を参照してください。
患者情報
アルコールとの相互作用
腹部痙攣、吐き気、嘔吐、頭痛、紅潮が起こる可能性があるため、FLAGYL 400mg の服用中およびその後少なくとも 3 日間は、アルコール飲料またはプロピレングリコールを含む製品の摂取を中止してください ( 禁忌 と 予防 、 薬物相互作用 )。
細菌感染症および寄生虫感染症の治療
FLAGYL 400mg は細菌感染症および寄生虫感染症の治療にのみ使用するよう患者に説明する必要があります。 FLAGYL 400mg は、ウイルス感染症 (風邪など) を治療しません。 FLAGYL が細菌感染症の治療のために処方された場合、患者は治療の初期に気分が良くなることがよくありますが、指示どおりに服用する必要があることを患者に伝えてください。投与をスキップしたり、治療の全コースを完了しなかったりすると、(1) 当面の治療の有効性が低下し、(2) 細菌が耐性を獲得し、将来的に FLAGYL 400mg で治療できなくなる可能性が高くなる可能性があります。
