Duricef 250mg, 500mg Cefadroxil 使用法、副作用および投与量。 オンライン薬局の価格。 処方箋不要のジェネリック医薬品。
Duricef とは何ですか? また、どのように使用されますか?
デュリセフ(セファドロキシル)は、細菌によって引き起こされるさまざまな種類の感染症の治療に使用されるセファロスポリン系抗生物質です。ブランド名のデュリセフは廃止され、セファドロキシルはジェネリックの形で入手できます。
デュリセフの副作用は何ですか?
デュリセフ(セファドロキシル)の一般的な副作用は次のとおりです。
- 胃のむかつきや痛み、
- 吐き気、
- 嘔吐、
- 下痢、
- 凝り固まった筋肉、
- 関節痛、
- 落ち着きのなさや多動を感じ、
- あなたの口の中で異常または不快な味、
- かゆみや皮膚発疹、または
- 膣のかゆみまたは分泌物。
次のようなデュリセフ(セファドロキシル)の非常に深刻な副作用がある可能性は低い場合は、医師に相談してください。
- 持続的な吐き気や嘔吐、
- 目や肌の黄ばみ、
- 暗い尿、
- 感染の新たな徴候(例えば、持続性の喉の痛みまたは発熱)、
- あざや出血しやすい、
- 尿量の変化、または
- 精神/気分の変化 (混乱など)。
説明
DURICEF (セファドロキシル) は、経口投与を目的とした半合成セファロスポリン系抗生物質です。白色から黄白色の結晶性粉末です。水に溶け、酸に安定です。 5-チア-1-アザビシクロ[4.2.0]オクタ-2-エン-2-カルボン酸、7-[[アミノ(4-ヒドロキシフェニル)アセチル]アミノ]-3-メチル-8-オキソとして化学的に指定されています。 -、一水和物[6R-[6α,7β(R*)]]-。化学式は C16H17N3O5S•H20 で、分子量は 381.40 です。次の構造式があります。
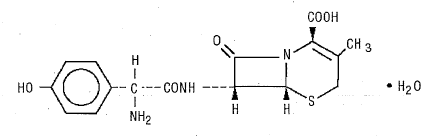
DURICEF (セファドロキシル) フィルムコーティング錠 1 g には、次の不活性成分が含まれています: 微結晶性セルロース、ヒドロキシプロピルメチルセルロース、ステアリン酸マグネシウム、ポリエチレングリコール、ポリソルベート 80、シメチコンエマルジョン、および二酸化チタン。
DURICEF (cefadroxil) for Oral Suspension には、次の不活性成分が含まれています: FD&C 黄色 6 号、香料 (天然および人工)、ポリソルベート 80、安息香酸ナトリウム、スクロース、およびキサンタンガム。
DURICEF (セファドロキシル) カプセルには、次の不活性成分が含まれています: D&C 赤色 28 号、FD&C 青色 1 号、FD&C 赤色 40 号、ゼラチン、ステアリン酸マグネシウム、および二酸化チタン。
適応症
デュリセフ(セファドロキシル)は、以下の疾患の指定微生物の感受性株による感染症患者の治療に適応されます。
大腸菌による尿路感染症; P. mirabilis、および Klebsiella 種。
ブドウ球菌および/または連鎖球菌によって引き起こされる皮膚および皮膚構造の感染症。
Streptococcus pyogenes (グループ A ベータ溶血性連鎖球菌) によって引き起こされる咽頭炎および/または扁桃炎。
ノート: 筋肉内投与経路によるペニシリンのみが、リウマチ熱の予防に有効であることが示されています。デュリセフ(セファドロキシル)は、一般的に中咽頭からのレンサ球菌の根絶に効果的です。ただし、その後のリウマチ熱の予防に対するDUICEF(セファドロキシル)の有効性を確立するデータは入手できません。
ノート: 培養および感受性試験は、治療前および治療中に開始する必要があります。必要に応じて腎機能検査を実施する必要があります。
薬剤耐性菌の発生を減らし、デュリセフ(セファドロキシル)やその他の抗菌薬の有効性を維持するために、デュリセフ(セファドロキシル)は、感受性のある細菌が原因であることが証明されているか、強く疑われる感染症の治療または予防にのみ使用する必要があります。培養および感受性の情報が利用可能である場合、それらは抗菌療法の選択または変更において考慮されるべきです。そのようなデータがない場合、地域の疫学および感受性パターンが治療の経験的選択に寄与する可能性があります。
投薬と管理
デュリセフ(セファドロキシル)は酸安定性があり、食事に関係なく経口投与できます。食物と一緒に投与することは、経口セファロスポリン療法に時折関連する潜在的な胃腸の不調を軽減するのに役立つかもしれません.
大人
尿路感染症: 合併症のない下部尿路感染症(すなわち、膀胱炎)の場合、通常の投与量は、1 日あたり 1 または 2 g を 1 回(qd)または分割して(bid)投与します。
他のすべての尿路感染症の場合、通常の投与量は 1 日 2 g を分割投与 (bid) します。
皮膚および皮膚構造の感染症: 皮膚および皮膚構造の感染症の場合、通常の投与量は 1 日 1 g で、単回投与 (qd) または分割投与 (bid) で行われます。
咽頭炎および扁桃炎: グループ A ベータ溶血性連鎖球菌咽頭炎および扁桃炎の治療 - 1 日あたり 1 g を 1 回 (qd) または分割用量 (bid) で 10 日間。
子供
尿路感染症の場合、小児の推奨される 1 日量は 30 mg/kg/日で、12 時間ごとに分割されます。咽頭炎、扁桃炎、膿痂疹の場合、小児の推奨される 1 日用量は 30 mg/kg/日で、1 回または 12 時間ごとに等分割されます。その他の皮膚および皮膚構造の感染症の場合、推奨される 1 日量は 30 mg/kg/日で、12 時間ごとに均等に分割されます。ベータ溶血性レンサ球菌感染症の治療では、DURICEF (セファドロキシル) の治療用量を少なくとも 10 日間投与する必要があります。
小児の 1 日総投与量については、チャートを参照してください。
腎障害
腎障害のある患者では、セファドロキシル一水和物の投与量は、薬物の蓄積を防ぐためにクレアチニンクリアランス速度に従って調整する必要があります.次のスケジュールが推奨されます。成人の場合、初期用量はDUICEF(セファドロキシル)1000mgであり、維持用量(クレアチニンクリアランス速度[mL/分/1.73M2]に基づく)は500mgで、以下に示す時間間隔で投与されます。
クレアチニンクリアランス率が 50 mL/min を超える患者は、正常な腎機能を有する患者であるかのように治療することができます。
供給方法
DURICEF® (セファドロキシル一水和物、USP) 500 mg カプセル: 不透明、あずき色、白色のハード ゼラチン カプセルで、一方の端に「PPP」と「784」、もう一方の端に「DUICEF (セファドロキシル)」と「500 mg」と刻印されています。 .
カプセルは次のように提供されます。
N 0430-0780-19..................50本入
15° - 30° C (59° - 86° F) に制御された室温で保管してください。
DURICEF® (セファドロキシル) 1 グラム 錠剤: 白色からオフホワイト、上部が 2 等分、楕円形、2 分の 1 面に「PPP」、もう 1 面に「785」と刻印されています。タブレットは次のように提供されます。
N 0430-0781-19..................50本入
15° - 30° C (59° - 86° F) に制御された室温で保管してください。
DURICEF® (cefadroxil) for Oral Suspension はオレンジパイナップル風味で、次のように供給されます。
250mg/5mL.................................N 0430-2782-15 50mLボトル
再構成前: 15° - 30° C (59° - 86° F) に制御された室温で保管してください。
Bristol-Myers Squibb Co. Princeton, NJ 08543 が製造。Warner Chilcott Company, Inc. Fajardo, PR 00738 向け。Warner Chilcott (US), Inc. Rockaway, NJ 07866 が販売。2007 年 4 月改訂。 2007 年 5 月
副作用
胃腸
抗生物質治療中または治療後に、偽膜性大腸炎の症状が現れることがあります( 警告 )。消化不良、吐き気、嘔吐がまれに報告されています。下痢も発生。
過敏症
アレルギー(発疹、蕁麻疹、血管性浮腫、かゆみなど)が観察されています。これらの反応は通常、薬を中止すると治まります。アナフィラキシーも報告されています。
他の
他の反応には、胆汁うっ滞および血清トランスアミナーゼの上昇、性器掻痒症、性器モニリア症、膣炎、中等度の一過性好中球減少症、発熱などの肝機能障害が含まれます。無顆粒球症、血小板減少症、特異体質性肝不全、多形紅斑、スティーブンス・ジョンソン症候群、血清病、および関節痛はめったに報告されていません。
セファドロキシルで治療された患者で観察された上記の有害反応に加えて、セファロスポリンクラスの抗生物質について、次の有害反応および臨床検査の変更が報告されています。
中毒性表皮壊死融解症、腹痛、重複感染、腎機能障害、中毒性腎症、再生不良性貧血、溶血性貧血、出血、プロトロンビン時間延長、クームス試験陽性、BUN上昇、クレアチニン上昇、アルカリホスファターゼ上昇、アスパラギン酸アミノトランスフェラーゼ(AST)上昇、上昇アラニンアミノトランスフェラーゼ(ALT)、ビリルビンの上昇、LDHの上昇、好酸球増加症、汎血球減少症、好中球減少症。
いくつかのセファロスポリンは、用量を減らさなかった場合に、特に腎機能障害のある患者で発作を誘発することに関与している( 用法・用量および過剰摂取 )。薬物療法に関連する発作が発生した場合は、薬物を中止する必要があります。臨床的に必要な場合は、抗けいれん療法を行うことができます。
薬物相互作用
薬物/実験室試験の相互作用
セファロスポリン抗生物質による治療中に、陽性の直接クームス試験が報告されています。抗グロブリン検査がマイナー側で行われる場合の血液学的研究または輸血クロスマッチング手順、または母親が分娩前にセファロスポリン抗生物質を投与された新生児のクームス検査では、陽性のクームス検査が原因である可能性があることを認識する必要があります。薬。
警告
デュリセフ(セファドロキシル)による治療を開始する前に、患者が以前にセファドロクステル、セファロスポリン、ペニシリン、またはその他の薬物に対して過敏反応を起こしたことがあるかどうかを判断するために、慎重な問診を行う必要があります。この製品をペニシリン感受性の患者に投与する場合は、注意が必要です。なぜなら、β-ラクタム系抗生物質間の交差感受性が明確に文書化されており、ペニシリン アレルギーの既往のある患者の最大 10% で発生する可能性があるためです。
デュリセフ (セファドロキシル) に対するアレルギー反応が発生した場合は、薬を中止してください。深刻な急性過敏症反応は、臨床的に示されているように、酸素、静脈内輸液、静脈内抗ヒスタミン薬、コルチコステロイド、プレッサーアミン、および気道管理を含む、エピネフリンおよびその他の緊急措置による治療を必要とする場合があります。
クロストリジウム・ディフィシル関連下痢症 (CDAD) は、DUICEF (セファドロキシル) を含むほぼすべての抗菌薬の使用で報告されており、重症度は軽度の下痢から致命的な大腸炎までさまざまです。抗菌剤による治療は、結腸の正常な細菌叢を変化させ、C. difficile の異常増殖を引き起こします。
C. difficile は、CD AD の発症に寄与する毒素 A および B を産生します。 C. difficile の高毒素産生株は、これらの感染症が抗菌療法に抵抗性である可能性があり、結腸切除術を必要とする可能性があるため、罹患率と死亡率の増加を引き起こします。 CD AD は、抗生物質の使用後に下痢を呈するすべての患者で考慮されなければなりません。 CD AD は抗菌薬投与後 2 か月以上経過すると報告されているため、病歴には注意が必要です。
CD AD が疑われるか確認された場合、C. difficile に対するものではない継続的な抗生物質の使用を中止する必要があるかもしれません。適切な体液と電解質の管理、タンパク質の補給、C. difficile の抗生物質治療、および外科的評価を、臨床的に必要な場合に開始する必要があります。
予防
全般的
デュリセフ(セファドロキシル)は、腎機能が著しく損なわれている場合(クレアチニンクリアランス速度が50mL/分/1.73M2未満)には注意して使用する必要があります。 (見る 投薬と管理 .) 腎機能障害が既知または疑われる患者では、治療前および治療中に注意深い臨床観察および適切な検査を行う必要があります。
証明された、または強く疑われる細菌感染、または予防的適応がない場合にデュリセフ(セファドロキシル)を処方することは、患者に利益をもたらす可能性が低く、薬剤耐性菌の発生のリスクを高めます。
デュリセフ(セファドロキシル)を長期間使用すると、感受性生物が過剰増殖する可能性があります。患者の注意深い観察が不可欠です。治療中に重複感染が発生した場合は、適切な対策を講じる必要があります。
デュリセフ(セファドロキシル)は、胃腸疾患、特に大腸炎の病歴のある人には慎重に処方する必要があります。
発がん、突然変異誘発および生殖能力の障害
発がん性の可能性を判断するための長期研究は実施されていません。遺伝毒性試験は実施されていません。
妊娠: 妊娠カテゴリーB
生殖研究は、ヒト用量の最大 11 倍の用量でマウスとラットで実施されており、セファドロキシル一水和物による生殖能力の障害や胎児への害の証拠は明らかにされていません。しかし、妊娠中の女性を対象とした十分に管理された研究はありません。動物の繁殖研究は常に人間の反応を予測できるわけではないため、この薬は明らかに必要な場合にのみ妊娠中に使用する必要があります.
労働と配達
デュリセフ(セファドロキシル)の分娩中の使用については研究されていません。明らかに必要な場合にのみ治療を行うべきです。
授乳中の母親
セファドロキシル一水和物を授乳中の母親に投与する場合は注意が必要です。
小児用
(見る 投薬と管理。 )
高齢者の使用
つの臨床試験で尿路感染症の治療のためにセファドロキシルを投与された約 650 人の患者のうち、28% が 60 歳以上で、16% が 70 歳以上でした。 14件の臨床試験で皮膚および皮膚構造感染症の治療のためにセファドロキシルを投与された約1,000人の患者のうち、12%が60歳以上で、4%が70歳以上でした。これらの研究の高齢患者と若年患者との間で、安全性の全体的な違いは観察されませんでした。セファドロキシルの臨床研究。咽頭炎または扁桃炎の治療には、若い患者と異なる反応を示すかどうかを判断するのに十分な数の 65 歳以上の患者が含まれていませんでした。セファドロキシルに関する他の報告された臨床経験では、高齢患者と若年患者の反応の違いは確認されていませんが、一部の高齢者の感受性が高いことは除外できません。
セファドロキシルは実質的に腎臓から排泄されるため、腎障害のある患者には投与量の調整が必要です ( 用法・用量: 腎障害 )。高齢患者は腎機能が低下している可能性が高いため、投与量の選択には注意が必要であり、腎機能のモニタリングが役立つ場合があります。
過剰摂取
6 歳未満の子供を対象とした研究では、250 mg/kg 未満のセファロスポリンの摂取は有意な結果とは関連していないことが示唆されました。一般的なサポートと監視以外のアクションは必要ありません。量が 250 mg/kg を超える場合は、胃内容排出を誘導します。
5 人の無尿症患者では、6 ~ 8 時間の血液透析セッション中に、1 g の経口投与量の平均 63% が体から抽出されることが実証されました。
禁忌
デュリセフ(セファドロキシル)は、抗生物質のセファロスポリン群に対する既知のアレルギーのある患者には禁忌です。
臨床薬理学
デュリセフ(セファドロキシル)は経口投与後、急速に吸収されます。 500 mg および 1000 mg の単回投与後、平均ピーク血清濃度はそれぞれ約 16 および 28 μg/mL でした。測定可能なレベルは、投与後 12 時間で存在しました。薬物の 90% 以上が 24 時間以内に変化せずに尿中に排泄されます。 500 mg を 1 回経口投与した後の期間中の尿中濃度のピークは、約 1800 pg/mL です。投与量の増加は、一般に、DURICEF (セファドロキシル一水和物、USP) の尿中濃度に比例した増加をもたらします。尿中抗生物質濃度は、1 g の投与後、20 時間から 22 時間、感受性尿病原体の MIC を十分に超えて維持されました。
微生物学
インビトロ試験は、セファロスポリンが細胞壁合成を阻害するために殺菌性であることを示しています。セファドロキシルは、in vitro および臨床感染の両方で、次の微生物に対して活性があることが示されています ( 適応症 ):
ベータ溶血性レンサ球菌 ペニシリナーゼ産生株を含むブドウ球菌
ノート: Entervcoccus faecalis (以前の Streptococcus faecalis) および Enterococcus faecium (以前の Streptococcus faecium) のほとんどの菌株は、DURICEF (セファドロキシル) に対して耐性があります。エンテロバクター種のほとんどの菌株、モルガネラ モルガニ (以前のプロテウス モルガニ)、および P. ブルガリスに対しては活性がありません。シュードモナス属およびアシネトバクター・カルコアセチクス(以前のミマ属およびヘレリア属)に対しては活性がありません。
感受性試験: 拡散法
ゾーンの直径を測定する抗生物質ディスク感受性試験方法を使用すると、抗生物質感受性を正確に推定できます。セファドロキシルに対する生物の感受性を試験するためにディスクを使用することが推奨されている標準手順の 1 つは、セファロスポリン クラス (セファロチン) ディスクを使用します。解釈には、ディスク試験で得られた直径とセファドロキシルの最小発育阻止濃度 (MIC) との相関関係が含まれます。
30 µg のセファロチン ディスクを使用した標準的な単一ディスクの感受性試験の結果を示す検査室からのレポートは、次の基準に従って解釈する必要があります。
「感受性」のレポートは、病原体が一般的に達成可能な血中濃度によって抑制される可能性が高いことを示します。 「中程度の感受性」の報告は、高用量が使用された場合、または感染が高い抗生物質レベルに達した組織および体液 (尿など) に限定された場合、生物が感受性になることを示唆しています。 「耐性」の報告は、抗生物質の達成可能な濃度が阻害的である可能性が低く、他の治療法を選択する必要があることを示しています。
標準化された手順では、実験室の制御生物を使用する必要があります。 30 μg のセファロチン ディスクは、次のゾーン直径を与える必要があります。
希釈法
NCCLS 寒天希釈または培養液希釈 (微量希釈を含む) 法 2 または同等の方法を使用する場合、セファロチンの MIC (最小発育阻止濃度) 値が 8 µg/mL 以下の場合、細菌分離株は感受性があると見なすことができます。 MIC が 32 µg/mL 以上の場合、生物は耐性があると見なされます。 MIC 値が 32 µg/mL 未満で 8 µg/mL を超える生物は中間です。
標準的な拡散法と同様に、希釈手順では実験室の制御生物を使用する必要があります。標準的なセファロチン パウダーは、黄色ブドウ球菌 ATCC 29213 に対して 0.12 μg/mL から 0.5 μg/mL の範囲の MIC 値を与える必要があります。 Streptococcus faecalis ATCC 29212 の場合、MIC 範囲は 8.0 ~ 32.0 µg/mL である必要があります。
参考文献
1. 米国臨床検査基準委員会、承認基準、抗菌ディスク感受性試験の性能基準、第 4 版、Vol. 10 (7): M2-A4、ペンシルバニア州ヴィラノバ、1990 年 4 月。
2. 全米臨床検査基準委員会、承認基準:好気的に増殖する細菌の希釈抗菌剤感受性試験方法、第 2 版、Vol. 10 (8): M7-A2、ペンシルベニア州ヴィラノバ、1990 年 4 月。
患者情報
デュリセフ(セファドロキシル)を含む抗菌薬は、細菌感染症の治療にのみ使用するよう患者に説明する必要があります。ウイルス感染症(風邪など)は治療しません。デュリセフ(セファドロキシル)が細菌感染症の治療に処方されている場合、患者は治療の初期に気分が良くなるのが一般的ですが、指示どおりに薬を服用する必要があることを伝えなければなりません.投与をスキップしたり、治療の全コースを完了しなかったりすると、(1) 当面の治療の有効性が低下し、(2) 細菌が耐性を獲得し、DUICEF (セファドロキシル) または他の抗菌薬で将来的に治療できなくなる可能性が高くなる可能性があります。 .
下痢は抗生物質によって引き起こされる一般的な問題であり、通常は抗生物質の使用を中止すると終了します。抗生物質による治療を開始した後、患者は、抗生物質の最後の用量を服用してから2か月以上経っても、水様便や血便(胃痙攣や発熱の有無にかかわらず)を発症することがあります.これが発生した場合、患者はできるだけ早く医師に連絡する必要があります。
