Tofranil 25mg, 50mg, 75mg Imipramine 使用法、副作用および投与量。 オンライン薬局の価格。 処方箋不要のジェネリック医薬品。
トフラニールとは何ですか?
トフラニール 50mg は、うつ病の症状を治療するために使用される処方薬です。トフラニール 25mg は、単独で使用することも、他の薬と併用することもできます。
トフラニールは、抗うつ薬、TCA と呼ばれる種類の薬に属しています。
トフラニールが 6 歳未満の子供に安全で有効であるかどうかはわかっていません。
トフラニール 50mg の副作用の可能性は何ですか?
トフラニルは、次のような重大な副作用を引き起こす可能性があります。
- 気分や行動の変化、
- 不安、
- パニック発作、
- 寝られない、
- 衝動的な行動、
- 過敏性、
- 攪拌、
- 敵意、
- 侵略、
- 落ち着きのなさ、
- 多動性(精神的または肉体的)、
- より多くのうつ病、
- 自殺念慮、
- ぼやけた視界、
- 視野狭窄、
- 目の痛みや腫れ、
- ライトの周りにハローが見える
- 立ちくらみ、
- 胸痛の新規または悪化、
- ドキドキする心臓の鼓動、
- 胸の中でときめき、
- 突然のしびれや衰弱、
- 視覚、発話、バランスの問題、
- 熱、
- 喉の痛み、
- 錯乱、
- 幻覚、
- 異常な思考や行動、
- 痛みや排尿困難、
- 発作、および
- 皮膚や目の黄変(黄疸)
上記の症状がある場合は、すぐに医療機関を受診してください。
トフラニールの最も一般的な副作用は次のとおりです。
- ピリピリ感、
- 弱点、
- 協調性の欠如、
- 口渇、
- 吐き気、
- 嘔吐、
- 便秘、
- 下痢、
- 視界の変化、
- あなたの耳に鳴り響く、
- 乳房の腫れ(男性と女性の両方)、
- 性欲減退、
- インポテンス、および
- オーガズムを持つのが難しい
気になる副作用や治らない副作用がある場合は、医師に相談してください。
これらは、トフラニールの考えられるすべての副作用ではありません。詳細については、医師または薬剤師にお尋ねください。
自殺傾向と抗うつ薬
抗うつ薬は、大うつ病性障害(MDD)およびその他の精神障害の短期研究において、小児、青年、および若年成人の自殺念慮および自殺行動(自殺傾向)のリスクをプラセボと比較して増加させました。塩酸イミプラミンまたはその他の抗うつ薬を小児、青年、または若年成人に使用することを検討している人は誰でも、このリスクと臨床上の必要性とのバランスを取らなければなりません.短期間の研究では、24 歳を超える成人のプラセボと比較して、抗うつ薬による自殺のリスクの増加は示されませんでした。 65歳以上の成人では、プラセボと比較して抗うつ薬のリスクが低下しました.うつ病やその他の特定の精神障害は、それ自体が自殺のリスクの増加と関連しています。抗うつ薬治療を開始したすべての年齢の患者は、臨床的悪化、自殺傾向、または行動の異常な変化について適切に監視し、注意深く観察する必要があります。家族や介護者は、処方者との綿密な観察とコミュニケーションの必要性を知らされるべきです。塩酸イミプラミンは、小児患者への使用は承認されていません( 警告 、臨床症状の悪化と自殺のリスク。 予防 、患者のための情報;と 予防 、小児使用)。
説明
Tofranil™ は、経口投与用の錠剤の形で提供されます。
トフラニール 75mg、塩酸イミプラミン USP、元の三環系抗うつ薬は、化合物のジベンズアゼピン グループのメンバーです。これは、5-3-(ジメチルアミノ)プロピル-10,11-ジヒドロ-5Hジベンズ[b,f]-アゼピン一塩酸塩と呼ばれる。その構造式は次のとおりです。
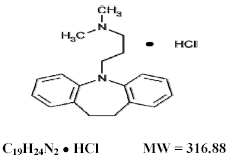
イミプラミン塩酸塩 USP は、白色からオフホワイト、無臭、または実質的に無臭の結晶性粉末です。水とアルコールに溶けやすく、アセトンに溶け、エーテルとベンゼンに溶けない。
不活性成分
リン酸カルシウム、セルロース化合物、ドキュセートナトリウム、酸化鉄、ステアリン酸マグネシウム、ポリエチレングリコール、ポビドン、デンプングリコール酸ナトリウム、スクロース、タルク、二酸化チタン。
適応症
うつ
うつ病の症状の緩和に。内因性うつ病は、他のうつ病状態よりも緩和される可能性が高くなります。最適な治療効果が明らかになるまでには、1 ~ 3 週間の治療が必要になる場合があります。
小児夜尿症
考えられる器質的な原因が適切な検査によって除外された後、6歳以上の子供の夜尿症を減らすための一時的な補助療法として役立つかもしれません.日中に頻繁に緊急の症状がみられる患者では、必要に応じて膀胱尿道造影および膀胱鏡検査を排尿検査に含める必要があります。投薬を続けると治療効果が低下することがあります。
投薬と管理
うつ
高齢者や青年には低用量が推奨されます。綿密な監視下にある入院患者と比較して、外来患者にも低用量が推奨されます.投与量は低レベルから開始し、臨床反応と不耐性の証拠を注意深く観察しながら徐々に増加させる必要があります。寛解に続いて、寛解を維持するための最低用量で、より長期間の維持投薬が必要になる場合があります。
通常の成人用量
入院患者
最初は 1 日 100 mg を分割して、必要に応じて 1 日 200 mg まで徐々に増やしました。 2 週間経っても反応がない場合は、1 日 250 ~ 300 mg に増やしてください。
外来患者
最初は、75 mg/日から 150 mg/日に増量されました。 200 mg/日を超える用量は推奨されません。維持、50 ~ 150 mg/日。
思春期および高齢者の患者
最初は、30~40mg/日。通常、1 日あたり 100 mg を超える必要はありません。
小児夜尿症
最初は、6 歳以上の子供に 25 mg/日の経口投与を試みる必要があります。投薬は就寝の1時間前に行う必要があります。 1 週間以内に満足のいく反応が得られない場合は、12 歳未満の子供では毎晩 50 mg に用量を増やします。 12 歳以上の子供は、毎晩最大 75 mg を受け取ることができます。 1 日 75 mg を超える用量では、有効性が向上せず、副作用が増加する傾向があります。エビデンスによると、夜更かしの患者では、薬剤をより早く、分割量(すなわち、午後半ばに 25 mg を就寝時に繰り返す)で投与するとより効果的であることが示唆されています。良好な反応が得られた適切な治療試験の後、薬物を使用しない期間を設定することを検討する必要があります。投与量は、突然中止するのではなく、徐々に減らしていく必要があります。これにより、再発する傾向が低下する可能性があります。薬を中止したときに再発した小児は、その後の一連の治療に必ずしも反応するとは限りません。
2.5 mg/kg/日の用量を超えてはなりません。この量の 2 倍の用量の小児患者で、未知の重要性の ECG 変化が報告されています。
6 歳未満の子供の夜尿症に対する一時的な補助療法としてのトフラニールの安全性と有効性は確立されていません。
供給方法
Tofranil™ (塩酸イミプラミン USP) の 3 つの強度は、次のとおりです。
– 三角形、両凸、サンゴ赤褐色、砂糖でコーティングされた錠剤で、片面に「10」が黒で刻印されています。
30本のボトル NDC 0406-9920-03 100本入 NDC 0406-9920-01
– 丸型、両凸、サンゴ赤褐色、砂糖でコーティングされた錠剤で、片面に「25」、もう片面に黒で刻印されています。
30本のボトル NDC 0406-9921-03 100本入 NDC 0406-9921-01
– 丸型、両凸、サンゴ赤褐色、砂糖でコーティングされた錠剤で、片面に「50」、もう片面に黒で刻印されています。
30本のボトル NDC 0406-9922-03 100本入 NDC 0406-9922-01
20° ~ 25°C (68° ~ 77°F) [USP 制御室温を参照] で保管してください。
チャイルド レジスタント クロージャー付きの密閉容器 (USP) に分注してください。
製造元: Patheon Inc. ウィットビー、オンタリオ、カナダ、L1N 5Z5。改訂: 2017 年 4 月
副作用
ノート – 以下のリストには、この特定の薬物で報告されていないいくつかの副作用が含まれていますが、三環系抗うつ薬間の薬理学的類似性により、トフラニール 25mg を投与する際に各反応を考慮する必要があります。
心臓血管: 起立性低血圧、高血圧、頻脈、動悸、心筋梗塞、不整脈、心ブロック、心電図変化、うっ血性心不全の沈降、脳卒中。
精神的: 幻覚、見当識障害、妄想を伴う混乱状態(特に高齢者)。不安、落ち着きのなさ、動揺;不眠症と悪夢;軽躁病;精神病の悪化。
神経学的: 四肢のしびれ、うずき、感覚異常;協調運動失調、運動失調、振戦;末梢神経障害;錐体外路症状;発作、脳波パターンの変化;耳鳴り。
抗コリン作用: 口渇、およびまれに、舌下腺炎を伴う;かすみ目、調節障害、散瞳;便秘、麻痺性イレウス;尿閉、排尿遅延、尿路の拡張。
アレルギー: 皮膚発疹、点状出血、蕁麻疹、かゆみ、光線過敏症;浮腫(一般的または顔と舌の);薬物熱;デシプラミンとの交差感受性。
血液学: 無顆粒球症を含む骨髄抑制;好酸球増加症;紫斑;血小板減少症。
胃腸: 吐き気と嘔吐、食欲不振、上腹部痛、下痢。独特の味覚、口内炎、腹部痙攣、黒い舌。
内分泌: 男性の女性化乳房;女性の乳房肥大と乳汁漏出;性欲の増加または減少、インポテンス;精巣腫脹;血糖値の上昇または低下;不適切な抗利尿ホルモン (ADH) 分泌症候群。
他の: 黄疸(閉塞性のシミュレート);肝機能の変化;体重の増減;汗;フラッシング;頻尿;眠気、めまい、衰弱、疲労;頭痛;耳下腺腫脹;脱毛症;落下傾向。
禁断症状: 中毒を示すものではありませんが、長期間の治療後に治療を突然中止すると、吐き気、頭痛、倦怠感が生じることがあります.
ノート – トフラニール 75mg で治療された遺尿症の子供では、最も一般的な有害反応は、神経過敏、睡眠障害、疲労感、軽度の胃腸障害です。これらは通常、投薬を継続したり、投薬量を減らしたりすると消失します。報告されているその他の反応には、便秘、痙攣、不安、情緒不安定、失神、虚脱などがあります。大人の使用で報告されたすべての悪影響を考慮する必要があります。
薬物相互作用
P450 2D6 によって代謝される薬物
薬物代謝アイソザイム シトクロム P450 2D6 (デブリソキン ヒドロキシラーゼ) の生化学的活性は、白人集団のサブセットで低下します (白人の約 7% から 10% は、いわゆる「低代謝者」です)。アジア人、アフリカ人、およびその他の集団におけるP450 2D6アイソザイム活性の低下の有病率の信頼できる推定値はまだ入手できていません。代謝が悪い人は、通常の用量で三環系抗うつ薬 (TCA) の血漿中濃度が予想よりも高くなります。 P450 2D6 によって代謝される薬物の割合に応じて、血漿濃度の増加は小さい場合もあれば、非常に大きい場合もあります (TCA の血漿 AUC の 8 倍の増加)。
さらに、特定の薬物はこのアイソザイムの活性を阻害し、正常な代謝者を低代謝者に似せます。所定の用量のTCAで安定している個人は、併用療法としてこれらの阻害薬の1つを投与すると、突然毒性になる可能性があります.シトクロム P450 2D6 を阻害する薬物には、酵素によって代謝されないもの (キニジン; シメチジン) や、P450 2D6 の基質となる多くの薬物 (他の多くの抗うつ薬、フェノチアジン、および 1C 型抗不整脈薬のプロパフェノンとフレカイニド) が含まれます。フルオキセチン、セルトラリン、パロキセチンなどのすべての選択的セロトニン再取り込み阻害剤 (SSRI) は P450 2D6 を阻害しますが、阻害の程度はさまざまです。 SSRI-TCA 相互作用が臨床上の問題を引き起こす可能性がある程度は、関連する SSRI の阻害の程度と薬物動態に依存します。それにもかかわらず、TCA と SSRI のいずれかとの同時投与、およびあるクラスから別のクラスへの切り替えには注意が必要です。特に重要なことは、フルオキセチンから離脱している患者で TCA 治療を開始する前に、親と活性代謝物の半減期が長いことを考えると、十分な時間が経過しなければならないことです (少なくとも 5 週間は必要な場合があります)。
チトクローム P450 2D6 を阻害できる薬と三環系抗うつ薬を併用する場合は、通常、三環系抗うつ薬または他の薬に処方される用量よりも少ない用量が必要になる場合があります。さらに、これらの他の薬のいずれかが併用療法から中止されるたびに、三環系抗うつ薬の増量が必要になる場合があります。 TCA が P450 2D6 の阻害剤であることが知られている別の薬物と同時投与される場合は常に、TCA 血漿レベルを監視することが望ましいです。
イミプラミンの血漿中濃度は、薬物が肝酵素阻害剤(シメチジン、フルオキセチンなど)と同時に投与されると増加し、肝酵素誘導剤(バルビツレート、フェニトインなど)との同時投与によって減少する可能性があるため、イミプラミンの投与量の調整が必要になる場合があります。必要があります。
時折感受性のある患者または抗コリン作動薬(抗パーキンソニズム薬を含む)を受けている患者では、アトロピン様作用がより顕著になることがあります(例、麻痺性イレウス)。塩酸イミプラミンを抗コリン薬と併用する場合は、厳重な管理と慎重な用量調節が必要です。
三環系抗うつ薬はカテコールアミンの効果を増強する可能性があることが報告されているため、うっ血除去薬や局所麻酔薬など、交感神経刺激アミン(エピネフリン、ノルエピネフリンなど)を含む製剤の使用は避けてください。
塩酸イミプラミンを血圧降下剤と併用する場合は注意が必要です。イミプラミン塩酸塩は、中枢神経系抑制薬の効果を増強する可能性があります。
患者は、塩酸イミプラミンがアルコールの CNS 抑制効果を増強する可能性があることを警告する必要があります。 警告 )。
警告
臨床的悪化と自殺リスク
成人および小児の大うつ病性障害(MDD)の患者は、抗うつ薬を服用しているかどうかにかかわらず、うつ病の悪化および/または自殺念慮および自殺行動(自殺傾向)の出現、または行動の異常な変化を経験する可能性があります。リスクは、有意な寛解が起こるまで持続する可能性があります。自殺は、うつ病やその他の特定の精神障害の既知のリスクであり、これらの障害自体が自殺の最も強力な予測因子です。しかし、抗うつ薬が治療の初期段階で特定の患者のうつ病の悪化と自殺傾向の出現を誘発する役割を果たしている可能性があるという長年の懸念がありました.抗うつ薬 (SSRI など) の短期プラセボ対照試験のプール分析では、これらの薬が大うつ病の子供、青年、若年成人 (18 歳から 24 歳) の自殺念慮および行動 (自殺傾向) のリスクを高めることが示されました。障害(MDD)およびその他の精神障害。短期間の研究では、24 歳を超える成人のプラセボと比較して、抗うつ薬による自殺のリスクの増加は示されませんでした。 65 歳以上の成人では、プラセボと比較して抗うつ薬が減少しました。
MDD、強迫性障害(OCD)、またはその他の精神障害を有する小児および青年を対象としたプラセボ対照試験のプール分析には、4,400 人を超える患者を対象とした 9 種類の抗うつ薬の合計 24 の短期試験が含まれていました。 MDD またはその他の精神障害を有する成人を対象としたプラセボ対照試験のプール分析には、77,000 人を超える患者を対象とした 11 種類の抗うつ薬の合計 295 件の短期試験 (期間の中央値は 2 か月) が含まれていました。薬物間で自殺のリスクにかなりのばらつきがありましたが、研究されたほとんどすべての薬物で若い患者が増加する傾向がありました。さまざまな適応症で自殺の絶対リスクに違いがあり、MDD での発生率が最も高かった。ただし、リスクの違い (薬物とプラセボ) は、年齢層内および適応症全体で比較的安定していました。これらのリスクの違い (治療を受けた患者 1000 人あたりの自殺傾向の症例数における薬物とプラセボの違い) を表 1 に示します。
どの小児科試験でも自殺は発生していません。成人試験では自殺がありましたが、自殺に対する薬物の影響について結論を出すには十分な数ではありませんでした。
自殺リスクが長期間の使用、つまり数ヶ月以上の使用に及ぶかどうかは不明です。しかし、うつ病の成人におけるプラセボ対照維持試験から、抗うつ薬の使用がうつ病の再発を遅らせることができるという実質的な証拠があります.
適応症を問わず抗うつ薬で治療されているすべての患者は、特に薬物療法のコースの最初の数か月間、または用量変更時に、臨床的悪化、自殺傾向、行動の異常な変化について適切に監視し、注意深く観察する必要があります。または減少します。
大うつ病性障害で抗うつ薬を服用している成人および小児患者においても、不安、興奮、パニック発作、不眠症、易怒性、敵意、攻撃性、衝動性、アカシジア(精神運動の落ち着きのなさ)、軽躁病、躁病の症状が報告されています。他の適応症に関しては、精神医学的および非精神医学的の両方です。そのような症状の出現と、うつ病の悪化および/または自殺衝動の出現との間の因果関係は確立されていませんが、そのような症状が自殺傾向の出現の前兆を表している可能性があるという懸念があります.
うつ病が持続的に悪化している患者、またはうつ病や自殺傾向の悪化の前兆である可能性のある緊急の自殺願望または症状を経験している患者では、場合によっては投薬を中止することを含め、治療計画の変更を検討する必要があります。特にこれらの症状が重度で突然の場合発症したか、患者の症状の一部ではありませんでした。
大うつ病性障害またはその他の適応症(精神医学的および非精神医学的両方)の抗うつ薬で治療されている患者の家族および介護者は、動揺、過敏性、行動の異常な変化、および上記のその他の症状の出現について患者を監視する必要性について警告する必要があります。 、および自殺傾向の出現、およびそのような症状を医療提供者に直ちに報告すること。このようなモニタリングには、家族や介護者による毎日の観察が含まれる必要があります。 塩酸イミプラミンの処方は、過剰摂取のリスクを軽減するために、適切な患者管理と一致する最小量の錠剤用に作成する必要があります。
双極性障害の患者のスクリーニング
大うつ病エピソードは、双極性障害の最初の症状である可能性があります。このようなエピソードを抗うつ薬のみで治療すると、双極性障害のリスクがある患者に混合/躁病エピソードが発生する可能性が高くなる可能性があると一般的に考えられています (対照試験では確立されていません)。上記の症状のいずれかがそのような変換を表しているかどうかは不明です。ただし、抗うつ薬による治療を開始する前に、抑うつ症状のある患者を適切にスクリーニングして、双極性障害のリスクがあるかどうかを判断する必要があります。そのようなスクリーニングには、自殺、双極性障害、うつ病の家族歴など、詳細な精神病歴を含める必要があります。塩酸イミプラミンは、双極性うつ病の治療に使用することは承認されていないことに注意してください。
閉塞隅角緑内障
トフラニールを含む多くの抗うつ薬の使用後に発生する瞳孔散大は、虹彩切除術を行っていない解剖学的に狭い隅角を持つ患者に閉鎖隅角発作を引き起こす可能性があります。
子供
トフラニール 25 mg の 2.5 mg/kg/日の用量は、小児期に超えてはなりません。この量の 2 倍の用量の小児患者で、未知の重要性の ECG 変化が報告されています。
伝導障害、不整脈、うっ血性心不全、心筋梗塞、脳卒中、および頻脈の可能性があるため、心血管疾患のある患者。これらの患者は、薬物のすべての用量レベルで心臓の監視が必要です。
薬物の抗コリン作用による尿閉の病歴、または狭隅角緑内障の病歴のある患者;心血管毒性の可能性があるため、甲状腺機能亢進症患者または甲状腺薬を服用している患者;
この薬は発作閾値を下げることが示されているため、発作障害の病歴のある患者;
グアネチジン、クロニジン、または同様の薬剤を投与されている患者。トフラニールはこれらの薬剤の薬理学的効果を阻害する可能性があるため。
メチルフェニデート塩酸塩を投与されている患者。メチルフェニデート塩酸塩はトフラニール75mgの代謝を阻害する可能性があるため、メチルフェニデート塩酸塩と併用する場合は、イミプラミン塩酸塩の用量調節が必要になる場合があります。
トフラニールは、アルコールの CNS 抑制効果を高める可能性があります。したがって、過剰な量のアルコールを使用している患者では、自殺未遂や偶発的な薬物の過剰摂取に固有の危険性が高まる可能性があることに留意する必要があります (以下を参照)。 予防 )。
トフラニールは、自動車や機械の操作など、潜在的に危険な作業の実行に必要な精神的および/または身体的能力を損なう可能性があるため、患者はそれに応じて注意する必要があります.
予防
全般的
トフラニールの通常より多量の投与を開始する前に、その後は安定状態に達するまで適切な間隔で心電図を記録する必要があります。 (心血管疾患の証拠がある患者は、薬物のすべての用量レベルで心臓の監視が必要です。 警告 .) 高齢患者および心疾患または心疾患の既往歴のある患者は、トフラニールの使用に関連する心臓異常を発症する特別なリスクがあります。
重度のうつ病患者の自殺の可能性は病気に固有のものであり、有意な寛解が得られるまで持続する可能性があることに留意する必要があります.このような患者は、トフラニール 75mg による治療の初期段階で注意深く監視する必要があり、入院が必要になる場合があります。処方箋は可能な限り最小限の金額で書かれるべきです。軽躁病または躁病エピソードが発生する可能性があり、特に周期性障害の患者で顕著です。このような反応は、薬物の中止を必要とする場合があります。必要に応じて、これらのエピソードが緩和されたら、トフラニール 75mg を低用量で再開することができます。
精神安定剤の投与は、そのようなエピソードを制御するのに役立つ場合があります。
精神病の活性化は、統合失調症患者で時折観察される場合があり、投与量の削減とフェノチアジンの追加が必要になる場合があります。
トフラニール 50mg と電気ショック療法の同時投与は、危険性を高める可能性があります。臨床経験が限られているため、そのような治療は、それが不可欠な患者に限定されるべきです。
塩酸イミプラミンを服用している患者は、光感作の報告があるため、過度の日光への曝露を避ける必要があります.
塩酸イミプラミンの使用により、血糖値の上昇と低下の両方が報告されています。
腎機能または肝機能が著しく低下している患者には、塩酸イミプラミンを慎重に使用する必要があります。
塩酸イミプラミンによる治療中に発熱と喉の痛みを発症した患者は、白血球と血球分画を実施する必要があります。病理学的好中球抑制の証拠がある場合は、塩酸イミプラミンを中止する必要があります。
待機的手術の前に、臨床状況が許す限り塩酸イミプラミンを中止する必要があります。
患者様向け情報
処方者または他の医療専門家は、患者、その家族、およびその介護者に、塩酸イミプラミンによる治療に関連する利点とリスクについて知らせ、適切な使用法について助言する必要があります。患者 投薬ガイド イミプラミン塩酸塩について「抗うつ薬、うつ病などの重篤な精神疾患、および自殺念慮または自殺行動」について掲載しています。処方者または医療専門家は、患者、その家族、および介護者に投薬ガイドを読むように指示し、その内容を理解できるように支援する必要があります。患者には、投薬ガイドの内容について話し合い、質問があれば回答を得る機会を与える必要があります。投薬ガイドの全文は、この文書の最後に転載されています。
患者は次の問題について知らされ、イミプラミン塩酸塩の服用中にこれらの問題が発生した場合は処方者に警告するよう求められる.
患者は、トフラニールを服用すると軽度の瞳孔散大を引き起こす可能性があり、影響を受けやすい個人では、閉塞隅角緑内障のエピソードにつながる可能性があることをアドバイスする必要があります.既存の緑内障は、ほとんどの場合、開放隅角緑内障です。診断された場合、閉塞隅角緑内障は虹彩切除術で確実に治療できるからです。開放隅角緑内障は、閉塞隅角緑内障の危険因子ではありません。患者は、隅角閉鎖の影響を受けやすいかどうかを判断するために検査を受け、影響を受けやすい場合は予防処置(虹彩切除術など)を受けることを希望する場合があります。
臨床的悪化と自殺リスク
患者、その家族、および介護者は、不安、動揺、パニック発作、不眠症、過敏性、敵意、攻撃性、衝動性、アカシジア(精神運動の落ち着きのなさ)、軽躁病、躁病、その他の行動の異常な変化の出現に注意するよう奨励されるべきである. 、うつ病の悪化、および自殺念慮、特に抗うつ薬治療中の初期および用量が上下に調整された場合。患者の家族や介護者は、変化が突然起こる可能性があるため、日常的にそのような症状の出現を探すようにアドバイスされるべきです.このような症状は、患者の処方者または医療専門家に報告する必要があります。特に、それらが重度である場合、突然発症する場合、または患者の症状の一部ではない場合はそうです。これらのような症状は、自殺念慮や行動のリスクの増加と関連している可能性があり、非常に綿密な監視と、場合によっては投薬の変更が必要であることを示しています.
妊娠
動物の生殖に関する研究では、決定的な結果が得られていません (以下も参照)。 動物薬理学 )。
胎児に対するトフラニールの効果を決定するために、妊婦を対象に実施された十分に管理された研究はありません.しかし、薬物の使用に関連する先天性奇形の臨床報告がありました。これらの影響と薬剤との因果関係は確立できませんでしたが、トフラニールの母体摂取による胎児リスクの可能性は排除できません。したがって、トフラニールは、臨床状態が胎児への潜在的なリスクを明らかに正当化する場合にのみ、妊娠中または妊娠する可能性のある女性に使用する必要があります.
授乳中の母親
限られたデータは、トフラニール 75mg がヒトの母乳に排泄される可能性が高いことを示唆しています。原則として、薬剤が母乳中に排泄され、子供に有害である可能性があるため、薬剤を服用している女性は看護を受けるべきではありません。
小児用
夜尿症の小児患者以外の小児集団における安全性と有効性は確立されていません。 ボックス警告 と 警告 、 臨床的悪化と自殺リスク )。小児または青年にイミプラミン塩酸塩の使用を検討している人は誰でも、潜在的なリスクと臨床上の必要性とのバランスを取らなければなりません.
6歳未満の小児患者における夜尿症の一時的補助療法としての安全性と有効性は確立されていません。
6歳以上の小児患者における夜尿症の補助療法としての長期慢性使用に対する薬物の安全性は確立されていません。良好な反応が得られた適切な治療試験の後、薬物を使用しない期間を設定することを検討する必要があります。
小児期には 2.5 mg/kg/日の用量を超えてはなりません。この量の 2 倍の用量の小児患者で、未知の重要性の ECG 変化が報告されています。
高齢者の使用
文献では、高齢者集団でトフラニール 50mg を使用して行われた、よく管理された無作為化二重盲検並行群比較臨床試験が 4 件ありました。これらの研究には合計651人の被験者が含まれていました。これらの研究では、若い被験者との比較は提供されていません。高齢者で特定された追加の有害な経験はありませんでした。
当初の申請におけるトフラニール 75mg の臨床試験には、65 歳以上の対象者が若い対象者と異なる反応を示すかどうかを判断するのに十分な数の対象者が含まれていませんでした。市販後の臨床経験では、高齢者と若年者の間の反応の違いは確認されていません。一般に、高齢者の用量選択は慎重に行う必要があり、通常は用量範囲の下限から開始します。これは、肝臓、腎臓、または心機能の低下、および付随する疾患または他の薬物療法の頻度が高いことを反映しています。
(こちらもご覧ください 投薬と管理 、 思春期 と 高齢患者 .)
(こちらもご覧ください 予防 、 全般的。 )
過剰摂取
このクラスの薬物の過剰摂取により死亡する可能性があります。複数の薬物摂取 (アルコールを含む) は、意図的な三環系の過剰摂取でよく見られます。管理は複雑で変化するため、医師は毒物管理センターに連絡して治療に関する最新情報を入手することをお勧めします。三環系の過剰摂取後、毒性の兆候と症状が急速に現れます。したがって、できるだけ早く病院の監視が必要です。
子供は、塩酸イミプラミンの急性過剰摂取に対して成人よりも敏感であると報告されています。特に、乳児や幼児の急性過剰摂取は、量に関係なく、深刻で致命的な可能性があると見なす必要があります。
徴候
これらは、吸収された薬物の量、患者の年齢、および薬物摂取と治療開始の間の間隔などの要因に応じて、重症度が異なる場合があります。過剰摂取の重大な症状には、不整脈、重度の低血圧、痙攣、および昏睡を含む中枢神経系の抑制が含まれます。心電図の変化、特に QRS 軸または幅の変化は、三環系毒性の臨床的に重要な指標です。
他の中枢神経系症状には、眠気、昏迷、運動失調、落ち着きのなさ、動揺、多動性反射、筋肉の硬直、アテトーゼ状および舞踏運動が含まれる場合があります。
心臓の異常には、頻脈およびうっ血性不全の徴候が含まれる場合があります。呼吸抑制、チアノーゼ、ショック、嘔吐、高熱、散瞳、発汗もみられることがあります。
管理
心電図を取得し、すぐに心臓の監視を開始します。患者の気道を保護し、静脈ラインを確立し、胃の除染を開始します。心臓モニタリングによる最低 6 時間の観察と、CNS または呼吸抑制、低血圧、不整脈および/または伝導ブロック、および発作の徴候の観察が必要です。この期間中にいつでも毒性の兆候が見られた場合は、長期にわたる監視が必要です。過剰摂取後、致命的な不整脈に陥った患者の症例報告があります。これらの患者は、死亡前に重大な中毒の臨床的証拠があり、ほとんどが不十分な消化管除染を受けていました。血漿薬物レベルのモニタリングは、患者の管理の指針とすべきではありません。
胃腸の除染
三環系の過剰摂取が疑われるすべての患者は、胃腸の除染を受ける必要があります。これには、大量の胃洗浄とそれに続く活性炭が含まれます。意識が損なわれている場合は、洗浄前に気道を確保する必要があります。嘔吐は禁忌です。
心臓血管
≥0.10 秒の最大四肢誘導 QRS 持続時間は、過剰摂取の重症度を示す最良の指標である可能性があります。静脈内重炭酸ナトリウムを使用して、血清pHを7.45~7.55の範囲に維持する必要があります。 pH 応答が不十分な場合は、過換気も使用できます。過換気と重炭酸ナトリウムの併用は、頻繁に pH をモニタリングしながら、細心の注意を払って行う必要があります。 pH >7.60 または pCO2
まれに、血液灌流は、急性毒性のある患者の急性難治性心血管不安定性に有益な場合があります。しかし、血液透析、腹膜透析、交換輸血、および強制利尿は、一般に、三環系中毒には効果がないと報告されています。
中枢神経系
CNS 抑制の患者では、急激な悪化の可能性があるため、早期の挿管が推奨されます。発作はベンゾジアゼピンで制御する必要があります。これらが無効な場合は、他の抗けいれん薬(例、フェノバルビタール、フェニトイン)で制御する必要があります。フィゾスチグミンは、他の治療法に反応しなかった生命を脅かす症状を治療する場合を除いて推奨されず、毒物管理センターと相談する場合にのみ推奨されます.
精神科のフォローアップ
過剰摂取はしばしば意図的なものであるため、患者は回復期に他の手段で自殺を試みる可能性があります。精神科への紹介が適切かもしれません。
小児管理
子供と大人の過剰摂取の管理の原則は似ています。特定の小児科の治療については、医師が地元の毒物管理センターに連絡することを強くお勧めします。
禁忌
モノアミンオキシダーゼ阻害化合物の併用は禁忌です。このような組み合わせを受けた患者では、高熱発作または重度のけいれん発作が発生する可能性があります。副作用の増強は深刻な場合もあれば、致命的な場合さえあります。モノアミンオキシダーゼ阻害剤を投与されている患者でトフラニールを代用したい場合は、臨床状況が許す限り、最低でも 14 日間の間隔を空ける必要があります。最初の投与量は低くすべきであり、増加は段階的かつ慎重に処方する必要があります.
この薬は、心筋梗塞後の急性回復期には禁忌です。この化合物に対する既知の過敏症のある患者には、この薬を投与しないでください。他のジベンズアゼピン化合物に対する交差感受性の可能性に留意する必要があります。
臨床薬理学
トフラニール 25mg の作用機序は明確にわかっていません。しかし、主に中枢神経系の刺激によって作用するわけではありません。臨床効果は、神経終末でのノルエピネフリンの取り込みをブロックすることによるアドレナリン作動性シナプスの増強によるものと仮定されています。小児夜尿症の制御における薬物の作用機序は、その抗うつ効果とは別物であると考えられています。
動物薬理学および毒物学
A.急性
経口 LD50 の範囲は次のとおりです。
ラット 355~682mg/kg イヌ 100~215mg/kg
両種の投与量に応じて、毒性の兆候は、抑うつ、不規則な呼吸、運動失調から、痙攣や死へと進行しました。
B. 生殖/催奇形性
全体的な評価は、次のように要約できます。
経口: 3 種 (ラット、マウス、およびウサギ) での独立した研究により、トフラニールを経口投与すると、最初の 2 種ではヒトの最大用量の約 2.5 倍、ヒトの最大用量の 25 倍までの用量で投与されることが明らかになりました。 3 番目の種の用量では、薬物は本質的に催奇形性の可能性がありません。研究された 3 つの種では、胎児の異常は 1 例だけ (ウサギで) 発生し、その研究では対照群にも同様の異常がありました。しかし、ラットの研究から、全身毒性および胚毒性の可能性が実証可能であるという証拠が存在します。これは、同腹子数の減少、死産率のわずかな増加、および平均出生体重の減少によって明らかになります。
