Naprelan 250mg, 500mg Naproxen 使用法、副作用および投与量。 オンライン薬局の価格。 処方箋不要のジェネリック医薬品。
ナプレランとは何ですか?
ナプレランは、関節リウマチ、変形性関節症、アンキロシン脊椎炎、月経困難症、急性痛風および疼痛の症状を治療するために使用される処方薬です。ナプレランは、単独で使用することも、他の薬と併用することもできます。
ナプレランは、NSAIDs と呼ばれる薬物のクラスに属します。
ナプレラン 250mg が 2 歳未満の子供に安全で効果的かどうかはわかっていません。
ナプレラン 500mg の副作用の可能性は何ですか?
ナプレランは、次のような重大な副作用を引き起こす可能性があります。
- 蕁麻疹、
- 呼吸困難、
- 顔、唇、舌、喉の腫れ、
- あざや出血しやすい、
- 困難または痛みを伴う嚥下、
- 耳鳴り、
- 気分の変化、
- 尿量の変化、
- 原因不明の肩こり、
- 視界の変化、
- 足首や足のむくみ、
- 異常な疲労感
- 異常で突然の体重増加、
- 暗い尿、
- 持続的な吐き気や嘔吐、
- 食欲減少、
- 腹痛、
- 目や皮膚が黄色くなる(黄疸)
- 重度のめまい
上記の症状がある場合は、すぐに医療機関を受診してください。
ナプレランの最も一般的な副作用は次のとおりです。
- 胃のむかつき、
- 吐き気、
- 胸焼け、
- 頭痛、
- 血圧上昇
- 眠気、および
- めまい
気になる副作用や治らない副作用がある場合は、医師に相談してください。
これらは、ナプレランの考えられるすべての副作用ではありません.詳細については、医師または薬剤師にお尋ねください。
副作用に関する医学的アドバイスについては、医師に連絡してください。 1-800-FDA-1088 で副作用を FDA に報告できます。
警告
重篤な心血管および胃腸イベントのリスク
心血管血栓性イベント
- 非ステロイド性抗炎症薬 (NSAID) は、心筋梗塞や脳卒中などの重篤な心血管血栓性イベントのリスクを高め、致命的になる可能性があります。このリスクは、治療の初期に発生する可能性があり、使用期間とともに増加する可能性があります [警告と注意事項を参照]。
- NAPRELAN は、冠動脈バイパス移植 (CABG) 手術の設定では禁忌です [禁忌および警告と注意事項を参照]。
消化管出血、潰瘍、および穿孔
- NSAID は、胃や腸の出血、潰瘍、穿孔など、致命的な可能性がある重篤な胃腸 (GI) の有害事象のリスクを高めます。これらのイベントは、使用中にいつでも発生する可能性があり、警告の症状はありません。高齢患者および消化性潰瘍疾患および/または消化管出血の既往歴のある患者は、深刻な消化管イベントのリスクが高くなります[警告と注意事項を参照]。
説明
NAPRELAN (ナプロキセン ナトリウム) 放出制御錠は、経口投与用の 375 mg、500 mg、および 750 mg の放出制御錠として入手可能な非ステロイド性抗炎症薬です。化学名は2-ナフタレン酢酸、6-メトキシ-α-メチル-ナトリウム塩、(S)-です。分子量は252.24です。その分子式は C14H13NaO3 で、次の化学構造を持っています。
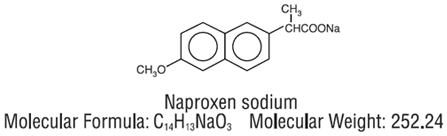
ナプロキセン ナトリウムは無臭の結晶性粉末で、白色からクリーム色です。メタノールと水に溶けます。 NAPRELAN 250mg 錠剤には、412.5 mg、550 mg、または 825 mg のナプロキセン ナトリウムが含まれており、それぞれ 375 mg、500 mg、および 750 mg のナプロキセンと、37.5 mg、50 mg、および 75 mg のナトリウムに相当します。各 NAPRELAN 250mg タブレットには、次の不活性成分も含まれています: メタクリル酸アンモニウム コポリマー タイプ A、メタクリル酸アンモニウム コポリマー タイプ B、クエン酸、クロスポビドン、ステアリン酸マグネシウム、メタクリル酸コポリマー タイプ A、微結晶性セルロース、ポビドン、およびタルク。錠剤のコーティングには、ヒドロキシプロピルメチルセルロース、ポリエチレングリコール、および二酸化チタンが含まれています。
適応症
ナプレラン 250mg 錠は、以下の治療に適応されます。
- 関節リウマチ(RA)
- 変形性関節症(OA)
- 強直性脊椎炎 (AS)
- 腱炎、滑液包炎
- 急性痛風
- 原発性月経困難症 (PD)
- 軽度から中等度の痛みの軽減
 [参照 警告と注意事項 ]。
投薬と管理
一般的な投与指示
NAPRELAN の使用を決定する前に、NAPRELAN およびその他の治療オプションの潜在的な利点とリスクを慎重に検討してください。個々の患者の治療目標に一致する最短の期間で最低の有効用量を使用する [参照 警告と注意事項 ]。
NAPRELAN による初期治療に対する反応を観察した後、個々の患者のニーズに合わせて用量と頻度を調整する必要があります。
関節リウマチ、変形性関節症、強直性脊椎炎
成人におけるナプレラン錠の推奨開始用量は、ナプレラン 375 mg 錠 (750 mg) を 1 日 1 回 2 錠、ナプレラン 750 mg 錠 (750 mg) を 1 日 1 回 1 錠、ナプレラン 500 mg 錠 (1,000 mg) を 1 日 1 回 2 錠です。すでにナプロキセン 250mg、375mg、または 500mg を 1 日 2 回(朝晩)服用している患者は、1 日 1 回の服用量としてナプロキセン 500mg 錠に置き換えてください。
長期投与中、ナプレラン 250mg 錠の投与量は、患者の臨床反応に応じて増減することがあります。低用量のナプレラン錠に十分に耐えられる患者では、より高いレベルの抗炎症作用が得られる限られた期間、1 日 1 回ナプレラン 750 mg 錠 (1,500 mg) 2 錠、またはナプレラン 500 mg 錠 (1,500 mg) 3 錠に増量することができます。 /鎮痛作用が必要です。特に高用量レベルで患者を治療する場合、医師は、潜在的なリスクの増加を相殺するのに十分な臨床的利益の増加を観察する必要があります[参照 臨床薬理学 ]。最小の有効用量を求め、すべての患者で使用する必要があります。関節炎の症状の改善は通常 1 週間以内に始まります。ただし、治療効果を得るには 2 週間の治療が必要な場合があります。
疼痛、原発性月経困難症、急性の腱炎および滑液包炎の管理
推奨開始用量は、ナプレラン 500 mg 錠 (1,000 mg) を 1 日 1 回 2 錠です。より大きな鎮痛効果を必要とする患者には、限られた期間、ナプレラン750mg錠(1,500mg)を2錠、またはナプレラン500mg錠(1,500mg)を3錠使用することができます。その後、1日総量はナプレラン500mg錠2錠(1,000mg)を超えないこと。
急性痛風
1日目の推奨用量は、ナプレラン500mg錠2~3錠(1,000~1,500mg)を1日1回、その後ナプレラン500mg錠2錠(1,000mg)を1日1回、発作がおさまるまで服用することです。
肝障害患者における用量調整
腎障害または肝障害のある患者または高齢の患者では、より低い用量を考慮する必要があります。 警告と注意事項 ]。調査によると、ナプロキセンの総血漿濃度は変化していませんが、ナプロキセンの非結合血漿分画は高齢者で増加しています。高用量が必要な場合は注意が必要であり、高齢の患者では用量の調整が必要になる場合があります。高齢者に使用される他の薬と同様に、最小の有効用量を使用することが賢明です.
供給方法
剤形と強度
NAPRELAN (ナプロキセン ナトリウム) 徐放性錠剤は、次のように入手できます。
- NAPRELAN 375:片面に「N」、裏面に「375」の白いカプセル型の錠剤。各錠剤には、ナプロキセン 375 mg に相当する 412.5 mg のナプロキセン ナトリウムが含まれています。
- NAPRELAN 500:片面に「N」、裏面に「500」と書かれた白いカプセル型の錠剤。各錠剤には、500 mg のナプロキセンに相当する 550 mg のナプロキセン ナトリウムが含まれています。
- NAPRELAN 750:片面に「N」、裏面に「750」の白色のカプセル型錠剤。各錠剤には、ナプロキセン 750 mg に相当する 825 mg のナプロキセン ナトリウムが含まれています。
保管と取り扱い
ナプレラン(ナプロキセンナトリウム) 375 mg、500 mg、および 750 mg は制御放出錠剤で、次のように供給されます。
ナプレラン375 : 白色のカプセル状の錠剤で、片面に「N」、裏面に「375」。 100本のボトルで。 NDC 52427-272-01。各錠剤には、ナプロキセン 375 mg に相当する 412.5 mg のナプロキセン ナトリウムが含まれています。
ナプレラン500 : 片面に「N」、裏面に「500」の白色のカプセル型錠剤。 75本のボトルで。 NDC 52427-273-75。各錠剤には、500 mg のナプロキセンに相当する 550 mg のナプロキセン ナトリウムが含まれています。
ナプレラン750 : 片面に「N」、裏面に「750」の白色のカプセル型錠剤。 30本のボトルで。 NDC 52427-274-30。各錠剤には、ナプロキセン 750 mg に相当する 825 mg のナプロキセン ナトリウムが含まれています。
保管所
室温、20° ~ 25°C (68° ~ 77°F)、15° ~ 30°C (59° ~ 86°F) の範囲で保管してください [USP 制御室温を参照]。薬剤師: 密閉容器に調剤してください。
販売元: Almatica Pharma, Inc. Morristown, NJ 07960 USA.改訂: 2021 年 4 月
副作用
次の副作用については、ラベルの他のセクションで詳しく説明しています。
- 心血管血栓性イベント [参照 警告と注意事項 ]
- 消化管出血、潰瘍および穿孔 [参照 警告と注意事項 ]
- 肝毒性 [参照 警告と注意事項 ]
- 高血圧 [参照 警告と注意事項 ]
- 心不全および浮腫 [参照 警告と注意事項 ]
- 腎毒性および高カリウム血症 [参照 警告と注意事項 ]
- アナフィラキシー反応 [参照 警告と注意事項 ]
- 深刻な皮膚反応 [参照 警告と注意事項 ]
- 血液毒性 [参照 警告と注意事項 ]
臨床試験の経験
臨床試験はさまざまな条件下で実施されるため、ある医薬品の臨床試験で観察された副作用率を別の医薬品の臨床試験で観察された率と直接比較することはできず、実際に観察された率を反映していない可能性があります。
このクラスのすべての薬と同様に、有害事象の頻度と重症度はいくつかの要因によって異なります。患者の年齢、性別、体調同時に発生する医学的診断または個々の危険因子。以下の副作用は、頻度と、これらの有害事象との因果関係の可能性の有無に基づいて、3つの部分に分けられます。 「因果関係の可能性」としてリストされている反応には、薬物使用と報告された事象との間に因果関係があることを示唆する証拠がある各副作用について少なくとも1つのケースがあります.報告された有害反応は、3 か月間の 2 つの二重盲検対照臨床試験の結果に基づいており、さらに 9 か月の非盲検延長が行われました。合計 542 人の患者が、二重盲検期間または 9 か月間の非盲検延長期間のいずれかで NAPRELAN 錠の投与を受けました。これら 542 人の患者のうち、232 人が NAPRELAN 錠の投与を受け、167 人が最初に Naprosyn® で治療され、143 人が最初にプラセボで治療されました。ナプレラン 500mg 錠を投与された患者から報告された副作用を体のシステム別に示します。ナプロキセンで観察されたが、ナプロラン錠を使用した対照試験で報告されていない有害反応はイタリック体で表示されています。
二重盲検および非盲検臨床試験で最も頻繁に見られた有害事象は頭痛 (15%) で、続いて消化不良 (14%)、インフルエンザ症候群 (10%) でした。患者の 3% から 9% で発生するその他の有害事象の発生率は、アスタリスクでマークされています。
患者の 3% 未満で発生するこれらの反応はマークされていません。
発生率 1%以上 (因果関係の可能性あり)
全身 - 痛み(背中)*、痛み*、感染症*、発熱、怪我(事故)、無力症、胸痛、頭痛(15%)、インフルエンザ症候群(10%)。
胃腸 - 吐き気*、下痢*、便秘*、腹痛*、鼓腸、胃炎、嘔吐、嚥下障害、消化不良 (14%)、胸やけ*、口内炎。
血液学 - 貧血、斑状出血。
呼吸器 - 咽頭炎*、鼻炎*、副鼻腔炎*、気管支炎、咳が増加しました。
腎臓 - 尿路感染*、膀胱炎。
皮膚科 - 皮膚発疹*、皮疹*、斑状出血*、紫斑。
代謝と栄養 - 末梢浮腫、高血糖。
中枢神経系 - めまい、感覚異常、不眠症、眠気*、立ちくらみ。
心臓血管 - 高血圧、浮腫*、呼吸困難*、動悸。
筋骨格 - けいれん(足)、筋肉痛、関節痛、関節障害、腱障害。
特別な感覚 - 耳鳴り*、聴覚障害、視覚障害。
全般的 - 渇き。
発生率 1%未満(因果関係の可能性あり)
全身 - 膿瘍、モニリア、首の硬直、首の痛み、腹部の肥大、がん、蜂窩織炎、浮腫全般、LE症候群、倦怠感、粘膜障害、アレルギー反応、骨盤痛。
胃腸 - 食欲不振、胆嚢炎、胆石症、おくび、消化管出血、直腸出血、アフタ性口内炎、口内炎、口内炎、胃潰瘍、歯周膿瘍、心臓痙攣、大腸炎、食道炎、胃腸炎、消化管障害、直腸障害、歯障害、肝脾腫、肝機能異常、下血、食道潰瘍、吐血、黄疸、膵炎、壊死。
腎臓 - 月経困難症、排尿困難、腎機能異常、夜間頻尿、前立腺障害、腎盂腎炎、乳房癌、尿失禁、腎結石、腎不全、月経過多、子宮出血、乳房新生物、腎硬化症、血尿、腎臓痛、膿尿、尿異常、頻尿、尿貯留、子宮けいれん、膣炎、糸球体腎炎、高カリウム血症、間質性腎炎、ネフローゼ症候群、腎疾患、腎不全、腎乳頭壊死。
血液学 - 白血球減少症、出血時間の増加、好酸球増加症、異常な赤血球、異常な白血球、血小板減少症、無顆粒球症、顆粒球減少症。
中枢神経系 - 抑うつ、不安、筋緊張亢進、神経過敏、神経痛、神経炎、めまい、記憶喪失、錯乱、協調運動障害、異常複視、情緒不安定、硬膜下血腫、麻痺、夢異常、集中力低下、筋力低下
皮膚科: 血管性皮膚炎、単純ヘルペス、乾燥肌、発汗、皮膚潰瘍、にきび、脱毛症、接触皮膚炎、湿疹、帯状疱疹、爪障害、皮膚壊死、皮下結節、そう痒症、蕁麻疹、皮膚新生物、光過敏性皮膚炎、遅発性ポルフィリン症に似た光過敏反応、表皮水疱症。
特別な感覚 - 弱視、強膜炎、白内障、結膜炎、難聴、耳障害、角結膜炎、流涙障害、中耳炎、眼痛。
心臓血管 - 狭心症、冠動脈疾患、心筋梗塞、深部血栓性静脈炎、血管拡張、血管異常、不整脈、脚ブロック、心電図異常、右心不全、出血、片頭痛、大動脈弁狭窄症、失神、頻脈、うっ血性心不全。
呼吸器 - 喘息、呼吸困難、肺水腫、喉頭炎、肺障害、鼻出血、肺炎、呼吸困難、呼吸障害、好酸球性肺炎。
筋骨格 - 筋無力症、骨障害、自然骨折、線維性腱炎、骨痛、眼瞼下垂、一般的なけいれん、滑液包炎。
代謝と栄養 - クレアチニン上昇、糖尿、高コレステロール血症、アルブミン尿、アルカローシス、BUN上昇、脱水、浮腫、耐糖能低下、高尿酸血症、低カリウム血症、SGOT上昇、SGPT上昇、体重減少。
全般的 - アナフィラキシー様反応、血管神経性浮腫、月経障害、低血糖、発熱(悪寒および発熱)。
発生率 1%未満(因果関係不明)
ナプロキセンのパッケージラベルに記載されているが、ナプロラン錠を服用した人によって報告されていないその他の副作用は斜体で示されています.これらの観察結果は、医師への警告情報としてリストされています。
血液学 - 再生不良性貧血、溶血性貧血。
中枢神経系 - 無菌性髄膜炎、認知機能障害。
皮膚科 - 表皮壊死融解症、多形紅斑、スティーブンス・ジョンソン症候群。
胃腸 - 非消化性消化管潰瘍、潰瘍性口内炎。
心臓血管 - 血管炎。
薬物相互作用
ナプロキセンとの臨床的に重要な薬物相互作用については、表 1 を参照してください。
薬物/実験室試験の相互作用
警告
の一部として含まれています 予防 セクション。
予防
心血管血栓性イベント
いくつかの COX-2 選択的および非選択的 NSAID の最大 3 年間の臨床試験では、致命的な可能性がある心筋梗塞 (MI) や脳卒中などの重篤な心血管 (CV) 血栓症のリスクが増加することが示されています。利用可能なデータに基づくと、CV 血栓イベントのリスクがすべての NSAID で同様であることは明らかではありません。 NSAID の使用によってもたらされるベースラインを超える重篤な心血管血栓性イベントの相対的な増加は、既知の心血管疾患または心血管疾患の危険因子がある場合とない場合で同様であるように思われます。しかし、既知の心血管疾患または危険因子を持つ患者は、ベースライン率が高いため、過剰な重篤な心血管血栓イベントの絶対発生率が高くなりました。いくつかの観察研究では、深刻な CV 血栓症のリスクの増加は、治療の最初の数週間で始まったことがわかりました。 CV 血栓リスクの増加は、高用量で最も一貫して観察されています。
NSAID 治療を受けている患者の有害な CV イベントの潜在的なリスクを最小限に抑えるために、可能な限り短い期間で最小の有効用量を使用してください。医師と患者は、以前の心血管症状がなくても、治療過程全体を通して、そのような事象の発生に注意を払う必要があります。重篤な心血管イベントの症状と、発生した場合の対処法について、患者に説明する必要があります。
アスピリンの同時使用が、NSAID の使用に関連する重篤な CV 血栓イベントのリスク増加を軽減するという一貫した証拠はありません。アスピリンとナプロキセンなどの NSAID の同時使用は、重篤な胃腸(GI)イベントのリスクを高める [参照 警告と注意事項 ]。
冠動脈バイパス移植(CABG)手術後の状態
CABG 手術後の最初の 10 ~ 14 日間の痛みの治療のための COX-2 選択的 NSAID の 2 つの大規模な対照臨床試験では、心筋梗塞と脳卒中の発生率が増加していることがわかりました。 NSAIDs は、CABG の状況では禁忌です [参照 禁忌 ]。
MI後の患者
デンマーク国民登録簿で実施された観察研究では、MI 後の期間に NSAID で治療された患者は、治療の最初の週から、再梗塞、心血管関連死、および全死因死亡のリスクが高いことが示されました。この同じコホートでは、MI 後 1 年間の死亡率は、非 NSAID 曝露患者では 100 人年あたり 12 であるのに対し、NSAID 治療患者では 100 人年あたり 20 でした。絶対死亡率は MI 後 1 年目から幾分低下したが、NSAID 使用者の死亡の相対リスクの増加は、少なくともその後 4 年間の追跡調査で持続した。
最近心筋梗塞を発症した患者では、CV 血栓性イベントの再発のリスクを上回ると期待される場合を除き、NAPRELAN 250mg の使用を避けてください。最近心筋梗塞を起こした患者に NAPRELAN を使用する場合は、心虚血の徴候がないか患者を監視してください。
消化管出血、潰瘍、および穿孔
ナプロキセンを含む NSAIDs は、食道、胃、小腸、または大腸の炎症、出血、潰瘍、穿孔など、致命的な可能性がある重篤な胃腸 (GI) の有害事象を引き起こします。これらの重篤な有害事象は、NSAID で治療されている患者において、警告症状の有無にかかわらず、いつでも発生する可能性があります。 NSAID 療法で重篤な上部消化管の有害事象を発症した患者の 5 人に 1 人のみが症状を示します。 NSAID による上部消化管潰瘍、肉眼的出血、または穿孔は、3 ~ 6 か月間治療を受けた患者の約 1%、1 年間治療を受けた患者の約 2% ~ 4% で発生しました。ただし、短期間の NSAID 治療でもリスクがないわけではありません。
消化管出血、潰瘍、および穿孔の危険因子
消化性潰瘍疾患および/または消化管出血の既往歴があり、NSAID を使用した患者は、これらの危険因子のない患者と比較して、消化管出血を発症するリスクが 10 倍以上高くなりました。 NSAID で治療された患者の消化管出血のリスクを高めるその他の要因には、NSAID 治療の長期化が含まれます。経口コルチコステロイド、アスピリン、抗凝固薬、または選択的セロトニン再取り込み阻害薬(SSRI)の併用。喫煙;アルコールの使用;高齢;および一般的な健康状態が悪い。致命的な消化管イベントに関する市販後の報告のほとんどは、高齢者または衰弱した患者で発生しました。さらに、進行した肝疾患および/または凝固障害のある患者は、消化管出血のリスクが高くなります。
NSAID 治療患者の消化管リスクを最小限に抑えるための戦略
- 可能な限り短い期間で最低の有効量を使用してください。
- 一度に複数の NSAID を投与することは避けてください。
- 利点が出血のリスクの増加を上回ると予想される場合を除き、リスクの高い患者への使用は避けてください。そのような患者、および活動性消化管出血のある患者については、NSAIDs 以外の代替療法を検討してください。
- NSAID 治療中は、消化管潰瘍や出血の徴候や症状に注意してください。
- 深刻な消化管有害事象が疑われる場合は、直ちに評価と治療を開始し、深刻な消化管有害事象が除外されるまで NAPRELAN 250mg を中止してください。
- 心臓予防のために低用量アスピリンを併用している状況では、消化管出血の証拠について患者をより綿密に監視する[参照 薬物相互作用 ]。
肝毒性
ALT または AST の上昇 (正常 [ULN] の上限の 3 倍以上) が、臨床試験で NSAID 治療を受けた患者の約 1% で報告されています。さらに、劇症肝炎、肝壊死、肝不全などのまれな、時には致命的な重度の肝障害の症例が報告されています。
ALT または AST の上昇 (ULN の 3 倍未満) は、ナプロキセンを含む NSAID で治療された患者の最大 15% で発生する可能性があります。
肝毒性の徴候と症状(吐き気、疲労、無気力、下痢、かゆみ、黄疸、右上腹部圧痛、「インフルエンザ様」症状など)について患者に知らせる。肝疾患に一致する臨床徴候および症状が発現した場合、または全身症状が発生した場合(例、好酸球増加症、発疹など)、ナプレラン 500mg を直ちに中止し、患者の臨床評価を実施してください。
高血圧症
NAPRELAN を含む NSAID は、既存の高血圧症の新たな発症または悪化につながる可能性があり、いずれも CV イベントの発生率の増加に寄与する可能性があります。アンギオテンシン変換酵素 (ACE) 阻害薬、サイアザイド利尿薬、またはループ利尿薬を服用している患者は、NSAID を服用すると、これらの治療に対する反応が損なわれる可能性があります [参照 薬物相互作用 ]。
NSAID 治療の開始時および治療中は、血圧 (BP) を監視します。
心不全と浮腫
Coxib と従来の NSAID Trialists’ Collaboration によるランダム化比較試験のメタ分析では、COX-2 選択的治療を受けた患者と非選択的 NSAID 治療を受けた患者では、プラセボ治療を受けた患者と比較して、心不全による入院が約 2 倍増加したことが示されました。心不全患者を対象としたデンマーク国立登録簿の研究では、NSAID の使用により心筋梗塞、心不全による入院、および死亡のリスクが増加しました。
さらに、体液貯留と浮腫は、NSAID で治療された一部の患者で観察されています。ナプロキセンの使用は、これらの病状の治療に使用されるいくつかの治療薬(例、利尿薬、ACE 阻害薬、またはアンギオテンシン受容体遮断薬 [ARB])の CV 効果を鈍らせる可能性があります。 薬物相互作用 ]。
ベネフィットが心不全の悪化のリスクを上回ると予想される場合を除き、重度の心不全患者への NAPRELAN 250mg の使用は避けてください。重度の心不全患者にナプレランを使用する場合は、心不全の悪化の徴候がないか患者を監視してください。
腎毒性と高カリウム血症
腎毒性
NSAIDs の長期投与は、腎乳頭壊死およびその他の腎損傷をもたらしました。
腎毒性は、腎プロスタグランジンが腎灌流の維持において代償的役割を果たしている患者にも見られます。これらの患者では、NSAID の投与によりプロスタグランジン生成が用量依存的に減少し、二次的に腎血流が減少し、明らかな腎代償不全が引き起こされる可能性があります。この反応のリスクが最も高い患者は、腎機能障害、脱水、循環血液量減少、心不全、肝機能障害、利尿薬および ACE 阻害薬または ARB を服用している患者、および高齢者です。通常、NSAID 療法を中止すると、治療前の状態に戻ります。
進行した腎疾患患者におけるNAPRELANの使用に関する対照臨床試験から得られる情報はありません。ナプレラン 250mg の腎作用は、既存の腎疾患を有する患者の腎機能障害の進行を早める可能性があります。
NAPRELAN を開始する前に、脱水症または血液量減少症の患者の体液量の状態を修正します。 NAPRELAN の使用中に、腎障害または肝障害、心不全、脱水、または循環血液量減少の患者の腎機能を監視する [参照 薬物相互作用 ]。腎機能が悪化するリスクを上回ると期待される場合を除き、腎疾患が進行した患者には NAPRELAN 500mg を使用しないでください。進行した腎疾患の患者にナプレランを使用する場合は、腎機能の悪化の徴候がないか患者を監視してください。
高カリウム血症
高カリウム血症を含む血清カリウム濃度の上昇は、腎機能障害のない一部の患者でさえ、NSAID の使用で報告されています。腎機能が正常な患者では、これらの影響は低レニン血症-低アルドステロン症状態に起因するとされています。
アナフィラキシー反応
ナプロキセンは、ナプロキセンに対する既知の過敏症のある患者とない患者、およびアスピリン感受性喘息患者のアナフィラキシー反応と関連しています。 禁忌 と 警告と注意事項 ]。
アナフィラキシー反応が発生した場合は、緊急の助けを求めてください。
アスピリン感受性に関連する喘息の増悪
喘息患者の亜集団は、鼻ポリープを合併した慢性副鼻腔炎を含む可能性があるアスピリン感受性喘息を有する可能性があります。重度の致命的な気管支痙攣;および/またはアスピリンやその他の NSAID に対する不耐性。このようなアスピリン感受性患者では、アスピリンと他の NSAID との交差反応性が報告されているため、NAPRELAN 250mg は、この形態のアスピリン感受性を持つ患者には禁忌です [ 禁忌 ]。既存の喘息患者(アスピリン感受性のない患者)に NAPRELAN を使用する場合は、喘息の徴候と症状の変化について患者を監視してください。
深刻な皮膚反応
ナプロキセンを含む NSAIDs は、剥脱性皮膚炎、スティーブンス・ジョンソン症候群 (SJS)、中毒性表皮壊死症 (TEN) などの重篤な皮膚有害反応を引き起こし、致命的になる可能性があります。これらの重大なイベントは、予告なしに発生する可能性があります。深刻な皮膚反応の徴候と症状について患者に知らせ、皮膚発疹または過敏症の他の兆候が最初に現れた場合は、ナプレラン 500mg の使用を中止してください。
NAPRELAN は、以前に NSAIDs に対して重篤な皮膚反応を示した患者には禁忌です [参照 禁忌 ]。
好酸球増加症および全身症状を伴う薬物反応 (DRESS)
NAPRELAN などの NSAID を服用している患者では、好酸球増加症および全身症状 (DRESS) を伴う薬物反応が報告されています。これらのイベントのいくつかは、致命的または生命を脅かすものです。 DRESS は通常、発熱、発疹、リンパ節腫脹、および/または顔面の腫れを示しますが、これに限定されません。他の臨床症状には、肝炎、腎炎、血液学的異常、心筋炎、または筋炎が含まれる場合があります。 DRESS の症状は、急性のウイルス感染に似ている場合があります。好酸球増加症がしばしば存在します。この障害は症状がさまざまであるため、ここに記載されていない他の臓器系が関与している可能性があります。発疹が明らかでない場合でも、発熱やリンパ節腫脹などの過敏症の初期症状が存在する可能性があることに注意することが重要です。そのような徴候または症状が存在する場合は、NAPRELAN を中止し、直ちに患者を評価してください。
胎児毒性
胎児動脈管の早期閉鎖
妊娠約 30 週以降の妊婦には、NAPRELAN を含む NSAID の使用を避けてください。 NAPRELAN を含む NSAID は、ほぼこの妊娠期間で胎児の動脈管の早期閉鎖のリスクを高めます。
羊水過少症/新生児腎障害
ナプレラン 500mg を含む NSAIDs を妊娠約 20 週以降に使用すると、羊水過少症や、場合によっては新生児の腎障害につながる胎児の腎機能障害を引き起こす可能性があります。これらの有害な転帰は、平均して数日から数週間の治療後に見られますが、NSAID開始後48時間で羊水過少症が報告されることはめったにありません.羊水過少症は、常にではありませんが、多くの場合、治療を中止すれば元に戻ります。長期にわたる羊水過少症の合併症には、例えば、四肢拘縮および肺成熟の遅延が含まれる場合があります。市販後の新生児腎機能障害の一部の症例では、交換輸血や透析などの侵襲的処置が必要でした。
妊娠 20 週から 30 週の間に NSAID 治療が必要な場合は、NAPRELAN 500mg の使用を可能な限り最小の有効用量と最短の期間に制限してください。 NAPRELAN 治療が 48 時間を超える場合は、羊水の超音波モニタリングを検討してください。羊水過少症が発生した場合はNAPRELANを中止し、臨床診療に従ってフォローアップする[参照 特定の集団での使用 ]。
血液毒性
NSAID治療を受けた患者に貧血が発生しました。これは、潜在的または総失血、体液貯留、または不完全に記述された赤血球生成への影響が原因である可能性があります。 NAPRELAN 500mg で治療された患者に貧血の徴候または症状がある場合は、ヘモグロビンまたはヘマトクリットを監視してください。
NAPRELAN を含む NSAID は、出血イベントのリスクを高める可能性があります。凝固障害、ワルファリンの併用、他の抗凝固薬、抗血小板薬(アスピリンなど)、セロトニン再取り込み阻害薬(SSRI)、セロトニン・ノルエピネフリン再取り込み阻害薬(SNRI)などの併存疾患は、このリスクを高める可能性があります。これらの患者の出血の徴候を監視します [参照 薬物相互作用 ]。
炎症と発熱のマスキング
ナプレラン 250mg の炎症および場合によっては発熱を軽減する薬理学的活性は、感染を検出する際の診断的徴候の有用性を低下させる可能性があります。
ラボモニタリング
深刻な消化管出血、肝毒性、および腎障害は、警告の症状や徴候なしに発生する可能性があるため、長期の NSAID 治療を受けている患者を定期的に CBC および化学的プロファイルでモニタリングすることを検討してください。 警告と注意事項 ]。
患者相談情報
患者に、FDA 承認の患者ラベル ( 投薬ガイド ) 調剤される各処方箋に添付されます。 NAPRELAN 500mg による治療を開始する前に、また治療中は定期的に、患者、家族、またはその介護者に次の情報を知らせてください。
心血管血栓性イベント
胸痛、息切れ、脱力感、ろれつが回らないなどの心血管血栓性イベントの症状に注意し、これらの症状があればすぐに医療提供者に報告するように患者に助言する[参照 警告と注意事項 ]。
消化管出血、潰瘍、および穿孔
NAPRELAN 500mg は、他の NSAID と同様に、消化管の不快感を引き起こす可能性があり、まれに、潰瘍や出血などの重篤な消化管副作用を引き起こし、入院や死に至ることさえあります。心窩部痛、消化不良、下血、吐血などの潰瘍や出血の症状を医療提供者に報告するよう患者に助言します。心臓予防のために低用量アスピリンを併用する状況では、患者に消化管出血のリスクの増加とその徴候と症状を知らせる[参照 警告と注意事項 ]。
肝毒性
肝毒性の兆候と症状(吐き気、疲労、無気力、かゆみ、下痢、黄疸、右上腹部圧痛、「インフルエンザ様」症状など)について患者に知らせる。これらが発生した場合は、NAPRELAN を中止し、直ちに医学的治療を受けるように患者に指示する [参照 警告と注意事項 ]。
心不全と浮腫
息切れ、原因不明の体重増加、または浮腫などのうっ血性心不全の症状に注意し、そのような症状が発生した場合は医療提供者に連絡するよう患者に助言する[参照 警告と注意事項 ]。
アナフィラキシー反応
アナフィラキシー反応の徴候(例、呼吸困難、顔や喉の腫れ)を患者に知らせてください。これらが発生した場合は、直ちに緊急の助けを求めるように患者に指示します[参照 禁忌 と 警告と注意事項 ]。
DRESSを含む深刻な皮膚反応
NAPRELAN 500mg は、他の NSAID と同様に、剥脱性皮膚炎、SJS、TEN などの深刻な皮膚の副作用を引き起こし、入院や死に至ることさえあります。何らかの発疹や発熱が生じた場合は、ナプレランの服用を直ちに中止し、できるだけ早く医療提供者に連絡するように患者にアドバイスしてください。 警告と注意事項 ]。
女性の生殖能力
妊娠を希望する生殖能力のある女性には、NAPRELAN 250mg を含む NSAIDs が排卵の可逆的遅延と関連している可能性があることをアドバイスする [ 特定の集団での使用 ]。
胎児毒性
妊婦には、胎児の動脈管が早期に閉鎖するリスクがあるため、妊娠 30 週からナプレラン 500mg やその他の NSAID の使用を避けるように伝えてください。ナプレラン 500mg による治療が妊娠約 20 ~ 30 週の妊婦に必要な場合は、治療が 48 時間以上続く場合は、羊水過少症のモニタリングが必要になる可能性があることを彼女に伝えてください。 警告と注意事項 と 特定の集団での使用 ]。
NSAIDの併用を避ける
NAPRELAN と他の NSAIDs またはサリチル酸塩(例、ジフルニサル、サルサレート)との併用は、胃腸毒性のリスクが高く、有効性がほとんどまたはまったく増加しないため、推奨されないことを患者に知らせてください。 警告と注意事項 と 薬物相互作用 ]。風邪、発熱、または不眠症の治療のための「市販薬」に NSAID が含まれている可能性があることを患者に警告します。
NSAID と低用量アスピリンの使用
医療提供者に相談するまで、ナプレラン 250mg と併用して低用量アスピリンを使用しないように患者に伝えてください。 薬物相互作用 ]。
非臨床毒性学
発がん、突然変異誘発、生殖能力の障害
発がん
8 mg/kg/日、16 mg/kg/日、および 24 mg/kg/日 (推奨される最大値の 0.05、0.1、および 0.16 倍) の用量でナプロキセンの発がん性を評価するために、ラットで 2 年間の研究が行われました。体表面積の比較に基づくヒトの1日量は1,500 mg /日です)。腫瘍形成性の証拠は見つかりませんでした。
突然変異誘発
ナプロシン懸濁液の変異原性を評価する研究は完了していません。
生殖能力の障害
男性または女性の生殖能力に対するナプロキセンの影響を評価する研究は完了していません。
特定の集団での使用
妊娠
リスクの概要
NAPRELAN 500mgを含むNSAIDの使用は、胎児の動脈管の早期閉鎖および胎児の腎機能障害を引き起こし、羊水過少症を引き起こし、場合によっては新生児の腎機能障害を引き起こす可能性があります。これらのリスクがあるため、NAPRELAN 500mg の使用量と期間は妊娠約 20 ~ 30 週に制限し、妊娠約 30 週以降の NAPRELAN 500mg の使用は避けてください ( 臨床上の考慮事項 、 データ )。
胎児動脈管の早期閉鎖
ナプレラン 500mg を含む NSAID を妊娠約 30 週以降に使用すると、胎児の動脈管が早期に閉鎖するリスクが高まります。
羊水過少症/新生児腎障害
妊娠約 20 週以降の妊娠での NSAID の使用は、羊水過少症につながる胎児の腎機能障害の症例と関連しており、場合によっては新生児の腎機能障害と関連しています。
妊娠第 1 期または第 2 期の女性における NSAID 使用の他の潜在的な胚胎児リスクに関する観察研究のデータは決定的ではありません。ラット、ウサギ、マウスでの動物繁殖研究では、ナプロキセンを器官形成期にヒトの最大推奨日用量 1,500 mg/日のそれぞれ 0.13、0.26、0.6 倍の用量で投与した場合、催奇形性や胎児への害の証拠はありませんでした。動物データに基づいて、プロスタグランジンは子宮内膜の血管透過性、胚盤胞着床、および脱落膜化において重要な役割を果たしていることが示されています。動物実験では、ナプロキセンなどのプロスタグランジン合成阻害剤の投与により、着床前および着床後の損失が増加しました。プロスタグランジンは、胎児の腎臓の発達にも重要な役割を果たしていることが示されています。公表された動物研究では、プロスタグランジン合成阻害剤は、臨床的に適切な用量で投与された場合、腎臓の発達を損なうことが報告されています。
示された集団の主要な先天性欠損症および流産の推定背景リスクは不明です。すべての妊娠には、先天性欠損症、喪失、またはその他の有害な転帰の背景リスクがあります。米国の一般集団では、臨床的に認識された妊娠における主要な先天性欠損症および流産の推定背景リスクは、それぞれ 2% ~ 4% および 15% ~ 20% です。
臨床上の考慮事項
胎児/新生児の有害反応
胎児の動脈管の早期閉鎖: 妊娠約 30 週以降の女性への NSAID の使用は避けてください。 データ )。
羊水過少症/新生児の腎機能障害: 妊娠約 20 週以降に NSAID が必要な場合は、使用を最小限の有効用量と可能な限り短い期間に制限してください。 NAPRELAN 500mg の治療が 48 時間以上続く場合は、羊水過少症を超音波で監視することを検討してください。羊水過少症が発生した場合は、ナプレラン 500mg を中止し、臨床診療に従ってフォローアップします ( データ )。
労働または配達
分娩中の NAPRELAN 500mg の効果に関する研究はありません。動物実験では、ナプロキセン ナトリウムを含む NSAIDS はプロスタグランジン合成を阻害し、分娩を遅らせ、難産の発生率を高め、死産の発生率を高めます。
データ
ヒューマンデータ
プロスタグランジン合成の阻害剤を使用して早産を遅らせると、壊死性腸炎、動脈管開存、頭蓋内出血などの新生児合併症のリスクが高まることを示唆する証拠がいくつかあります。分娩を遅らせるために妊娠後期に行われたナプロキセン治療は、早産児の持続性肺高血圧症、腎機能障害、および異常なプロスタグランジン E レベルと関連しています。ヒト胎児心血管系(動脈管の閉鎖)に対するこのクラスの薬物の影響が知られているため、妊娠第三期中の使用は避けるべきです。
胎児動脈管の早期閉鎖
出版された文献によると、妊娠約 30 週以降に NSAID を使用すると、胎児の動脈管が早期に閉鎖する可能性があります。
羊水過少症/新生児腎障害
発表された研究および市販後のレポートでは、妊娠約 20 週以降の母親の NSAID 使用が、羊水過少症、場合によっては新生児の腎障害につながる胎児の腎機能障害に関連していると記載されています。これらの有害な転帰は、平均して数日から数週間の治療後に見られますが、NSAID開始後48時間で羊水過少症が報告されることはめったにありません.すべてではありませんが、多くの場合、羊水の減少は一過性であり、薬物の中止により元に戻りました。母体の NSAID 使用および羊水過少症を伴わない新生児の腎機能障害の限られた数の症例報告があり、そのうちのいくつかは不可逆的でした。新生児腎機能障害の一部の症例では、交換輸血や透析などの侵襲的処置による治療が必要でした。
これらの市販後研究およびレポートの方法論的限界には、対照群の欠如が含まれます。薬物曝露の用量、期間、およびタイミングに関する限られた情報。および他の薬の併用。これらの制限により、母体の NSAID 使用による胎児および新生児の有害転帰のリスクの信頼できる推定値を確立することができなくなります。新生児転帰に関する公表された安全性データは主に早産児に関係しているため、母親の使用を通じてNSAIDに曝露された満期産児に対する特定の報告されたリスクの一般化可能性は不明です.
動物データ
生殖試験は、ラットで 20 mg/kg/日 (体表面積の比較に基づくヒトの最大推奨 1 日用量 1,500 mg/日の 0.13 倍) で、ウサギで 20 mg/kg/日 (ヒトの最大推奨用量の 0.26 倍) で実施されています。 170 mg/kg/日 (体表面積の比較に基づくヒトの最大推奨 1 日用量の 0.6 倍) のマウスで、受胎能の障害または胎児への害の証拠はありません。薬。動物データに基づいて、プロスタグランジンは子宮内膜の血管透過性、胚盤胞着床、および脱落膜化において重要な役割を果たしていることが示されています。動物実験では、ナプロキセン ナトリウムなどのプロスタグランジン合成阻害剤の投与により、着床前および着床後の損失が増加しました。
授乳
リスクの概要
ナプロキセン陰イオンは、授乳中の女性の母乳中に、血漿中に見られる濃度の約 1% の濃度で見出されています。母乳育児の発達上および健康上の利点は、母親のNAPRELANの臨床的必要性、およびNAPRELANまたは基礎となる母体の状態から母乳で育てられた乳児への潜在的な悪影響とともに考慮されるべきです.
生殖能力のある雌と雄
不妊
女性
作用機序に基づいて、NAPRELAN を含むプロスタグランジンを介した NSAID の使用は、一部の女性の可逆的不妊症に関連している卵胞の破裂を遅らせるか、または防止する可能性があります。発表された動物研究は、プロスタグランジン合成阻害剤の投与が、排卵に必要なプロスタグランジン媒介卵胞破裂を妨害する可能性があることを示しています. NSAIDs で治療された女性を対象とした小規模な研究でも、可逆的な排卵遅延が示されています。妊娠困難な女性や不妊症の調査を受けている女性では、NAPRELAN 250mgを含むNSAIDの中止を検討してください。
小児用
小児集団における NAPRELAN 500mg の安全性と有効性は確立されていません。
高齢者の使用
高齢の患者は、若い患者と比較して、NSAID に関連する重篤な心血管、胃腸、および/または腎臓の副作用のリスクが高くなります。高齢患者にとって予想される利益がこれらの潜在的なリスクを上回る場合は、投与範囲の下限から投与を開始し、副作用について患者を監視します[参照 警告と注意事項 ]。
ナプロキセンとその代謝物は腎臓から実質的に排泄されることが知られており、腎機能が低下している患者では、この薬剤に対する副作用のリスクが高くなる可能性があります。高齢の患者は腎機能が低下している可能性が高いため、この患者集団では注意が必要であり、腎機能のモニタリングが役立つ場合があります [参照 臨床薬理学 ]。
過剰摂取
急性 NSAID の過剰摂取に続く症状は通常、無気力、眠気、吐き気、嘔吐、心窩部痛に限定されており、支持療法で一般的に回復可能です。消化管出血が発生しました。高血圧、急性腎不全、呼吸抑制、および昏睡が発生しましたが、まれでした [ 警告と注意事項 ]。
少数の患者が発作を経験しましたが、これらが薬物関連であったかどうかは明らかではありません.どのくらいの用量で生命を脅かすかはわかっていません。
NSAID の過剰摂取後は、対症療法と支持療法で患者を管理します。特定の解毒剤はありません。ナプロキセンのタンパク質結合度が高いため、血液透析によってナプロキセンの血漿濃度が低下することはありません。嘔吐および/または活性炭 (成人で 60 ~ 100 グラム、小児患者では体重 1 kg あたり 1 ~ 2 グラム) および/または摂取後 4 時間以内に見られる症状のある患者または大量の過剰摂取 (推奨用量の 5 ~ 10 倍)。強制利尿、尿のアルカリ化、血液透析、または血液灌流は、タンパク質結合が高いため役に立たない場合があります。
過剰摂取の治療に関する追加情報については、毒物管理センター (1-800-222-1222) にお問い合わせください。
禁忌
ナプレラン 500mg は、次の患者には禁忌です。
-ナプロキセンまたは製剤の成分に対する既知の過敏症(例、アナフィラキシー反応および重篤な皮膚反応)[参照 警告と注意事項 ]
-アスピリンまたは他のNSAIDを服用した後の喘息、蕁麻疹、またはその他のアレルギー型反応の病歴。そのような患者では、NSAIDsに対する重度の、時には致命的なアナフィラキシー反応が報告されています[ 警告と注意事項 ]
冠動脈バイパス移植 (CABG) 手術の状況 [参照 警告と注意事項 ]
臨床薬理学
作用機序
ナプロキセンには、鎮痛、抗炎症、および解熱特性があります。
NAPRELAN の作用機序は、他の NSAID と同様に完全には解明されていませんが、シクロオキシゲナーゼ (COX-1 および COX-2) の阻害が関与しています。
ナプロキセン ナトリウムは、in vitro でのプロスタグランジン合成の強力な阻害剤です。治療中に到達したナプロキセン ナトリウム濃度は、in vivo 効果を生み出しました。プロスタグランジンは求心性神経を敏感にし、動物モデルで痛みを誘発するブラジキニンの作用を増強します。
プロスタグランジンは炎症のメディエーターです。ナプロキセン ナトリウムはプロスタグランジン合成の阻害剤であるため、その作用機序は末梢組織におけるプロスタグランジンの減少によるものと考えられます。
薬力学
健康なボランティアの研究では、ナプロキセン 220 mg を 1 日 1 回、低用量の即放性アスピリン (81 mg) と 10 日間併用投与すると、24 時間での血清トロンボキサン B2 阻害 % で測定されるアスピリンの抗血小板活性との相互作用が示されました。 10 日目の投与後 [98.7% (アスピリン単独) vs 93.1% (ナプロキセンとアスピリン)]。相互作用は、11日目にナプロキセンを中止した後でも観察されましたが(アスピリン投与は継続)、13日目までに正常化しました。同じ研究では、アスピリンの30分前にナプロキセンを投与した場合に相互作用がより大きくなりました[98.7% vs 87.7%]ナプロキセンの 30 分前にアスピリンを投与した場合は最小でした [98.7% 対 95.4%]。
ナプロキセン 220 mg を 1 日 2 回、低用量の即時放出型アスピリンと一緒に投与した後 (アスピリンの 30 分前に最初のナプロキセンを投与)、相互作用は 10 日目の投与の 24 時間後に最小限でした [98.7% 対 95.7%]。しかし、相互作用は11日目にナプロキセンの中止(ウォッシュアウト)後により顕著になり[98.7%対84.3%]、13日目までに完全に正常化することはなかった[98.5%対90.7%]。 [見る 薬物相互作用 ]。
薬物動態
ナプロキセン自体はよく吸収されますが、ナトリウム塩の形はより急速に吸収され、その結果、所定の用量のピーク血漿レベルが高くなります.ナプロラン 500mg 錠の総ナプロキセン ナトリウム投与量の約 30% が即時放出成分として剤形に含まれています。残りのナプロキセン ナトリウムは微粒子としてコーティングされ、徐放性を提供します。経口投与後、ナプロキセンの血漿レベルは投与後 30 分以内に検出され、ピーク血漿レベルは投与後約 5 時間で発生します。即時放出ナプロキセン ナトリウムおよび NAPRELAN 錠剤の両方から観察されたナプロキセンの最終消失半減期は、約 15 時間です。ナプロキセンの定常状態レベルは 3 日で達成され、血中のナプロキセン蓄積の程度はこれと一致しています。
血漿ナプロキセン濃度 被験者 24 人の平均値 (+/-2SD) (定常状態、5 日目)
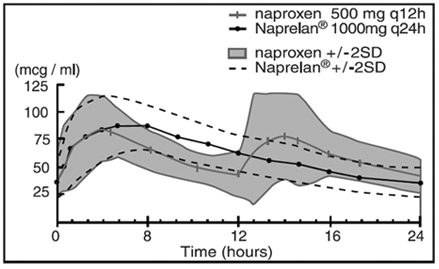
定常状態 5 日目の薬物動態パラメーター (24 人の被験者の平均値)
吸収
ナプロキセン自体は、消化管から迅速かつ完全に吸収され、in vivo でのバイオアベイラビリティは 95% です。薬物動態プロファイルに基づいて、ナプレラン 250mg 錠の吸収段階は、投与後最初の 4 ~ 6 時間で発生します。これは、胃での錠剤の崩壊、徐放性微粒子の小腸を通って近位の大腸への移動と一致します。 in vivo イメージング研究が健康なボランティアで実施され、錠剤マトリックスの急速な崩壊と微粒子の分散が確認されました。
ナプロラン錠の徐放性微粒子成分の吸収速度は、従来のナプロキセンナトリウム錠よりも遅くなります。血漿レベルを維持し、1 日 1 回の投与を可能にするのは、この薬物吸収プロセスの延長です。
食事の影響
24名の被験者にナプレラン500mg錠500mgを一晩絶食後または食後30分に単回投与したところ、有意な食事の影響は認められませんでした。従来のナプロキセンおよびナプロキセン ナトリウム製剤と同様に、ナプロキセン 250mg 錠の投与後、食物はナプロキセンの吸収率をわずかに低下させます。
分布
ナプロキセンの分布量は 0.16 L/kg です。治療レベルでは、ナプロキセンは 99% 以上のアルブミンに結合しています。 500 mg/日を超えるナプロキセンの用量では、より高い用量での血漿タンパク質結合の飽和によって引き起こされるクリアランスの増加により、血漿レベルの増加は比例的ではありません。しかし、結合していないナプロキセンの濃度は、用量に比例して増加し続けています。 NAPRELAN 錠は同様の用量比例特性を示します。
排除
代謝
ナプロキセンは広範囲に代謝されて 6-0-デスメチル ナプロキセンになり、親と代謝物の両方が代謝酵素を誘導しません。
排泄
ナプレラン 500mg 錠と従来のナプロキセンの半減期は約 15 時間です。ナプレラン錠を 2 ~ 3 回服用すると、安定した状態になります。薬物の大部分は、主に未変化のナプロキセン (1% 未満)、6-O-デスメチル ナプロキセン (1% 未満)、およびそれらのグルクロニドまたは他の結合体 (66 ~ 92%) として尿中に排泄されます。少量 (
特定の集団
小児科
NAPRELAN 500mg 錠を使用した小児研究は実施されていないため、小児集団における NAPRELAN 500mg 錠の安全性は確立されていません。
肝障害
慢性アルコール性肝疾患、およびおそらく血漿タンパク質 (アルブミン) の減少または異常を伴うその他の疾患は、ナプロキセンの総血漿濃度を低下させますが、結合していないナプロキセンの血漿濃度は上昇します。高用量が必要な場合は注意が必要であり、これらの患者では用量の調整が必要になる場合があります。最小の有効用量を使用することが賢明です。
腎障害
ナプロキセンの薬物動態は、腎不全の被験者では決定されていません。ナプロキセンが代謝され、コンジュゲートが主に腎臓によって排泄されることを考えると、ナプロキセン代謝産物が腎不全の存在下で蓄積する可能性が存在します。重度の腎障害のある患者では、ナプロキセンの排泄が減少します。ナプロキセン含有製品は、中等度から重度および重度の腎機能障害 (クレアチニンクリアランス 警告と注意事項 ]。
薬物相互作用研究
アスピリン
NSAID をアスピリンと一緒に投与すると、NSAID のタンパク質結合は減少しましたが、遊離 NSAID のクリアランスは変化しませんでした。この相互作用の臨床的意義は不明です。 NSAID とアスピリンとの臨床的に重要な薬物相互作用については、表 1 を参照してください。 薬物相互作用 ]。
臨床研究
関節リウマチ
関節リウマチの兆候と症状を管理するための NAPRELAN 500mg 錠の使用は、348 人の患者を対象とした 12 週間の二重盲検、無作為化、プラセボ、実薬対照試験で評価されました。 1 日 1 回の NAPRELAN 500 mg 錠剤 (1000 mg) 2 錠と 1 日 2 回のナプロキセン 500 mg 錠剤 (1,000 mg) は、プラセボよりも効果的でした。臨床効果は 1 週間で実証され、研究期間中継続されました。
変形性関節症
膝の変形性関節症の徴候と症状の管理のためのナプレラン錠の使用は、347 人の患者を対象とした 12 週間の二重盲検、プラセボ、および実薬対照試験で評価されました。 1 日 1 回の NAPRELAN 500 mg 錠剤 (1,000 mg) 2 錠と 1 日 2 回のナプロキセン 500 mg 錠剤 (1,000 mg) は、プラセボよりも効果的でした。臨床効果は 1 週間で実証され、研究期間中継続されました。
鎮痛
ナプレラン錠の鎮痛効果の発現は、口腔外科手術後の疼痛患者を対象とした薬物動態/薬力学的研究において、30 分以内に認められました。対照臨床試験では、ナプロキセンは金、D-ペニシラミン、メトトレキサート、およびコルチコステロイドと組み合わせて使用されています.アスピリンがナプロキセンの排泄速度を増加させるという証拠があり、ナプロキセンとアスピリンがアスピリン単独で達成されたよりも大きな改善をもたらすことを実証するにはデータが不十分であるため、サリチル酸との併用は推奨されません.さらに、他の NSAIDs と同様に、併用すると、いずれかの製品単独で示されるよりも高い頻度で有害事象が発生する可能性があります。
特別研究
二重盲検無作為並行群間試験では、19 人の被験者がナプロラン 500 mg 錠 (1,000 mg) を 1 日 1 回 2 錠、またはナプロキセン 500 mg 錠 (1,000 mg) を 1 日 2 回、7 日間投与されました。ナプレラン錠を投与された被験者では、粘膜生検のスコアと内視鏡のスコアが低かった。別の二重盲検無作為化クロスオーバー研究では、23 人の被験者がナプロラン 500 mg 錠剤 (1,000 mg) を 1 日 1 回 2 錠、ナプロキセン 500 mg 錠剤 (1,000 mg) を 1 日 2 回、アスピリン 650 mg を 1 日 4 回 (2,600 mg) 7 日間投与されました。各。ナプロキセンまたはアスピリンよりもナプレラン錠で見られた十二指腸びらんが有意に少なかった. NAPRELAN 錠とナプロキセンの両方で、アスピリンよりも胃びらんが有意に少なかった.これらの所見の臨床的意義は不明です。
患者情報
非ステロイド性抗炎症薬(NSAID)の投薬ガイド
非ステロイド性抗炎症薬 (NSAIDs) と呼ばれる薬について知っておくべき最も重要な情報は何ですか?
NSAID は、次のような重大な副作用を引き起こす可能性があります。
- 死に至る可能性のある心臓発作や脳卒中のリスクが高まります。 このリスクは治療の初期に発生する可能性があり、次のように増加する可能性があります。
- NSAIDsの増量に伴い
- NSAIDの長期使用
「冠動脈バイパス移植片 (CABG)」と呼ばれる心臓手術の直前または直後に NSAID を服用しないでください。最近の心臓発作の後に NSAID を服用しないでください。最近の心臓発作の後にNSAIDを服用すると、別の心臓発作のリスクが高くなる可能性があります.
- 食道(口から胃につながる管)、胃、腸の出血、潰瘍、裂傷(穿孔)のリスクの増加:
- 使用中いつでも
- 警告症状なし
- 死に至る可能性があるもの
潰瘍または出血のリスクは、次の場合に増加します。
- 胃潰瘍、またはNSAIDの使用による胃または腸の出血の過去の病歴
- 「コルチコステロイド」、「抗凝固薬」、「SSRI」、または「SNRI」と呼ばれる薬の服用
- NSAIDの増量
- 高齢
- NSAIDの長期使用
- 病弱
- 喫煙
- 進行した肝疾患
- アルコールを飲む
- 出血の問題
NSAID は次の場合にのみ使用してください。
- 規定どおり
- あなたの治療のために可能な限り低い用量で
- 必要最小限の時間で
NSAIDとは何ですか?
NSAID は、さまざまな種類の関節炎、月経痛、およびその他の種類の短期的な痛みなどの病状による痛みや発赤、腫れ、および熱 (炎症) を治療するために使用されます。
NSAIDsを服用してはいけない人は?
NSAID を服用しないでください。
- 喘息発作、蕁麻疹、またはアスピリンやその他の NSAID によるその他のアレルギー反応を起こしたことがある場合。
- 心臓バイパス手術の直前または直後。
NSAIDS を服用する前に、次の場合を含め、すべての病状について医療提供者に伝えてください。
- 肝臓または腎臓に問題がある
- 高血圧がある
- 喘息がある
- 妊娠している、または妊娠する予定がある。妊娠約 20 週以降に NSAID を服用すると、胎児に害を及ぼす可能性があります。妊娠 20 ~ 30 週の間に NSAID を 2 日以上服用する必要がある場合、医療提供者は赤ちゃんの周りの子宮内の液体の量を監視する必要がある場合があります。服用してはいけません 妊娠約30週以降のNSAID。
- 授乳中または授乳を計画している。
処方薬や市販薬、ビタミン、ハーブのサプリメントなど、服用しているすべての薬について医療提供者に伝えてください。 NSAIDs と他のいくつかの薬は相互に作用し、深刻な副作用を引き起こす可能性があります。 最初に医療提供者に相談せずに、新しい薬の服用を開始しないでください。
NSAIDsの考えられる副作用は何ですか?
NSAID は、次のような重大な副作用を引き起こす可能性があります。
「非ステロイド性抗炎症薬(NSAID)と呼ばれる薬について知っておくべき最も重要な情報は何ですか?」を参照してください。
- 新しいまたは悪化した高血圧
- 心不全
- 肝不全を含む肝臓の問題
- 腎不全を含む腎臓の問題
- 低赤血球(貧血)
- 生命を脅かす皮膚反応
- 生命を脅かすアレルギー反応
NSAID のその他の副作用には次のようなものがあります。 胃痛、便秘、下痢、ガス、胸やけ、吐き気、嘔吐、めまい。
次のいずれかの症状が現れた場合は、すぐに緊急援助を受けてください。
- 息切れまたは呼吸困難
- ろれつが回らない
- 胸痛
- 顔や喉の腫れ
- 体の一部または側面の脱力
次のいずれかの症状が現れた場合は、NSAID の使用を中止し、すぐに医療提供者に連絡してください。
- 吐き気
- 血を吐く
- いつもより疲れている、または弱っている
- 便に血が混じっている、またはタールのように黒くてねばねばしている
- 下痢
- かゆみ
- 異常な体重増加
- 肌や目が黄色く見える
- 発熱を伴う皮膚発疹または水ぶくれ
- 消化不良または胃痛
- 腕、脚、手、足のむくみ
- 風邪のような症状
NSAID の服用量が多すぎる場合は、すぐに医療提供者に連絡するか、医師の診察を受けてください。
これらは、NSAIDs の考えられるすべての副作用ではありません。詳細については、NSAID について医療提供者または薬剤師にお尋ねください。
副作用に関する医学的アドバイスについては、医師に連絡してください。 1-800-FDA-1088 で副作用を FDA に報告できます。
NSAID に関するその他の情報
- アスピリンは NSAID ですが、心臓発作の可能性を高めることはありません。アスピリンは、脳、胃、腸で出血を引き起こす可能性があります。アスピリンは、胃や腸に潰瘍を引き起こすこともあります。
- 一部の NSAID は、処方箋なしで低用量で販売されています (店頭)。市販の NSAID を 10 日以上使用する前に、医療提供者に相談してください。
NSAID の安全で効果的な使用に関する一般情報
医薬品は、医薬品ガイドに記載されている以外の目的で処方されることがあります。処方されていない状態に NSAID を使用しないでください。他の人があなたと同じ症状を持っていても、NSAID を他の人に与えないでください。それらに害を及ぼす可能性があります。
NSAID についてさらに詳しい情報が必要な場合は、医療提供者に相談してください。医療専門家向けに書かれた NSAID に関する情報については、薬剤師または医療提供者に尋ねることができます。
この医薬品ガイドは、米国食品医薬品局によって承認されています。
