Imdur 40mg, 20mg, 30mg, 60mg Isosorbide 使用法、副作用および投与量。 オンライン薬局の価格。 処方箋不要のジェネリック医薬品。
Imdur 30mg とは何ですか?
Imdur 30mg は、胸痛 (狭心症) の症状を治療するために使用される処方薬です。 Imdur 30mg は、単独で使用することも、他の薬と併用することもできます。
Imdur 20mg は、硝酸塩、狭心症と呼ばれる薬のクラスに属します。
Imdur 60mgが子供に安全で効果的かどうかは不明です.
Imdur の副作用にはどのようなものがありますか?
Imdur の副作用には次のようなものがあります。
- 失神、
- 速い、不規則な、またはドキドキする心拍、
- 発疹、
- かゆみ、
- 顔、舌、喉の腫れ、
- 重度のめまい、および
- 呼吸困難
上記の症状がある場合は、すぐに医療機関を受診してください。
Imdur 30mg の最も一般的な副作用は次のとおりです。
- 頭痛、
- めまい、
- 立ちくらみ、および
- 吐き気
気になる副作用や治らない副作用がある場合は、医師に相談してください。
これらは、Imdur の考えられるすべての副作用ではありません。詳細については、医師または薬剤師にお尋ねください。
副作用に関する医学的アドバイスについては、医師に連絡してください。 1-800-FDA-1088 で副作用を FDA に報告できます。
説明
有機硝酸塩であり、二硝酸イソソルビド(ISDN)の主要な生物活性代謝物である一硝酸イソソルビド(ISMN)は、動脈と静脈の両方に影響を与える血管拡張剤です。
IMDUR® 錠剤は、経口投与用で、30 mg、60 mg、または 120 mg のイソソルビドモノニトレートを徐放性製剤に含んでいます。さらに、各錠剤には次の不活性成分が含まれています: コロイド状二酸化ケイ素、硬化ヒマシ油、ヒプロメロース、ラクトース一水和物、ステアリン酸マグネシウム、微結晶性セルロース、タルク。
ISMN の分子式は C6H9NO6 で、分子量は 191.14 です。 ISMN の化学名は 1,4:3,6-ジアンヒドロ-,D-グルシトール 5-ニトレートです。この化合物は、次の構造式を持っています。
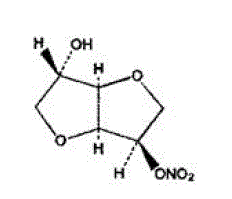
ISMN は白色、結晶性、無臭の化合物で、空気中および溶液中で安定しており、融点は約 90°C、旋光度は +144° (水中 2%、20°C) です。
一硝酸イソソルビドは、水、エタノール、メタノール、クロロホルム、酢酸エチル、およびジクロロメタンに溶けやすいです。
適応症
IMDUR 錠は、冠動脈疾患による狭心症の予防を目的としています。経口イソソルビドモノニトレートの作用の開始は、この製品が急性狭心症エピソードの中止に役立つほど十分に迅速ではありません.
投薬と管理
IMDUR 錠の推奨開始用量は、1 日 1 回 30 mg (30 mg 錠剤 1 錠または 60 mg 錠剤の 1/2 として投与) または 60 mg (1 錠として投与) です。数日後、1日1回120mg(120mg錠1錠または60mg錠2錠)に増量されます。まれに、240 mg が必要になることがあります。 IMDUR 錠の 1 日量は、起床時の朝に服用する必要があります。 IMDUR 徐放性錠剤は、噛んだり、砕いたりしないでください。コップ半分の液体と一緒に飲み込んでください。 30mgの錠剤を割らないでください。
供給方法
IMDUR徐放錠30mg 白いカプセル状の錠剤で、片面に刻み目があり、刻み目のない側に「IMDUR」と刻印されています。それらは次のように提供されます。
100本のボトル NDC 0085-1374-01
IMDUR徐放錠60mg 白いカプセル型の錠剤で、片面に「60-60」のスコアがあり、スコアのない側に「IMDUR」と刻印されています。次のように供給されます。
100本のボトル NDC 0085-2028-01
IMDUR 30mg徐放錠120mg 片面に「IMDUR」、もう片面に「120」と刻印された白いカプセル状の錠剤です。それらは次のように提供されます。
100本のボトル NDC 0085-0091-01
制御された室温 20°-25°C (68°-77°F) [USP を参照] で保管してください。
製造元:Kremers Urban Pharmaceuticals Inc、シーモア、IN47274、USA。改訂: 2010 年 12 月
副作用
以下の表は、実薬治療群の患者が 30 mg、60 mg、120 mg、または 240 mg のイソソルビドを投与された 3 つのプラセボ対照北米研究で、5% を超える被験者で発生した有害事象の頻度を示しています。 IMDUR 60mg 錠として 1 日 1 回一硝酸塩を服用してください。括弧内は、これらの有害事象が治療の中止に関連した頻度を同じ表に示しています。全体として、3 つのプラセボ対照北米研究で 30 mg、60 mg、120 mg、または 240 mg のイソソルビド一硝酸塩を投与された患者の 8% が、有害事象のために治療を中止しました。これらのほとんどは頭痛のために中止されました。めまいがこれらの研究からの離脱と関連することはめったにありませんでした。頭痛は用量に関連する副作用であり、治療を継続すると消失する傾向があるため、IMDUR 治療は低用量で数日間開始してから、望ましいレベルまで増加させることをお勧めします。
頻度と有害事象(廃止) *
さらに、北米で実施された 3 つの試験は、ヨーロッパで実施された 11 の対照試験とプールされました。 14の対照試験のうち、合計711人の患者がIMDUR錠に無作為に割り付けられました。プールされたデータを確認したところ、5%を超える患者から報告された有害事象は頭痛とめまいだけでした。その他の有害事象は、曝露した患者の 5% 以下で報告され、多くの場合、薬物治療との関連性が不明でした。
自律神経系疾患 :口渇、ほてり。
体全体 :無力症、腰痛、胸痛、浮腫、疲労感、発熱、風邪様症状、倦怠感、倦怠感
心血管疾患、一般 :心不全、高血圧、低血圧。
中枢神経系および末梢神経系の障害 :めまい、頭痛、知覚鈍麻、片頭痛、神経炎、麻痺、感覚異常、眼瞼下垂、振戦、めまい
消化器系疾患 :腹痛、便秘、下痢、消化不良、鼓腸、胃潰瘍、胃炎、舌炎、出血性胃潰瘍、痔疾、軟便、下血、吐き気、嘔吐
聴覚および前庭障害 :耳痛、耳鳴り、鼓膜穿孔。
心拍数とリズム障害 :不整脈、心房性不整脈、心房細動、徐脈、脚ブロック、期外収縮、動悸、頻脈、心室頻拍。
肝臓および胆道系の疾患 :SGOT上昇、SGPT上昇。
代謝および栄養障害 :高尿酸血症、低カリウム血症。
筋骨格系疾患 :関節痛、五十肩、筋力低下、筋骨格痛、筋肉痛、筋炎、腱障害、斜頸
筋、内膜、心膜および弁の疾患 :狭心症悪化、心雑音、心音異常、心筋梗塞、Q波異常。
血小板、出血および凝固障害 :紫斑、血小板減少。
精神障害 :不安、集中力低下、錯乱、性欲減退、うつ、インポテンス、不眠症、神経過敏、パロニリア、傾眠
赤血球障害 :低色素性貧血。
生殖障害、女性 :萎縮性膣炎、乳房痛。
抵抗機構障害 :細菌感染症、モニリア症、ウイルス感染症。
呼吸器系疾患 :気管支炎、気管支痙攣、せき、呼吸困難、たん増加、鼻づまり、咽頭炎、肺炎、肺浸潤、ラ音、鼻炎、副鼻腔炎
皮膚および付属器の疾患 :にきび、毛質異常、発汗増加、かゆみ、かぶれ、皮膚結節。
泌尿器系疾患 :多尿、腎結石、尿路感染症。
血管(心臓外)疾患 :紅潮、間欠性跛行、下肢潰瘍、静脈瘤。
視覚障害 :結膜炎、羞明、視力異常。
さらに、一硝酸イソソルビドの販売中に、次の自然発生的な有害事象が報告されています:失神。
薬物相互作用
一硝酸イソソルビドの血管拡張効果は、他の血管拡張剤の効果と相加的である可能性があります。特にアルコールは、この種の相加効果を示すことがわかっています。
カルシウムチャネル遮断薬と有機硝酸塩を併用した場合、顕著な症候性起立性低血圧が報告されています。いずれかのクラスのエージェントの用量調整が必要になる場合があります。
薬物/実験室試験の相互作用
硝酸塩と亜硝酸塩は、Zlatkis-Zak 呈色反応を妨害し、血清コレステロールの測定値が誤って低くなることがあります。
警告
シルデナフィルによる IMDUR の血管拡張効果の増幅は、重度の低血圧を引き起こす可能性があります。この相互作用の時間経過と用量依存性は研究されていません。適切な支持療法は研究されていませんが、これを硝酸塩の過剰摂取、四肢の挙上、および中心部の容積の拡大として扱うのが合理的と思われます.
急性心筋梗塞またはうっ血性心不全の患者における ISMN の利点は確立されていません。イソソルビド一硝酸塩の効果は急速に停止するのが難しいため、この薬はこれらの状況では推奨されません。
これらの状態で一硝酸イソソルビドを使用する場合は、低血圧および頻脈の危険を回避するために、注意深い臨床的または血行動態モニタリングを使用する必要があります。
予防
全般的
特に直立姿勢で重度の低血圧が、少量のイソソルビド一硝酸塩でも発生する可能性があります。したがって、この薬は、ボリュームが枯渇している可能性がある患者、または何らかの理由ですでに低血圧の患者には注意して使用する必要があります.一硝酸イソソルビドによって誘発される低血圧は、逆説的な徐脈および狭心症の増加を伴うことがある。
硝酸塩療法は、肥大型心筋症による狭心症を悪化させる可能性があります。
未知の(おそらく高用量の)有機硝酸塩に長期間曝露した産業労働者では、耐性が明らかに発生します.これらの労働者からの硝酸塩の一時的な離脱中に、胸痛、急性心筋梗塞、さらには突然死さえも発生しており、真の身体依存の存在が実証されています.経口イソソルビド一硝酸塩の日常的な臨床使用に対するこれらの観察の重要性は知られていない.
発がん、突然変異誘発、生殖能力の障害
雄に投与した研究の最初の 6 か月間は最大 900 mg/kg/日、残りの期間は 500 mg/kg/日の用量で一硝酸イソソルビドに曝露したラットでは、発がん性の証拠は観察されませんでした。最長 121 週間、女性は最長 137 週間投与されました。 900 mg/kg/日までの用量で 104 週間まで、餌に含まれる一硝酸イソソルビドに暴露されたマウスでは、発がん性の証拠は観察されませんでした。
一硝酸イソソルビドは、生物学的に適切な濃度で、遺伝子突然変異 (エイムズ試験、マウスリンパ腫試験) または染色体異常 (ヒトリンパ球およびマウス小核試験) を生じませんでした。
交配の 9 週間前から雄と雌のラットに 750 mg/kg/日までの用量を投与し、雌では交配の 2 週間前から受精能への影響は観察されませんでした。
妊娠
催奇形性効果
妊娠カテゴリーB
一硝酸イソソルビドの胚・胎児発生への影響を検出するために計画された研究では、妊娠中のラットおよびウサギに投与された最大 240 または 248 mg/kg/日の用量は、そのような影響の証拠とは関連がありませんでした。これらの動物の用量は、体重に基づいて比較すると、ヒトの最大推奨用量 (50 kg の女性で 120 mg) の約 100 倍です。体表面積で比較すると、ラットの投与量はヒトの投与量の約 17 倍、ウサギの投与量はヒトの投与量の約 38 倍です。しかし、妊娠中の女性を対象とした十分に管理された研究はありません。動物の繁殖研究は常に人間の反応を予測できるわけではないため、IMDUR 錠は明らかに必要な場合にのみ妊娠中に使用する必要があります。
非催奇形効果
妊娠後期および授乳期に、妊娠ラットに一硝酸イソソルビド 750 mg (300 mg ではない) mg/kg/日を経口投与した場合、新生児の生存と発育および死産の発生率に悪影響が及んだ。この用量(比較が体重に基づく場合はヒトの用量の約 312 倍、比較が体表面積に基づく場合はヒトの用量の 54 倍)は、母親の体重増加と運動活動の減少、および授乳障害の証拠と関連していました。
授乳中の母親
この薬が母乳中に排泄されるかどうかは不明です。多くの薬物が母乳中に排泄されるため、授乳中の母親に ISMN を投与する場合は注意が必要です。
小児用
小児患者における ISMN の安全性と有効性は確立されていません。
高齢者の使用
IMDUR 60mg 錠の臨床試験には、65 歳以上の患者に関する十分な情報が含まれておらず、若い患者と異なる反応を示すかどうかを判断することができませんでした。 IMDUR 20mgの他の報告された臨床経験では、高齢患者と若年患者の反応の違いは確認されていません.文献で報告されている有機硝酸塩の臨床経験では、重度の低血圧の可能性と高齢者の硝酸塩に対する感受性の増加が確認されています。一般に、高齢患者の用量選択は慎重に行う必要があり、通常は用量範囲の下限から開始します。これは、肝臓、腎臓、または心機能の低下、および付随する疾患または他の薬物療法の頻度が高いことを反映しています。
高齢患者は圧受容器機能が低下している可能性があり、血管拡張剤を使用すると重度の起立性低血圧を発症する可能性があります。したがって、IMDUR 60mgは、量が不足している可能性がある高齢の患者、複数の薬を服用している、または何らかの理由ですでに低血圧になっている患者には注意して使用する必要があります.一硝酸イソソルビドによって誘発される低血圧は、逆説的な徐脈および狭心症の増加を伴うことがある。
高齢の患者は低血圧になりやすく、治療用量のニトログリセリンで転倒するリスクが高くなる可能性があります。
硝酸塩療法は、特に高齢者において、肥大型心筋症によって引き起こされる狭心症を悪化させる可能性があります。
過剰摂取
血行動態効果
一硝酸イソソルビドの過剰摂取による悪影響は、一般に、一硝酸イソソルビドの血管拡張、静脈貯留、心拍出量の減少、および低血圧を誘発する能力の結果です。これらの血行動態の変化は、持続的なズキズキする頭痛、錯乱、および中等度の発熱のいずれかまたはすべてを伴う、頭蓋内圧の上昇を含む変幻自在の症状を示す可能性があります。めまい、動悸;視覚障害;吐き気と嘔吐(おそらく疝痛や血性下痢を伴う);失神(特に直立姿勢で);空気飢餓と呼吸困難、その後の換気努力の低下。発汗、皮膚が紅潮するか、冷たくてベトベトする。心臓ブロックおよび徐脈;麻痺;昏睡;発作と死。
イソソルビド一硝酸塩とその代謝物の血清レベルの実験室での測定は広く利用可能ではなく、いずれにせよ、そのような測定はイソソルビド一硝酸塩の過剰摂取の管理において確立された役割を持っていません.
イソソルビド一硝酸塩のどの用量がヒトの生命を脅かす可能性があるかを示唆するデータはありません.ラットとマウスでは、それぞれ 2000 mg/kg と 3000 mg/kg の用量で有意な致死率があります。
一硝酸イソソルビドの排泄を促進する可能性のある生理学的操作 (例、尿の pH を変化させる操作) を示唆するデータはありません。特に、透析は体から一硝酸イソソルビドを除去するのに効果がないことが知られています。
一硝酸イソソルビドの血管拡張作用に対する特異的なアンタゴニストは知られておらず、介入もありません 一硝酸イソソルビドの血管拡張作用に対する特異的なアンタゴニストは知られておらず、一硝酸イソソルビドの過剰摂取の治療法として対照研究の対象となった介入はありません。一硝酸イソソルビドの過剰摂取に伴う低血圧は、静脈拡張と動脈血量減少の結果であるため、この状況での慎重な治療は、中心体液量の増加に向けられるべきです。患者の脚を受動的に挙上するだけで十分ですが、通常の生理食塩水または同様の液体の静脈内注入も必要になる場合があります。
この状況でエピネフリンやその他の動脈血管収縮剤を使用すると、効果よりも害が大きくなる可能性があります。
腎疾患またはうっ血性心不全の患者では、中心容積の拡大をもたらす治療に危険がないわけではありません。これらの患者における一硝酸イソソルビドの過剰摂取の治療は微妙で困難な場合があり、侵襲的なモニタリングが必要になる場合があります。
メトヘモグロビン血症
メトヘモグロビン血症は、他の有機硝酸塩を投与されている患者で報告されており、おそらく一硝酸イソソルビドの副作用としても発生する可能性があります.確かに、一硝酸イソソルビドの代謝中に遊離した硝酸イオンは、ヘモグロビンを酸化してメトヘモグロビンにすることができます。しかし、シトクロム b レダクターゼ活性がまったくない患者であっても、一硝酸イソソルビドの硝酸部分がヘモグロビンの酸化に定量的に適用されると仮定しても、これらの患者のいずれかが臨床的に重大な症状を示す前に、約 2 mg/kg の一硝酸イソソルビドが必要になるはずです ( ≥10%) メトヘモグロビン血症。レダクターゼ機能が正常な患者では、メトヘモグロビンの有意な産生には、さらに多量のイソソルビド一硝酸塩が必要です。 36 人の患者が 3.1 ~ 4.4 mg/hr (硝酸イオンの総投与量で、1 時間あたりのイソソルビド一硝酸塩 7.8 ~ 11.1 mg に相当) で 2 ~ 4 週間の継続的なニトログリセリン療法を受けた 1 つの研究では、平均メトヘモグロビンレベル測定値は 0.2% でした。これは、プラセボを投与された並行患者で観察されたものと同等でした。
これらの観察にもかかわらず、有機硝酸塩の中程度の過剰摂取に関連した重大なメトヘモグロビン血症の症例報告があります。影響を受けた患者のいずれも、異常に感受性が高いとは考えられていませんでした。
メトヘモグロビン レベルは、ほとんどの臨床検査室で入手できます。十分な心拍出量と十分な動脈 pO2 にもかかわらず、酸素供給障害の徴候を示す患者では、この診断を疑う必要があります。古典的に、メトヘモグロビン血症の血液は、空気に触れても変色しないチョコレートブラウンと表現されています。メトヘモグロビン血症と診断された場合、選択される治療はメチレンブルー、1~2 mg/kg の静脈内投与です。
禁忌
IMDUR 20mg 錠は、他の硝酸塩または亜硝酸塩に対して過敏症または特異な反応を示した患者には禁忌です。
臨床薬理学
作用機序
IMDUR 製品は、二硝酸イソソルビドの主要な活性代謝物である ISMN の経口持続放出製剤です。二硝酸塩の臨床活性の大部分は、一硝酸塩に起因します。
ISMN およびすべての有機硝酸塩の主な薬理学的作用は、一般に血管平滑筋の弛緩であり、末梢動脈および静脈、特に後者の拡張を引き起こします。静脈の拡張は、血液の末梢貯留を促進し、心臓への静脈還流を減少させ、それによって左心室拡張終期圧および肺毛細血管楔入圧 (前負荷) を低下させます。細動脈の弛緩は、全身の血管抵抗、収縮期動脈圧、および平均動脈圧 (後負荷) を低下させます。冠動脈の拡張も起こります。前負荷軽減、後負荷軽減、および冠動脈拡張の相対的な重要性は未定義のままです。
薬力学
ほとんどの慢性的に使用される薬物の投与計画は、最小有効濃度より継続的に高い血漿濃度を提供するように設計されています。この戦略は、有機硝酸塩には不適切です。よく管理されたいくつかの臨床試験では、運動試験を使用して、継続的に供給される硝酸塩の抗狭心症の有効性が評価されています。これらの試験の大部分では、24 時間 (またはそれ以下) の連続治療後には、有効成分はプラセボと区別できませんでした。急性に使用される用量をはるかに超える用量であっても、用量漸増によって耐性を克服しようとする試みは一貫して失敗しています.硝酸塩が体内に数時間存在しない場合にのみ、その抗狭心症効果が回復します。 IMDUR 錠は、1 日 1 回 120 mg を 42 日間にわたって長期使用した場合、服用後 4 時間および 12 時間の時点で運動パフォーマンスを改善し続けましたが、その効果は (プラセボよりは優れていますが) 同等以下でした。 60mgの初回投与の効果。
薬物動態と代謝
溶液または即時放出錠剤としての ISMN の経口投与後、ISMN の最大血漿濃度は、約 100% の絶対バイオアベイラビリティで 30 ~ 60 分で達成されます。静脈内投与後、約 9 分で約 0.6 ~ 0.7 L/kg の分配量で、ISMN が全身の水分に分配されます。一硝酸イソソルビドは、ヒト血漿タンパク質に約 5% 結合し、血液細胞と唾液に分配されます。一硝酸イソソルビドは主に肝臓で代謝されますが、経口の二硝酸イソソルビドとは異なり、初回通過代謝を受けません。一硝酸イソソルビドは、イソソルビドへの脱硝および一硝酸塩としてのグルクロン酸抱合により除去され、投与量の 96% が 5 日以内に尿中に排泄され、わずか約 1% が糞便中に排泄されます。少なくとも 6 つの異なる化合物が尿中に検出され、投与量の約 2% が未変化の薬物と少なくとも 5 つの代謝物として排泄されました。代謝産物は薬理学的に活性ではありません。腎クリアランスは、体全体のクリアランスの約 4% しか占めていません。 ISMN の平均血漿消失半減期は約 5 時間です。
さまざまな程度の腎不全、肝硬変、または心機能障害の患者における ISMN の性質が評価され、健康な被験者で観察されるものと同様であることがわかりました。 ISMN の消失半減期は延長されず、複数回の経口投与後の慢性腎不全患者における薬物蓄積はありませんでした。
IMDUR 40mg 錠剤の薬物動態および/またはバイオアベイラビリティは、単回および複数回投与後の正常なボランティアと患者の両方で研究されています。これらの研究のデータは、IMDUR 錠として投与された ISMN の薬物動態が、正常な健康なボランティアと狭心症患者の間で類似していることを示唆しています。単回投与および複数回投与の研究では、ISMN の薬物動態は 30 mg から 240 mg の間で用量に比例していました。
反復投与試験では、IMDUR 60 mg および 120 mg (2 × 60 mg) の薬物動態プロファイルに対する年齢の影響が、45 歳以上の被験者で評価されました。その研究の結果は、IMDUR 60 mg の用量について、高齢者 (65 歳以上) と若年者 (45 ~ 64 歳) の間で ISMN の薬物動態変数のいずれにも有意差がないことを示しています。 IMDUR 錠 120 mg (60 mg 錠 2 錠を 24 時間ごとに 7 日間) を投与すると、Cmax と AUC が用量に比例して増加しましたが、Tmax または終末半減期は変化しませんでした。年配のグループ (65 ~ 74 歳) は、若いグループ (45 ~ 64 歳) と比較して、高用量 (120 mg) の後に見かけの経口クリアランス (Cl/F) が 30% 低いことを示しました。 Cl/F は、60 mg レジメン後の 2 つのグループ間で差はありませんでした。若いグループの Cl/F は用量とは無関係でしたが、年長のグループは、60 mg レジメンと比較して、120 mg レジメンの後にわずかに低い Cl/F を示しました。ただし、2 つの年齢グループ間の違いは、統計的に有意ではありませんでした。同じ研究で、雌は投与量を増やすとクリアランスがわずかに (15%) 減少したことが示されました。女性は男性と比較してより高い AUC と Cmax を示しましたが、これらの違いは 2 つのグループ間の体重の違いによって説明されました。変数として年齢を使用してデータを分析した場合、結果は、高齢者 (65 歳以上) と若年者 (45 ~ 64 歳) の間で ISMN の薬物動態変数のいずれにも有意差がないことを示しました。ただし、この研究の結果は、各年齢サブグループの被験者数が少なく、その結果、十分な統計的検出力が不足しているため、注意して表示する必要があります.
次の表は、経口液剤または IMDUR 錠として ISMN を単回および複数回投与した後の ISMN の主要な薬物動態パラメーターをまとめたものです。
食事の影響
IMDUR 錠 60 mg の単回投与後の ISMN のバイオアベイラビリティに対する食物の影響は、「軽い」朝食または高カロリー、高脂肪の朝食を含む 3 つの異なる研究で評価されました。これらの研究の結果は、付随する食物摂取が ISMN の吸収の速度 (Tmax の増加) を減少させる可能性があるが、吸収の程度 (AUC) を減少させない可能性があることを示しています。
臨床試験
IMDUR 錠を使用した対照試験では、急性および慢性投与後の抗狭心症活性が実証されています。 IMDUR 40mg 錠剤を 1 日 1 回投与し、起床時の早朝に服用すると、少なくとも 12 時間の抗狭心症活性が得られました。
プラセボ対照の並行試験では、30、60、120、および 240 mg の IMDUR 60 mg 錠を 1 日 1 回、最大 6 週間投与しました。無作為化の前に、すべての患者は 1 ~ 3 週間の単盲検プラセボ フェーズを完了し、硝酸塩の反応性と総運動トレッドミル時間の再現性を示しました。二重盲検期間の 1、7、14、28、および 42 日目の朝の投与の前、および投与の 4 時間後および 12 時間後に、Bruce Protocol を使用した運動負荷試験を実施しました。 IMDUR 60mg 錠剤 30 および 60mg (緊急に評価された用量のみ) は、最初の投与の投与後 4 時間および 12 時間で、プラセボと比較して総トレッドミル時間のベースラインからの有意な増加を示しました。 42 日目に、IMDUR 40mg 錠剤の 120 および 240 mg 用量は、投与後 4 時間および 12 時間で合計トレッドミル時間の有意な増加を示しましたが、42 日目までに、30 および 60 mg 用量はもはやプラセボと区別できなくなりました。長期投与を通じて、どの IMDUR 治療群でもリバウンドは観察されませんでした。
IMDUR 40mg 錠 60mg 1 日 1 回、ISDN 30mg QID、プラセボ QID を慢性安定狭心症患者に無作為化、二重盲検、3 ウェイ クロスオーバー デザインを使用して比較した他の 2 つの試験からのデータを統合したところ、統計的に有意な運動耐容能の増加が見られました4、8、12 時間目に IMDUR 20mg 錠をプラセボと比較し、4 時間目に ISDN を比較した。 .
患者情報
IMDUR 60mg 錠の抗狭心症効果は、処方された投与スケジュールを注意深く守ることによって維持できることを患者に説明する必要があります。ほとんどの患者にとって、これは起床時に服用することで達成できます。
他の硝酸塩と同様に、毎日の頭痛は、一硝酸イソソルビドによる治療を伴うことがあります.これらの頭痛を患っている患者では、頭痛は薬の活動のマーカーです.患者は、一硝酸イソソルビドによる治療スケジュールを変更して、頭痛を回避したいという誘惑に抵抗する必要があります。なぜなら、頭痛がなくなると抗狭心症の効果が同時に失われる可能性があるからです。アスピリンまたはアセトアミノフェンは、多くの場合、一硝酸イソソルビドの抗狭心症効果に悪影響を与えることなく、一硝酸イソソルビド誘発性の頭痛をうまく緩和します。
イソソルビドモノニトレートによる治療は、立っているとき、特に横になっているまたは座っている位置から立ち上がった直後に、立ちくらみと関連している可能性があります.この影響は、アルコールも摂取した患者でより頻繁に発生する可能性があります。
