Acyclovir cream 5% 10g, 5g 使用法、副作用および投与量。 オンライン薬局の価格。 処方箋不要のジェネリック医薬品。
ゾビラックス クリームとは?
Zovirax Cream は、口唇ヘルペス (口唇ヘルペス) および性器ヘルペスの症状を治療するために使用される処方薬です。ゾビラックス クリームは、単独で使用することも、他の薬と併用することもできます。
ゾビラックス クリームは、抗ウイルス薬と呼ばれる種類の薬です。
Zovirax Cream が 12 歳未満の子供に安全で効果的であるかどうかはわかっていません。
ゾビラックス クリームの副作用の可能性は?
Zovirax クリームは、次のような重大な副作用を引き起こす可能性があります。
- あざや出血しやすい、
- 皮膚の下の紫または赤のピンポイントスポット、
- 排尿がほとんどまたはまったくない、
- 痛みや排尿困難、
- 足や足首のむくみ、
- 疲労感と
- 呼吸困難
上記の症状がある場合は、すぐに医療機関を受診してください。
ゾビラックス クリームの最も一般的な副作用は次のとおりです。
- 吐き気、
- 嘔吐、
- 下痢、
- 一般的な不快感、
- 頭痛と
- アシクロビル口腔錠使用中の口の痛み
気になる副作用や治らない副作用がある場合は、医師に相談してください。
これらは、ゾビラックス クリームの考えられるすべての副作用ではありません。詳細については、医師または薬剤師にお尋ねください。
副作用に関する医学的アドバイスについては、医師に連絡してください。 1-800-FDA-1088 で副作用を FDA に報告できます。
説明
ZOVIRAX は、ヘルペス ウイルスに対して有効な合成ヌクレオシド類似体であるアシクロビルの商品名です。ゾビラックス クリーム 5% は、局所投与用の製剤です。
アシクロビルの化学名は、2-アミノ-1,9-ジヒドロ-9-[(2-ヒドロキシエトキシ)メチル]-6H-プリン-6-オンです。次の構造式があります。
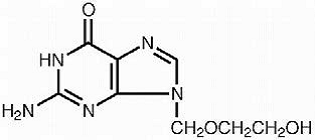
アシクロビルは、分子式が C8H11N5O3 で分子量が 225 の白色の結晶性粉末です。37°C での水への最大溶解度は 2.5 mg/mL です。アシクロビルの pKa は 2.27 と 9.25 です。
ゾビラックス クリーム 5% の各グラムには、50 mg のアシクロビルと次の不活性成分が含まれています: セトステアリル アルコール、ミネラル オイル、ポロキサマー 407、プロピレン グリコール、ラウリル硫酸ナトリウム、水、白色ワセリン。
適応症
ゾビラックス クリームは、免疫力のある成人および 12 歳以上の青少年における再発性口唇ヘルペス (口唇ヘルペス) の治療に適応される、単純ヘルペス ウイルス (HSV) デオキシヌクレオシド アナログ DNA ポリメラーゼ阻害剤です。
投薬と管理
ゾビラックス クリームは、1 日 5 回、4 日間塗布する必要があります。治療は、口唇ヘルペスの徴候または症状の発症後できるだけ早く、すなわち前駆期または病変が現れたときに開始する必要があります。
12歳以上の青少年の場合、投与量は成人と同じです。
供給方法
剤形と強度
ゾビラックス クリームの各グラムには、50 mg (5% w/w に相当) のアシクロビルが含まれています。
保管と取り扱い
ゾビラックス クリームの各グラムには、水性クリーム ベースに 50 mg (5% w/w に相当) のアシクロビルが含まれています。 ZOVIRAX クリームは次のように供給されます。
NDC 0187-0994-45:5gチューブ
25°C (77°F) 以下で保管してください。 15° ~ 30°C (59° ~ 86°F) [USP 制御室温を参照してください] まで許容されます。
販売元: Bausch Health US, LLC Bridgewater, NJ 08807 USA.製造元: Bausch Health Companies Inc. Laval, Quebec H7L 4A8, Canada.改訂: 2020 年 12 月
副作用
臨床試験の経験
臨床試験はさまざまな条件下で実施されるため、ある医薬品の臨床試験で観察された副作用率を別の医薬品の臨床試験で観察された率と直接比較することはできず、臨床現場で観察された率を反映していない可能性があります。
つの二重盲検プラセボ対照試験で、1,124 人の患者がゾビラックス クリームで治療され、1,161 人がプラセボ (ビヒクル) クリームで治療されました。局所適用部位反応は、ZOVIRAX Cream を投与された患者の 5%、プラセボを投与された患者の 4% で報告されました。局所適用部位での最も一般的な副作用は、唇の乾燥、落屑、皮膚の乾燥、唇のひび割れ、皮膚の灼熱感、かゆみ、皮膚の薄片化、および皮膚の刺痛でした。それぞれの副作用は、ZOVIRAX クリームとプラセボを投与された患者の 1% 未満で発生しました。ゾビラックス クリームを服用している 3 人の患者とプラセボを服用している 1 人の患者は、有害事象のために治療を中止しました。
22 名の健康な成人を登録した追加の研究を実施し、ゾビラックス クリームの皮膚への耐性を、単一閉塞および半閉塞パッチ テスト法を使用してビヒクルと比較して評価しました。ゾビラックス クリームとプラセボの両方が、高い累積的な刺激の可能性を示しました。 251 人の健康な成人を登録した別の研究では、反復刺激パッチテスト法を使用して、ゾビラックス クリームの接触感作の可能性を評価しました。評価可能な202人の被験者のうち、ゾビラックスクリームとプラセボの両方で同じ4人(2%)の被験者に皮膚感作反応の可能性が観察され、ゾビラックスクリームとプラセボの両方に対するこれらの反応は、再投与時に3人の被験者で確認されました.感作成分は特定されていません。
12 歳から 17 歳の患者の安全性プロファイルは、成人で観察されたものと同様でした。
市販後の経験
臨床試験から報告された有害事象に加えて、アシクロビル クリームの承認後の使用中に次の事象が確認されました。それらは未知のサイズの母集団から自発的に報告されるため、頻度の推定はできません。これらの事象は、その深刻さ、報告の頻度、またはアシクロビル クリームとの潜在的な因果関係の組み合わせにより、含めるために選択されました。
全般的: 血管性浮腫、アナフィラキシー。
肌: 接触皮膚炎、湿疹。
薬物相互作用
臨床経験では、ゾビラックス クリームと併用した他の薬剤の局所または全身投与による相互作用は確認されていません。ゾビラックス クリームの全身への吸収は最小限であるため、全身の薬物相互作用は起こりそうにありません。
警告
の一部として含まれています 予防 セクション。
予防
全般的
ゾビラックス クリームは、口唇ヘルペス患者の唇と顔の影響を受けた外側にのみ塗布してください。データがないため、ヒトの粘膜への適用は推奨されません。ゾビラックス クリームは皮膚への使用のみを目的としており、目や口、鼻には使用しないでください。
接触感作
ゾビラックス クリームには、刺激および接触感作の可能性があります [参照 有害反応 ]。
ゾビラックス クリームの効果は、免疫不全患者では確立されていません。
患者相談情報
患者に、FDA 承認の患者ラベル ( 患者情報 )。
全般的
ゾビラックス クリームは、顔面や唇に発生する口唇ヘルペス (再発性口唇ヘルペス) の治療のための処方外用クリームであることを患者に知らせる必要があります。ゾビラックス クリームは口唇ヘルペスの治療法ではありません。ゾビラックス クリームは、口唇ヘルペスおよび口の周りの皮膚への使用のみを意図していることを患者に説明する必要があります。ゾビラックス クリームを目、口、鼻、性器に使用しないでください。ゾビラックス クリームを使用している間は、患部に他の局所用製品を塗布しないように患者に指示する必要があります。
ゾビラックス クリームまたはゾビラックス クリームの成分にアレルギーのある方は使用しないでください。ゾビラックス クリームを使用する前に、妊娠中、妊娠を計画している場合、または授乳中の場合は医師に相談してください。
使用説明書
治療は、再発の徴候または症状が最も早い段階で開始する必要があります。塗布前に手を洗い、顔や唇が清潔で乾いていることを確認するように患者に指示してください。ゾビラックス クリームを 1 日 5 回、4 日間局所的に塗布するよう患者にアドバイスします。外縁を含む患部を覆うのに十分な量のゾビラックス クリームを局所的に塗布するよう患者に指示します。感染症の悪化や転移を避けるために、患部を不必要にこすらないように患者にアドバイスしてください。ゾビラックス クリームを使用した後は、石鹸と水で手を洗うように患者に指示してください。小児の手の届かない場所に保管。
考えられる副作用
ゾビラックス クリームを塗布したときに発生した一般的な皮膚関連の副作用には、塗布部位の反応が含まれます。ゾビラックス クリームは、刺激や接触感作の可能性があります。
非臨床毒性学
発がん、突然変異誘発、生殖能力の障害
アシクロビルの局所投与後の全身暴露は最小限です。皮膚発がん性試験は実施されていません。皮膚への塗布によるアシクロビルの曝露は最小限であるため、発がん、突然変異誘発、生殖能力に関する研究の結果は、ゾビラックス クリームの完全な処方情報には含まれていません。これらの研究に関する情報は、ゾビラックス カプセル、錠剤、懸濁液および注射用ゾビラックスの完全な処方情報で入手できます。
特定の集団での使用
妊娠
リスクの概要
アシクロビルは、局所投与経路に従って全身に吸収されることは最小限であり、母体の使用がゾビラックス クリームへの胎児の曝露をもたらすとは予想されない [参照 臨床薬理学 ]。観察研究を含む公表された文献に基づく、数十年にわたる妊婦へのアシクロビルの局所使用の経験では、主要な先天性欠損症、流産、または母体または胎児の有害転帰の薬物関連リスクは確認されていません。アシクロビルの全身暴露による動物繁殖試験が実施されています。詳細については、アシクロビルの処方情報を参照してください。
示された集団の主要な先天性欠損症および流産の推定背景リスクは不明です。すべての妊娠には、先天性欠損症、喪失、またはその他の有害な転帰の背景リスクがあります。米国の一般集団では、臨床的に認識された妊娠における主要な先天性欠損症および流産の推定背景リスクは、それぞれ 2% ~ 4% および 15% ~ 20% です。
授乳
リスクの概要
アシクロビルは、局所投与経路に従って全身に吸収されることは最小限であり、授乳によって子供がゾビラックス クリームにさらされることはないと予想されます。 臨床薬理学 ]。母乳で育てられた乳児または乳生産に対するゾビラックスの効果に関するデータはありません。母乳育児の発達上および健康上の利点は、ゾビラックス クリームに対する母親の臨床的必要性、およびゾビラックス クリームまたは母体の基礎疾患による母乳育児中の子供への潜在的な悪影響と併せて考慮する必要があります。
小児用
口唇ヘルペスを再発した 12 歳から 17 歳の患者 113 人を対象に、ZOVIRAX クリームを使用した非盲検非対照試験が実施されました。この試験では、成人と同じ投与計画を使用して治療が適用され、被験者の有害事象が追跡されました。安全性プロファイルは、成人で観察されたものと同様でした。 12 歳未満の小児患者における安全性と有効性は確立されていません。
高齢者の使用
アシクロビル クリームの臨床研究には、65 歳以上の対象者が若い対象者と異なる反応を示すかどうかを判断するのに十分な数の対象者が含まれていませんでした。他の報告された臨床経験では、年配の患者と若い患者の間の反応の違いは確認されていません。局所投与後のアシクロビルの全身吸収は最小限である[参照 臨床薬理学 ]。
過剰摂取
全身への曝露が最小限であるため、ZOVIRAX Cream の局所適用による過剰投与は考えにくい [参照 臨床薬理学 ]。過剰摂取に関する情報はありません。
禁忌
ゾビラックス クリームは、アシクロビル、バラシクロビル、または製剤の成分に対する既知の過敏症のある患者には禁忌です。
臨床薬理学
作用機序
アシクロビルは、α-ヘルペスウイルスに対して有効な抗ウイルス薬です [参照 微生物学 ]。
薬物動態
アシクロビルの経皮吸収を評価するために、成人ボランティアを対象にゾビラックス クリームを使用した臨床薬理試験が実施されました。 6 人の男性ボランティアを含むこの研究では、クリームをボランティアの背中の 710 cm² の領域に 1 日 5 回、2 時間間隔で合計 4 日間塗布しました。塗布したクリームの重量とアシクロビルの尿中排泄量を毎日測定しました。アシクロビルの血漿濃度は、最終適用の1時間後に分析した。アシクロビルの 1 日平均尿中排泄は、1 日適用用量の約 0.04% でした。血漿アシクロビル濃度は、5人の被験者で検出限界(0.01μM)未満であり、1人の被験者でかろうじて検出可能(0.014μM)でした。ゾビラックス クリームからのアシクロビルの全身吸収は、成人では最小限です。
クリームの局所塗布後のアシクロビルの全身吸収は、18 歳未満の患者では評価されていません。
微生物学
作用機序
アシクロビルは、細胞培養および HSV タイプ 1 (HSV-1) および 2 (HSV-2) DNA ポリメラーゼに対する in vivo 阻害活性を持つ合成プリン デオキシヌクレオシド アナログです。細胞培養およびin vivoでHSV-1およびHSV-2の複製を阻害します。
アシクロビルの阻害活性は、HSV によってコードされる酵素チミジンキナーゼ (TK) に対する親和性により選択的です。このウイルス酵素は、アシクロビルをデオキシヌクレオチド類似体であるアシクロビル一リン酸に変換します。一リン酸はさらに、細胞のグアニル酸キナーゼによって二リン酸に変換され、多くの細胞酵素によって三リン酸に変換されます。生化学的アッセイでは、アシクロビル三リン酸はα-ヘルペスウイルスDNAの複製を阻害します。この阻害は 3 つの方法で達成されます: 1) ウイルス DNA ポリメラーゼの競合的阻害、2) 成長中のウイルス DNA 鎖への取り込みと終結、および 3) ウイルス DNA ポリメラーゼの不活性化。
抗ウイルス活性
細胞培養中の抗ウイルス剤に対するヘルペスウイルスの感受性と治療に対する臨床反応との間の定量的関係は、ヒトでは確立されておらず、ウイルス感受性試験は標準化されていません。細胞培養中のウイルスの増殖を 50% 阻害するのに必要な薬剤の濃度 (EC50 値) として表される感度試験の結果は、多くの要因によって大きく異なります。 Vero 細胞でのプラーク減少アッセイを使用すると、単純ヘルペス ウイルス分離株に対するアシクロビルの EC50 値は、HSV-1 では 0.09 から 59.9 μM (0.02 から 13.5 μg/mL)、HSV-1 では 0.04 から 44.0 μM (0.01 から 9.9 μg/mL) の範囲です。 ) HSV-2 の場合。
抵抗
細胞培養において
アシクロビル耐性 HSV-1 および HSV-2 株は、細胞培養で分離されました。アシクロビル耐性 HSV は、ウイルス チミジン キナーゼ (TK; pUL23) および DNA ポリメラーゼ (POL; pUL30) 遺伝子の変異に起因します。フレームシフトは一般に分離され、HSV TK 産物の時期尚早の切断をもたらし、その結果、アシクロビルに対する感受性が低下します。ウイルスの TK 遺伝子の突然変異は、TK 活性の完全な喪失 (TK 陰性)、TK 活性のレベルの低下 (TK 部分的)、またはチミジンリン酸化能力の同等の喪失なしに薬物をリン酸化するウイルス TK の能力の変化 (TKaltered) につながる可能性があります。細胞培養では、HSV-1 および HSV-2 の TK に以下の耐性関連置換が観察されました (表 1)。
HSV 感染患者の場合
α-ヘルペスウイルス感染症の治療に失敗した患者から得られた臨床 HSV-1 および HSV-2 分離株を、TK および POL 遺伝子の遺伝子型の変化、およびアシクロビルに対する表現型の耐性について評価しました (表 2)。 TK および POL にフレーム シフト変異および耐性関連置換を有する HSV 分離株が同定されました。アシクロビルに対する感受性の低下につながる HSV TK および POL の置換のリストはすべてを網羅しているわけではなく、アシクロビルを含むレジメンに失敗した患者から分離された HSV バリアントで追加の変更が特定される可能性があります。アシクロビルに対するウイルス耐性の可能性は、治療中に反応しないか再発性のウイルス排出を経験する患者で考慮されるべきです.
交差抵抗
交差耐性は、フレームシフト変異および耐性関連置換を有する HSV 分離株で観察されており、ペンシクロビル (PCV)、ファムシクロビル (FCV)、およびホスカルネット (FOS) に対する感受性が低下しています [表 3]。
臨床研究
成人対象
ゾビラックス クリームは、再発性口唇ヘルペスの治療のための 2 つの二重盲検ランダム化プラセボ (溶媒) 対照試験で評価されました。平均的な患者は、過去 12 か月間に口唇ヘルペスを 5 回発症しました。最初の試験では、被験者の年齢の中央値は 37 歳 (18 ~ 81 歳の範囲) で、74% が女性、94% が白人でした。 2 回目の試験では、被験者の年齢の中央値は 38 歳 (18 ~ 87 歳の範囲) で、73% が女性、94% が白人でした。被験者は、徴候または症状に気付いてから 1 時間以内に治療を開始し、4 日間治療を継続するように指示されました。両方の研究で、口唇ヘルペス再発エピソードの平均期間は、ゾビラックス クリームで治療された被験者 (n = 682) では、プラセボで治療された被験者 (n = 703) と比較して、約 4.5 日対 5 日間で約半日短かった、 それぞれ。口唇ヘルペス病変の進行の予防において、ゾビラックス クリームまたはプラセボを投与された被験者間で有意差は観察されませんでした。
小児科
口唇ヘルペスを再発した 12 歳から 17 歳の患者 113 人を対象に、ZOVIRAX クリームを使用した非盲検非対照試験が実施されました。この試験では、成人と同じ投与計画を使用して治療が適用され、被験者の有害事象が追跡されました。安全性プロファイルは、成人で観察されたものと同様でした。
患者情報
ゾビラックス (zho-vahy-rex)(アシクロビル) クリーム
重要な情報: ゾビラックス クリームは、唇と口の周りの口唇ヘルペスにのみ使用できます。
ゾビラックス クリームは、目、口、鼻、性器には使用しないでください。
ゾビラックスクリームとは?
- ゾビラックス クリームは、正常な免疫システムを持つ成人および 12 歳以上の子供に再発する口唇ヘルペス (口唇ヘルペス) の治療に使用される処方薬です。
- ゾビラックス クリームは口唇ヘルペスの治療法ではありません。
ゾビラックス クリームが 12 歳未満の子供に安全で効果的かどうかはわかっていません。
ゾビラックス クリームを使用しないでください。 アシクロビル、バラシクロビル、またはゾビラックス クリームのいずれかの成分にアレルギーのある方。ゾビラックス クリームの全成分リストについては、このリーフレットの最後をご覧ください。
ZOVIRAX クリームを使用する前に、医療提供者に何を伝えるべきですか?
ゾビラックス クリームを使用する前に、以下の場合を含め、すべての病状について医療提供者に伝えてください。
- 非常に病気になりやすい(免疫システムが弱い)。
- 妊娠している、または妊娠する予定がある。ゾビラックス クリームが胎児に害を及ぼすかどうかはわかっていません。
- 授乳中または授乳を計画している。ゾビラックス クリームが母乳に移行するかどうかは不明です。ゾビラックス クリームを使用している場合は、赤ちゃんに与える最善の方法について医療提供者に相談してください。
あなたが服用しているすべての薬について、医療提供者に伝えてください。 処方薬および市販薬、ビタミン、ハーブサプリメントを含みます。
ゾビラックス クリームはどのように使用すればよいですか?
- ゾビラックス クリームは、医療機関から指示されたとおりに使用してください。
- かゆみ、発赤、灼熱感、ヒリヒリ感など口唇ヘルペスの最初の症状が現れたら、または口唇ヘルペスが現れたらすぐにゾビラックス クリームを使用してください。
- ゾビラックス クリームを塗布する前後は、石鹸と水で手を洗ってください。
- ゾビラックス クリームを塗布する前に、患部を清潔で乾燥させてください。
- ゾビラックス クリームを患部に 1 日 5 回、4 日間、外縁を含めて塗布します。
- ゾビラックス クリームによる治療中は、患部に他のスキン製品を使用しないでください。
- 口唇ヘルペスが口の周りの他の領域に広がったり、口唇ヘルペスを悪化させたりする可能性があるため、口唇ヘルペスを不必要にこすらないでください。
ゾビラックス クリームの副作用は何ですか?
ゾビラックス クリームの最も一般的な副作用は、治療部位の皮膚反応であり、唇の乾燥またはひび割れ、皮膚の剥離、剥がれまたは乾燥、灼熱感または刺痛感、およびかゆみが含まれる場合があります。
これらは、ZOVIRAX クリームの副作用のすべてではありません。
副作用に関する医学的アドバイスについては、医師に連絡してください。 1-800-FDA-1088 で副作用を FDA に報告できます。
ゾビラックス クリームの保管方法は?
- ゾビラックス クリームは、20°~25°C (68°~77°F) の室温で保管してください。
ゾビラックス クリームとすべての医薬品は、子供の手の届かないところに保管してください。
ゾビラックス クリームの安全で効果的な使用に関する一般的な情報。
医薬品は、患者情報リーフレットに記載されている以外の目的で処方されることがあります。ゾビラックス クリームが処方されていない状態には使用しないでください。ゾビラックス クリームを他の人に与えないでください。あなたと同じ症状の人がいる場合でも.それらに害を及ぼす可能性があります。医療専門家向けに作成されたゾビラックス クリームに関する情報については、薬剤師または医療提供者にお尋ねください。
ゾビラックス クリームの成分は何ですか?
有効成分: アシクロビル
不活性成分: セトステアリルアルコール、ミネラルオイル、ポロキサマー407、プロピレングリコール、ラウリル硫酸ナトリウム、水、白色ワセリン
この患者情報は、米国食品医薬品局によって承認されています。
