Plavix 75mg Clopidogrel 使用法、副作用および投与量。 オンライン薬局の価格。 処方箋不要のジェネリック医薬品。
Plavix 75mg とは何ですか?
プラビックス 75mg は、脳卒中、血栓、心臓発作後の深刻な心臓の問題、重度の胸痛、循環障害などの急性冠症候群の症状を治療するために使用される処方薬です。プラビックス 75mg は、単独で使用することも、他の薬と併用することもできます。
Plavix 75mg は、抗血小板剤、心臓血管、抗血小板剤、血液と呼ばれる薬のクラスに属します。
プラビックスが子供に安全で効果があるかどうかはわかっていません。
プラビックス 75mg の副作用の可能性は何ですか?
プラビックス 75mg は、次のような重大な副作用を引き起こす可能性があります。
- 薄い肌、
- あざができやすい、
- 皮膚の下や口の中の紫色の斑点、
- 皮膚や目の黄色化(黄疸)、
- 速い心拍、
- 呼吸困難、
- 頭痛、
- 熱、
- 弱点、
- 疲労感、
- 排尿がほとんどまたはまったくない、
- 発作(けいれん)、
- 突然のしびれや衰弱、
- 混乱、そして
- 視覚または発話の問題
上記の症状がある場合は、すぐに医療機関を受診してください。
プラビックスの最も一般的な副作用は次のとおりです。
- 出血の増加、
- 鼻血、
- 頭痛、
- かゆみ、そして
- あざ
警告
CYP2C19遺伝子の2つの機能喪失対立遺伝子を有する患者における抗血小板効果の減少
Plavix 75mg の有効性は、シトクロム P450 (CYP) システム、主に CYP2C19 による活性代謝物への変換に依存する抗血小板活性に起因します [ 警告と注意事項 、 臨床薬理学 ]。推奨用量のプラビックスは、活性代謝産物の形成が少ないため、CYP2C19 遺伝子の非機能的対立遺伝子のホモ接合体である患者 (「CYP2C19 低代謝者」と呼ばれる) の血小板活性への影響が減少します。 CYP2C19 代謝不良の患者を特定するための検査が利用可能である [参照 臨床薬理学 ]。 CYP2C19 代謝不良と特定された患者では、別の血小板 P2Y12 阻害剤の使用を検討してください。
説明
Plavix (クロピドグレル重硫酸塩) は、P2Y12 ADP 血小板受容体のチエノピリジン クラスの阻害剤です。化学的には、メチル (+)-(S)-α-(2-クロロフェニル)-6,7-ジヒドロチエノ[3,2-c]ピリジン-5(4H)-アセテート スルフェート (1:1) です。クロピドグレル重硫酸塩の実験式は C16H16ClNO2S・H2SO4 であり、その分子量は 419.9 です。構造式は次のとおりです。

クロピドグレル重硫酸塩は、白色からオフホワイトの粉末です。中性 pH で水にほとんど溶けないが、pH 1 で自由に溶ける。また、メタノールに溶けやすく、塩化メチレンにやや溶けにくく、エチル エーテルにほとんど溶けない。約 +56° の特定の旋光度があります。
経口投与用のプラビックスは、クロピドグレル塩基 75 mg のモル当量である 97.875 mg のクロピドグレル重硫酸塩を含むピンク色、円形、両凸型、デボス加工、フィルムコーティング錠、または 391.5 mg を含むピンク色、楕円形、デボス加工フィルムコーティング錠のいずれかとして提供されます。クロピドグレル塩基 300 mg のモル当量である重硫酸クロピドグレルの。
各錠剤には、硬化ヒマシ油、ヒドロキシプロピルセルロース、マンニトール、微結晶性セルロース、ポリエチレングリコール 6000 が不活性成分として含まれています。ピンク色のフィルム コーティングには、酸化鉄、ヒプロメロース 2910、ラクトース一水和物、二酸化チタン、トリアセチンが含まれています。錠剤はカルナバワックスで磨かれています。
適応症
急性冠症候群(ACS)
- Plavix 75mg は、以下の患者を含む、非 ST 上昇型 ACS (不安定狭心症 [UA]/非 ST 上昇型心筋梗塞 [NSTEMI]) 患者の心筋梗塞 (MI) および脳卒中の発生率を低下させることが示されています。医学的に管理されるものと、冠動脈血行再建術で管理されるもの。 Plavix 75mg は、アスピリンと併用して投与する必要があります。
- Plavix は、医学的に管理される急性 ST 上昇型心筋梗塞 (STEMI) 患者の心筋梗塞および脳卒中の発生率を低下させることが示されています。 Plavix 75mg は、アスピリンと併用して投与する必要があります。
最近の心筋梗塞、最近の脳卒中、または確立された末梢動脈疾患
末梢動脈疾患が確立されているか、最近の心筋梗塞(MI)または最近の脳卒中の病歴がある患者では、Plavix 75mg が MI および脳卒中の発生率を低下させることが示されています。
投薬と管理
急性冠症候群
数時間以内に抗血小板効果が必要な患者では、Plavix を 300 mg の経口負荷用量で開始し、その後 1 日 1 回 75 mg を継続します。負荷用量なしでプラビックス 75mg を開始すると、抗血小板効果の確立が数日遅れます。 臨床薬理学 と 臨床研究 ]。
最近の心筋梗塞、最近の脳卒中、または確立された末梢動脈疾患
75 mg を 1 日 1 回、負荷用量なしで経口投与 [参照 臨床薬理学 と 臨床研究 ]。
供給方法
剤形と強度
- 75 mg 錠: 片面に「75」、もう片面に「1171」と刻印されたピンク色、円形、両凸、フィルムコーティング錠
- 300mg錠:片面に「300」、片面に「1332」と刻印されたピンク色の長方形のフィルムコーティング錠
保管と取り扱い
プラビックス(クロピドグレル重硫酸塩)75mg 錠剤は、片面に「75」、もう片面に「1171」とデボス加工された、ピンク色の丸い両凸のフィルムコーティング錠として入手できます。タブレットは次のように提供されます。
NDC 63653-1171-6 30本入りボトル NDC 63653-1171-1 90本入りボトル NDC 63653-1171-5 500本入りボトル NDC 63653-1171-3 ブリスター 100 個
プラビックス(クロピドグレル重硫酸塩) 300mg 錠剤は、片面に「300」、もう片面に「1332」とデボス加工された、ピンク色の長方形のフィルムコーティング錠として入手できます。タブレットは次のように提供されます。
NDC 63653-1332-2 30 個の単位用量パッケージ
25°C (77°F) で保管してください。 15°C-30°C (59°F-86°F) [参照 USP制御の室温 ]。
配布元: Bristol-Myers Squibb/Sanofi Pharmaceuticals Partnership, Bridgewater, NJ 08807. 改訂: 2021 年 3 月
副作用
以下の重篤な副作用については、以下およびラベルの他の箇所で説明されています。
- 出血[参照 警告と注意事項 ]
- 血栓性血小板減少性紫斑病 [参照 警告と注意事項 ]
臨床試験の経験
臨床試験はさまざまな条件とフォローアップ期間の下で実施されるため、ある薬剤の臨床試験で観察された有害反応率を別の薬剤の臨床試験で観察された率と直接比較することはできず、実際に観察された率を反映していない可能性があります。
Plavix は、1 年以上治療を受けた 21,000 人以上の患者を含む 54,000 人以上の患者で安全性が評価されています。 Plavix 75mg + アスピリンとプラセボ + アスピリンを比較した試験、および Plavix 単独とアスピリン単独を比較した試験で観察された臨床的に重要な副作用について以下に説明します。
出血
治す
CURE では、プラビックスとアスピリンの併用は、アスピリンを含むプラセボと比較して、大出血 (主に胃腸および穿刺部位) の増加と関連していました (表 1 を参照)。頭蓋内出血 (0.1%) と致命的な出血 (0.2%) の発生率は、両群で同じでした。クロピドグレル群でより頻繁に報告されたその他の出血イベントは、鼻出血、血尿、あざでした。
出血の全体的な発生率を表 1 に示します。
専念
COMMIT では、Plavix 75mg 群とプラセボ群で同程度の大出血率が観察され、どちらもアスピリンも投与されました (表 2 を参照)。
CAPRIE(プラビックス対アスピリン)
CAPRIEでは、アスピリンを服用している患者では2.7%であったのに対し、プラビックス75mgを服用している患者では2.0%の割合で消化管出血が発生しました。入院を必要とする出血は、それぞれ 0.7% と 1.1% で発生しました。頭蓋内出血の発生率は、アスピリンの 0.5% と比較して、プラビックスの 0.4% でした。
Plavix 75mg群でより頻繁に報告された他の出血イベントは、鼻出血と血腫でした.
その他の有害事象
プラビックスとアスピリンをアスピリン単独と比較したCUREとCHARISMAでは、プラビックスとプラセボの間で(出血以外の)有害事象の発生率に差はありませんでした。
プラビックス 75mg とアスピリンを比較した CAPRIE では、プラビックスを服用している人でより頻繁にそう痒症が報告されました。有害事象(出血以外)の発生率に他の違いは報告されていません。
市販後の経験
プラビックスの承認後の使用中に、次の副作用が確認されました。これらの反応は未知の規模の集団から自発的に報告されるため、その頻度を確実に推定したり、薬物曝露との因果関係を確立したりすることが常に可能であるとは限りません。
致命的な転帰を伴うものを含む出血は、プラビックスで治療された患者で報告されています。
- 血液およびリンパ系の障害: 無顆粒球症、再生不良性貧血/汎血球減少症、血栓性血小板減少性紫斑病 (TTP)、後天性血友病 A
- 胃腸障害: 大腸炎(潰瘍性大腸炎、リンパ球性大腸炎を含む)、膵炎、口内炎、胃・十二指腸潰瘍、下痢
- 全身疾患および投与部位の状態: 熱
- 肝胆道障害: 急性肝不全、肝炎(非感染性)、肝機能検査異常
- 免疫系障害: 過敏症反応、アナフィラキシー反応、血清病、インスリン自己免疫症候群、重度の低血糖につながる可能性があります
- 筋骨格、結合組織および骨の障害: 筋肉痛、関節痛、関節炎
- 神経系障害: 味覚障害、頭痛、老化
- 精神障害: 混乱、幻覚
- 呼吸器、胸部および縦隔の障害: 気管支痙攣、間質性肺炎、好酸球性肺炎
- 腎および泌尿器疾患: クレアチニン値の上昇
- 皮膚および皮下組織の障害: 黄斑丘疹、紅斑性または剥離性発疹、蕁麻疹、水疱性皮膚炎、湿疹、中毒性表皮壊死融解症、スティーブンス・ジョンソン症候群、急性汎発性発疹性膿疱症(AGEP)、血管性浮腫、薬物誘発性過敏症症候群、好酸球増加症および全身症状を伴う薬物発疹(DRESS)、多形紅斑、扁平苔癬、全身のかゆみ
- 血管障害: 血管炎、低血圧
薬物相互作用
CYP2C19 インデューサー
クロピドグレルは CYP2C19 によって部分的にその活性代謝物に代謝されるため、この酵素の活性を誘導する薬物を使用すると、クロピドグレルの活性代謝物の薬物レベルが増加すると予想されます。
リファンピンは CYP2C19 を強く誘導し、クロピドグレルの活性代謝物レベルの上昇と血小板阻害の両方を引き起こし、特に出血のリスクを高める可能性があります。予防措置として、強力な CYP2C19 インデューサーの併用は避けてください [ 警告と注意事項 と 臨床薬理学 ]。
CYP2C19阻害剤
クロピドグレルは、CYP2C19 によって一部活性代謝物に代謝されます。この酵素の活性を阻害する薬剤を併用すると、クロピドグレルの活性代謝物の血漿中濃度が低下し、血小板阻害が低下する[参照 警告と注意事項 ]。
オメプラゾールまたはエソメプラゾール
Plavix 75mg とオメプラゾールまたはエソメプラゾールの併用は避けてください。臨床研究では、オメプラゾールは、同時にまたは12時間間隔で投与された場合、Plavix 75mgの抗血小板活性を大幅に低下させることが示されました.プラビックスと同時にエソメプラゾールを投与した場合、抗血小板活性の同様の低下が観察されました。デクスランソプラゾール、ランソプラゾール、およびパントプラゾールは、オメプラゾールまたはエソメプラゾールよりもプラビックスの抗血小板活性への影響が少なかった[参照 警告と注意事項 と 臨床薬理学 ]。
オピオイド
他の経口 P2Y12 阻害剤と同様に、オピオイドアゴニストの同時投与はクロピドグレルの吸収を遅らせ、減少させます。 臨床薬理学 ]。モルヒネまたは他のオピオイドアゴニストの同時投与が必要な急性冠症候群患者では、非経口抗血小板薬の使用を検討してください。
非ステロイド系抗炎症薬(NSAID)
Plavix 75mg と NSAIDs の同時投与は、消化管出血のリスクを高めます。
ワルファリン(CYP2C9基質)
クロピドグレル 75 mg/日の投与は、長期ワルファリン療法を受けている患者の S-ワルファリン (CYP2C9 基質) または INR の薬物動態を変更しませんでしたが、プラビックス 75 mg とワルファリンの同時投与は、止血。
しかし、in vitro での高濃度では、クロピドグレルは CYP2C9 を阻害します。
SSRIとSNRI
選択的セロトニン再取り込み阻害剤 (SSRI) およびセロトニン ノルエピネフリン再取り込み阻害剤 (SNRI) は血小板の活性化に影響を与えるため、SSRI および SNRI とクロピドグレルの併用は出血のリスクを高める可能性があります。
レパグリニド (CYP2C8 基質)
クロピドグレルのアシル-β-グルクロニド代謝産物は、CYP2C8 の強力な阻害剤です。 Plavix 75mg は、主に CYP2C8 によって除去される薬物への全身暴露を増加させる可能性があるため、用量調整と適切なモニタリングが必要です。
プラビックスは、レパグリニド曝露を 3.9 倍から 5.1 倍増加させた [参照 臨床薬理学 ]。レパグリニドとプラビックスの併用は避けてください。併用が避けられない場合は、レパグリニドを毎食前に 0.5 mg から開始し、1 日総用量 4 mg を超えないようにしてください。併用中は、グルコースモニタリングの頻度を増やす必要がある場合があります。
警告
の一部として含まれています 予防 セクション。
予防
CYP2C19機能障害患者における抗血小板活性の低下
クロピドグレルはプロドラッグです。クロピドグレルによる血小板凝集の阻害は、活性代謝物によって達成されます。クロピドグレルの活性代謝物への代謝は、CYP2C19 の遺伝的変異によって損なわれる可能性があります [参照 囲み警告 ]。
クロピドグレルの代謝は、オメプラゾールやエソメプラゾールなどの CYP2C19 を阻害する薬剤によっても損なわれる可能性があります。プラビックスとオメプラゾールまたはエソメプラゾールとの併用は避けてください。どちらもプラビックスの抗血小板活性を大幅に低下させるためです。 薬物相互作用 ]。
出血の一般的なリスク
プラビックスを含む P2Y12 阻害剤 (チエノピリジン) は、出血のリスクを高めます。
P2Y12 阻害剤 (チエノピリジン) は、血小板の寿命の間 (7 ~ 10 日間) 血小板凝集を阻害します。クロピドグレルの活性代謝物の半減期は短いため、外因性血小板を投与することで止血を回復できる可能性があります。ただし、負荷投与の 4 時間以内または維持投与の 2 時間以内の血小板輸血は、効果が低い可能性があります。
CYP2C19 の活性を誘導する薬物の使用は、クロピドグレルの活性代謝物の薬物レベルの増加をもたらすと予想され、出血リスクを増強する可能性があります。予防措置として、強力な CYP2C19 インデューサーの併用は避けてください [ 薬物相互作用 と 臨床薬理学 ]。
プラビックスの中止
プラビックスの中止は、心血管イベントのリスクを高めます。 Plavix を一時的に中止しなければならない場合 (例えば、出血の治療や出血のリスクが高い手術のため) は、できるだけ早く再開してください。可能であれば、そのような手術の 5 日前から Plavix による治療を中断してください。止血が達成されたらすぐにプラビックス 75mg を再開してください。
血栓性血小板減少性紫斑病 (TTP)
TTPは、時には致命的であり、Plavix 75mgの使用後、時には短期間(2週間未満)の使用後に報告されています. TTP は、プラズマフェレーシス (血漿交換) を含む緊急の治療を必要とする深刻な状態です。血小板減少症、微小血管障害性溶血性貧血(末梢塗抹標本で見られる分裂赤血球[断片化した赤血球])、神経学的所見、腎機能障害、発熱[ 有害反応 ]。
チエノピリジン間の交差反応性
発疹、血管性浮腫または血液反応を含む過敏症は、他のチエノピリジンに対する過敏症または血液反応の既往歴のある患者を含む、プラビックス 75mg を投与された患者で報告されています。 禁忌 と 有害反応 ]。
患者相談情報
FDA 承認の患者ラベリング ( 投薬ガイド )。
中止
Plavix を処方した医療提供者と最初に話し合うことなく、Plavix を中止しないように患者に助言する [ 警告と注意事項 ]。
出血
患者に次のことをアドバイスします。
- あざができて出血しやすくなります
- 止血に通常より時間がかかる
- 予期しない出血、長引く出血、過剰な出血、または便や尿に血が混じっている場合は報告する必要があります [参照 警告と注意事項 ]
血栓性血小板減少性紫斑病
他の方法では説明できない TTP の症状を経験した場合は、速やかに医師の診察を受けるよう患者に指示する [参照 警告と注意事項 ]。
侵襲的処置
手術や歯科処置の前に、プラビックスを服用していることを医師や歯科医に知らせるよう患者に助言する[参照 警告と注意事項 ]。
プロトンポンプ阻害剤
プラビックスを服用している間は、オメプラゾールまたはエソメプラゾールを服用しないように患者にアドバイスしてください。デクスランソプラゾール、ランソプラゾール、およびパントプラゾールは、オメプラゾールまたはエソメプラゾールよりもプラビックス 75mg の抗血小板活性に対する顕著な影響が少なかった [参照 薬物相互作用 ]。
非臨床毒性学
発がん、突然変異誘発、生殖能力の障害
クロピドグレルをマウスに 78 週間、ラットに 104 週間、1 日あたり最大 77 mg/kg の用量で投与した場合、腫瘍形成性の証拠はありませんでした。これにより、推奨される 1 日用量 75 mg でのヒトの 25 倍を超える血漿曝露が得られました。
クロピドグレルは、4 つの in vitro 試験 (Ames 試験、ラット肝細胞における DNA 修復試験、チャイニーズハムスター繊維芽細胞における遺伝子突然変異試験、およびヒトリンパ球の中期染色体分析) および 1 つの in vivo 試験 (経口経路による小核試験) で遺伝毒性を示さなかった。マウス)。
クロピドグレルは、1日400 mg/kg (mg/m²ベースでヒトの推奨用量の52倍) までの経口用量で、ペアリング前および妊娠期間を通して処置された雄および雌のラットの生殖能力に影響を及ぼさないことがわかった.
特定の集団での使用
妊娠
リスクの概要
出版された文献で報告された症例から得られた入手可能なデータと、妊娠中の女性におけるクロピドグレルの使用に関する市販後調査では、主要な先天性欠損症または流産の薬物関連リスクは特定されていません[参照 データ ].心筋梗塞や脳卒中に関連する妊婦や胎児へのリスクがあります[参照 臨床上の考慮事項 ]。クロピドグレルを、器官形成期の妊娠中のラットおよびウサギに、推奨されるヒトの 1 日用量の 65 倍および 78 倍に相当する用量で投与した場合、胎仔毒性の証拠は観察されませんでした。 データ ]。
示された集団の主要な先天性欠損症および流産の推定背景リスクは不明です。すべての妊娠には、先天異常、喪失、またはその他の有害な転帰の背景リスクがあります。米国の一般集団では、臨床的に認識された妊娠における主要な先天性欠損症および流産の推定背景リスクは、それぞれ 2% ~ 4% および 15% ~ 20% です。
臨床上の考慮事項
病気に関連する母体および/または胚/胎児のリスク
心筋梗塞と脳卒中は緊急事態です。胎児へのクロピドグレルの影響に関する潜在的な懸念があるため、妊娠中の女性の治療を差し控えるべきではありません。
労働または配達
分娩中または分娩中にクロピドグレルを使用すると、母体の出血や出血のリスクが高まります。脊髄血腫のリスクがあるため、クロピドグレルの使用中は神経軸ブロックを避けてください。可能であれば、陣痛、分娩、神経軸ブロックの 5 ~ 7 日前にクロピドグレルを中止してください。
データ
ヒューマンデータ
市販後 20 年間に使用された公開された症例報告から得られた入手可能なデータでは、妊娠中のクロピドグレルの使用と主要な先天性欠損症、流産、または有害な胎児転帰との関連性は確認されていません。
動物データ
胚・胎児発生毒性研究は、妊娠中のラットとウサギを対象に、器官形成期にそれぞれ最大 500 および 300 mg/kg/日の用量で実施されました。これらの用量は、mg/m² に基づいて、それぞれヒトの 1 日推奨用量の 65 倍および 78 倍に相当し、クロピドグレルによる受胎能障害または胎児毒性の証拠は明らかにされませんでした。
授乳
リスクの概要
母乳中のクロピドグレルの存在または乳生産への影響に関するデータはありません。少数の市販後症例において、授乳中の母親のクロピドグレル使用による、母乳育児に対する悪影響は観察されていません。ラットでの研究では、クロピドグレルおよび/またはその代謝物が乳汁中に存在することが示されています。薬物が動物の乳に存在する場合、その薬物は母乳にも存在する可能性があります。母乳育児の発達上および健康上の利点は、PLAVIX に対する母親の臨床的必要性、および PLAVIX 75mg または母体の基礎疾患による母乳育児への潜在的な悪影響と併せて考慮する必要があります。
小児用
小児集団における安全性と有効性は確立されていません。
無作為化プラセボ対照試験(CLARINET)では、全身から肺への動脈シャントで緩和されたチアノーゼ先天性心疾患の新生児および乳児におけるクロピドグレルの臨床的利点は示されませんでした。この結果に寄与する可能性のある要因は、クロピドグレルの投与量、アスピリンの併用投与、およびシャント緩和後の治療開始の遅れでした。異なるデザインの試験がこの患者集団に臨床的利益をもたらす可能性を排除することはできません.
高齢者の使用
CAPRIE および CURE 対照臨床試験の被験者総数のうち、プラビックスで治療された患者の約 50% が 65 歳以上で、15% が 75 歳以上でした。 COMMIT では、Plavix 75mg で治療された患者の約 58% が 60 歳以上で、そのうち 26% が 70 歳以上でした。
Plavix 75mg + アスピリン対プラセボ + アスピリンで観察された出血イベントの年齢区分別リスクは、CURE および COMMIT 試験についてそれぞれ表 1 および表 2 に示されています。 有害反応 ]。高齢患者では用量調整は必要ありません。
腎障害
重度および中等度の腎障害のある患者では経験が限られている[参照 臨床薬理学 ]。
肝障害
肝機能障害のある患者では、用量調整は必要ありません。 臨床薬理学 ]。
過剰摂取
プラビックスによる血小板阻害は不可逆的であり、血小板の寿命の間持続します。クロピドグレル投与後の過剰摂取は、出血性合併症を引き起こす可能性があります。 1500 または 2000 mg/kg のクロピドグレルの単回経口投与は、マウスとラットに、3000 mg/kg のヒヒに致死的でした。急性毒性の症状は、動物の嘔吐、衰弱、呼吸困難、および消化管出血でした。
生物学的妥当性に基づいて、血小板輸血は凝固能力を回復させる可能性があります。
禁忌
活発な出血
プラビックスは、消化性潰瘍や頭蓋内出血などの活発な病的出血のある患者には禁忌です。
過敏症
プラビックス 75 mg は、クロピドグレルまたは製品の成分に対する過敏症 (アナフィラキシーなど) のある患者には禁忌です [ 有害反応 ]。
臨床薬理学
作用機序
クロピドグレルは、その活性代謝物が血小板上の ADP 受容体の P2Y12 クラスに不可逆的に結合することにより、血小板の活性化と凝集を阻害します。
薬力学
クロピドグレルは、血小板凝集を阻害する活性代謝物を生成するために、CYP450 酵素によって代謝されなければなりません。クロピドグレルの活性代謝物は、アデノシン二リン酸 (ADP) の血小板 P2Y12 受容体への結合を選択的に阻害し、その後の ADP を介した糖タンパク質 GPIIb/IIIa 複合体の活性化を阻害し、それによって血小板凝集を阻害します。このアクションは元に戻せません。その結果、クロピドグレルの活性代謝物にさらされた血小板は、残りの寿命 (約 7 ~ 10 日) にわたって影響を受けます。 ADP 以外のアゴニストによって誘導される血小板凝集も、放出された ADP による血小板活性化の増幅をブロックすることによって阻害されます。
血小板凝集の用量依存的な阻害は、プラビックスの単回経口投与の2時間後に見られます。 1 日 75 mg の Plavix の反復投与は、初日に ADP 誘発血小板凝集を阻害し、阻害は 3 日目から 7 日目の間に定常状態に達します。 40% から 60% の間。血小板凝集および出血時間は、治療を中止した後、通常約 5 日で徐々にベースライン値に戻ります。
高齢患者
高齢者 (75 歳以上) と若い健康な被験者は、血小板凝集に対して同様の効果がありました。
腎障害患者
1日あたり75mgのPlavix 75mgを繰り返し投与した後、重度の腎障害(クレアチニンクリアランスが5から15mL /分)および中等度の腎障害(クレアチニンクリアランスが30から60mL /分)の患者は、 ADP 誘発血小板凝集。
肝障害患者
重度の肝障害を持つ患者に 1 日 75 mg の Plavix を 10 日間反復投与した後、ADP 誘発血小板凝集の阻害は、健康な被験者で観察されたものと同様でした。
性別
男性と女性を比較した小規模な研究では、女性では ADP による血小板凝集の抑制が少ないことが観察されました。
薬物動態
クロピドグレルはプロドラッグであり、薬理学的に活性な代謝物と不活性な代謝物に代謝されます。
吸収
クロピドグレルは、1 日 75 mg を単回および反復経口投与した後、急速に吸収されます。吸収は、クロピドグレル代謝物の尿中排泄に基づいて、少なくとも 50% です。
食事の効果
プラビックスは食事の有無にかかわらず投与できます。 1日あたり75mgのPlavixが標準的な朝食とともに与えられたときの健康な男性被験者の研究では、ADP誘発血小板凝集の平均阻害は9%未満減少した.活性代謝物 AUC0-24 は食物の存在下で変化しませんでしたが、活性代謝物 Cmax は 57% 減少しました。 Plavix 300 mg の負荷用量を高脂肪の朝食とともに投与した場合にも、同様の結果が観察されました。
代謝
クロピドグレルは、2 つの主要な代謝経路によって広範囲に代謝されます。1 つはエステラーゼによって媒介され、不活性なカルボン酸誘導体 (循環代謝産物の 85%) への加水分解をもたらし、もう 1 つは複数のシトクロム P450 酵素によって媒介されます。シトクロムは、最初にクロピドグレルを 2-オキソ-クロピドグレル中間代謝物に酸化します。 2-オキソクロピドグレル中間代謝産物のその後の代謝により、クロピドグレルのチオール誘導体である活性代謝産物が形成されます。活性代謝物は、CYP1A2、CYP2B6 および CYP3A を含むいくつかの他の CYP 酵素からの寄与により、主に CYP2C19 によって形成されます。活性チオール代謝物は血小板受容体に迅速かつ不可逆的に結合し、血小板の寿命の間血小板凝集を阻害します。
活性代謝物の Cmax は、300 mg のクロピドグレルを 1 回負荷投与した後の方が、75 mg の維持投与を 4 日間行った後よりも 2 倍高くなっています。 Cmax は、投与後約 30 ~ 60 分で発生します。 75 ~ 300 mg の用量範囲では、活性代謝物の薬物動態は用量比例性から逸脱します。用量が 4 倍になると、Cmax と AUC はそれぞれ 2.0 倍と 2.7 倍になります。
排除
ヒトに 14C 標識クロピドグレルを経口投与した後、投与後 5 日間で総放射能の約 50% が尿中に、約 46% が糞中に排泄された。 75 mg を 1 回経口投与した場合、クロピドグレルの半減期は約 6 時間です。活性代謝物の半減期は約 30 分です。
薬物相互作用
プラビックスに対する他の薬の効果
クロピドグレルは、CYP2C19 によって一部活性代謝物に代謝されます。
CYP2C19 インデューサー
CYP2C19 の強力なインデューサーを併用すると、クロピドグレルの活性代謝物の血漿濃度が増加し、血小板阻害が増加します。
リファンピン: 健康な成人にリファンピン 300 mg を 1 日 2 回 7 日間、負荷用量のクロピドグレル 600 mg と併用投与すると、クロピドグレルのチオール代謝産物の平均 AUC と Cmax が 3.8 倍増加しました。投与後 4 時間での血小板凝集の平均阻害は、クロピドグレルを単独で投与した場合と比較して、リファンピンの存在下で 34% 高かった。
CYP2C19阻害剤
この酵素の特定の阻害剤を併用すると、クロピドグレルの活性代謝物の血漿濃度が低下し、血小板阻害が低下します。
プロトンポンプ阻害剤 (PPI)
専用の薬物相互作用研究で評価された Plavix 75 mg の複数回投与後のクロピドグレル活性代謝物への全身暴露に対するプロトンポンプ阻害剤 (PPI) の効果を図 1 に示します。
図 1: Plavix 75 mg 単独またはプロトンポンプ阻害剤 (PPI) を複数回投与した後のクロピドグレル活性代謝物への曝露
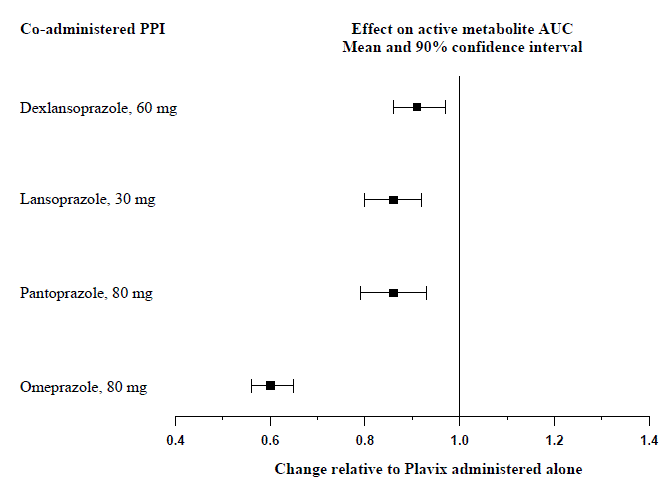
これらの研究で測定された薬力学的および薬物動態パラメータは、相互作用がオメプラゾールで最も高く、デキスランソプラゾールで最も少ないことを示しました。
オピオイド
健康な成人に 5 mg の静脈内モルヒネと 600 mg の負荷用量のクロピドグレルを同時投与すると、クロピドグレルのチオール代謝産物の AUC と Cmax が 34% 減少しました。平均血小板凝集は、モルヒネ同時投与で 2 ~ 4 時間まで高かった。
プラビックス 75mg が他の薬剤に及ぼす影響
in vitro 研究では、クロピドグレルのグルクロニド代謝物が CYP2C8 の強力な阻害剤であることが示されています。プラビックスとレパグリニドの併用投与は、レパグリニドへの全身暴露 (AUC0-∞) を負荷用量 (300 mg) 後に 5.1 倍、プラビックスの維持用量 (75 mg) の 3 日目に 3.9 倍増加させた [参照 薬物相互作用 ]。
ファーマコゲノミクス
CYP2C19 は、活性代謝物と 2-オキソ-クロピドグレル中間代謝物の両方の形成に関与しています。クロピドグレルの活性代謝物の薬物動態と抗血小板効果は、ex vivo 血小板凝集アッセイで測定され、CYP2C19 遺伝子型によって異なります。 CYP2C19 遺伝子の非機能的対立遺伝子のホモ接合体である患者は、「CYP2C19 低代謝者」と呼ばれます。白人患者の約 2% と黒人患者の 4% は代謝不良です。代謝不良の有病率は、アジア人患者でより高い(例えば、中国人の 14%)。 CYP2C19 代謝不良の患者を特定するための検査が利用可能です。
40 人の健康な被験者 (4 つの CYP2C19 代謝グループにそれぞれ 10 人) を対象としたクロスオーバー試験では、300 mg に続いて 1 日あたり 75 mg、600 mg に続いて 1 日あたり 150 mg をそれぞれ合計 5 日間使用して、薬物動態および抗血小板反応を評価しました。他のグループと比較して、低代謝者では、活性代謝物への曝露の減少と血小板凝集の抑制の減少が観察されました。
臨床研究
急性冠症候群
治す
CURE研究には、ST上昇(UAまたはNSTEMI)がなく、胸痛または虚血に一致する症状の最新エピソードの発症から24時間以内に発症した12,562人のACS患者が含まれた。患者は、新しい虚血に適合するECG変化(ST上昇なし)、または心筋酵素またはトロポニンIまたはTが正常上限の少なくとも2倍に上昇している必要がありました。
患者は無作為にプラビックス(300 mg の負荷量に続いて 75 mg を 1 日 1 回投与)またはプラセボの投与を受けるように無作為に割り付けられ、最大 1 年間治療されました。患者は、アスピリン (1 日 1 回 75 ~ 325 mg) およびヘパリンなどの他の標準治療も受けました。無作為化の 3 日前から、GPIIb/IIIa 阻害剤の使用は許可されませんでした。
患者集団は主に白人 (82%) で、38% が女性、52% が 65 歳以上でした。最初の入院中に血行再建術を受けた患者は約 20% にすぎず、緊急または緊急の血行再建術を受けた患者はほとんどいませんでした。
主要転帰(心血管死、心筋梗塞、または脳卒中)を経験した患者の数は、プラビックス治療群で 582 人(9.3%)、プラセボ治療群で 719 人(11.4%)であり、相対リスクが 20% 減少しました(95 Plavix 投与群の % CI は 10% ~ 28%、p
プラビックスの効果のほとんどは最初の 2 か月に現れましたが、プラセボとの差は試験期間中 (最大 12 か月) 維持されました (図 2 を参照)。
図 2: CURE 研究における心血管死、心筋梗塞、脳卒中
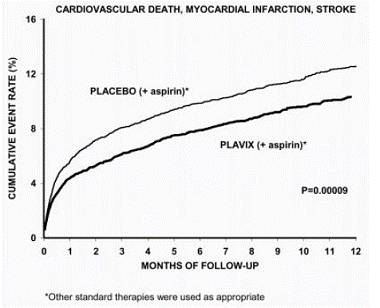
図 3 に示すように、プラビックス 75mg の効果は、さまざまなサブグループで有意差はありませんでした。 (GPIIb/IIIa) 阻害剤、脂質低下薬、ベータ遮断薬、および ACE 阻害薬。 Plavix の有効性は、アスピリンの投与量 (1 日 1 回 75 ~ 325 mg) とは無関係に観察されました。 CUREでは、経口抗凝固薬、研究対象外の抗血小板薬、および慢性NSAIDの使用は許可されていませんでした。
図 3: CURE 研究における患者のベースライン特性と研究中の併用薬/介入のハザード比
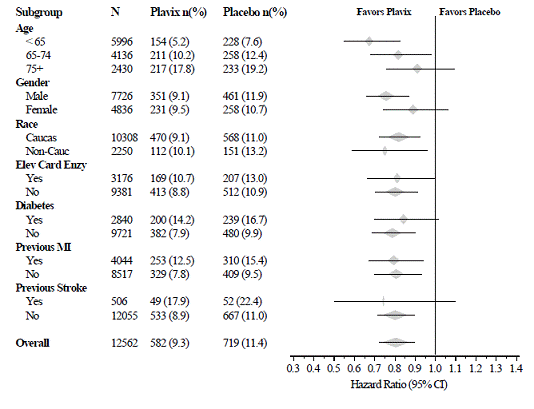
図 3: CURE 研究における患者のベースライン特性と研究中の併用薬/介入のハザード比 (続き)
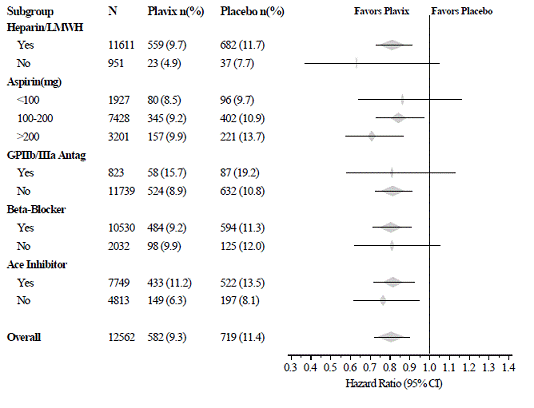
CUREでのプラビックスの使用は、血栓溶解療法の使用の減少と関連していました(プラビックス75mg群で71人の患者[1.1%]、プラセボ群で126人の患者[2.0%]; 43%の相対リスク減少)、およびGPIIb/IIIa 阻害剤 (Plavix 75mg グループの 369 人の患者 [5.9%]、プラセボ グループの 454 人の患者 [7.2%]、18% の相対リスク低減)。 CUREでのプラビックス75mgの使用は、CABGまたはPCI(ステント留置の有無にかかわらず)で治療された患者の数に影響を与えませんでした(プラビックス75mgグループで2253人の患者[36.0%]、プラセボグループで2324人の患者[36.9%];相対4.0%のリスク削減)。
専念
STEMI 患者における Plavix の安全性と有効性は、無作為化プラセボ対照二重盲検試験 COMMIT で評価されました。 COMMIT には、心筋梗塞の症状の発症から 24 時間以内に ECG 異常 (すなわち、ST 上昇、ST 低下、または左脚ブロック) を伴う 45,852 人の患者が含まれていました。患者は、28 日間または退院までのいずれか早い方で、アスピリン (1 日 162 mg) と組み合わせてプラビックス (1 日 1 回 75 mg) またはプラセボを投与される群に無作為に割り付けられました。
主要エンドポイントは、あらゆる原因による死亡と、再梗塞、脳卒中、または死亡の最初の発生でした。
患者集団は 28% が女性で、58% が 60 歳以上 (26% が 70 歳以上) でした。患者の 55% (55%) が血栓溶解薬を受け、PCI を受けたのはわずか 3% でした。
以下の表 5、図 4、および図 5 に示すように、プラビックスは、あらゆる原因による死亡の相対リスクを 7% (p=0.029) 大幅に減少させ、再梗塞、脳卒中または死亡の組み合わせの相対リスクを 9% ( p=0.002)。
図 4: COMMIT 研究における死亡の累積イベント発生率*
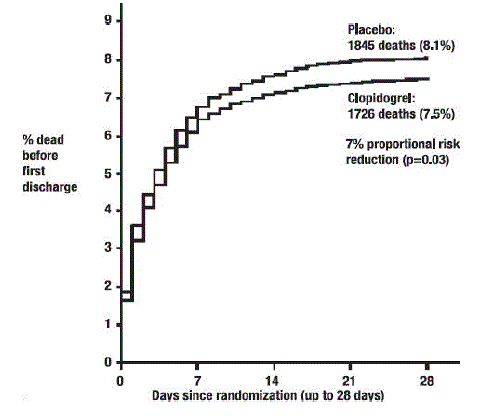
図 5: COMMIT スタディにおけるエンドポイントの再梗塞、脳卒中または死亡を組み合わせた累積イベント率*
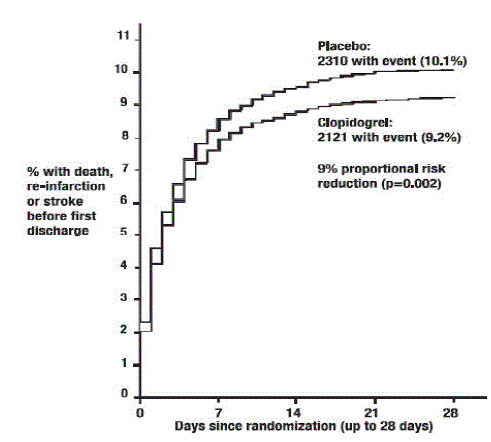
プラビックス 75mg の効果は、図 6 に示すように、事前に指定されたさまざまなサブグループで有意差はありませんでした。効果は、梗塞部位、キリップ クラス、または心筋梗塞の既往歴に基づくものを含む、事前に指定されていないサブグループでも同様でした。このようなサブグループ分析は慎重に解釈する必要があります。
図 6: アスピリンに Plavix 75mg を追加することによる、COMMIT 研究のベースラインおよび併用薬サブグループ全体の主要評価項目の組み合わせに対する効果
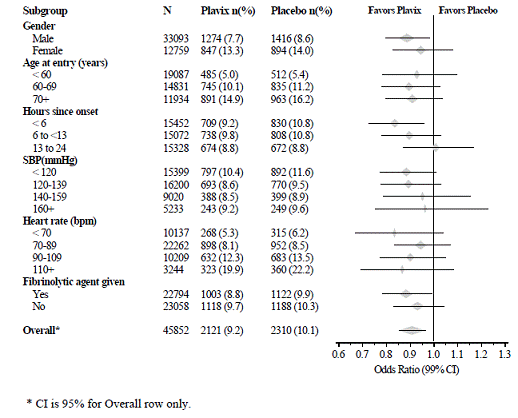
最近の心筋梗塞、最近の脳卒中、または確立された末梢動脈疾患
カプリ
CAPRIE試験は、プラビックス(毎日75mg)とアスピリン(毎日325mg)を比較する、19,185人の患者、304施設の国際的、無作為化、二重盲検、並行群間試験でした。登録する資格を得るには、患者は以下を持っていなければなりませんでした:1)最近の心筋梗塞の病歴(35日以内)。 2) 虚血性脳卒中の最近の病歴 (6 か月以内) で、少なくとも 1 週間の残存神経学的徴候;および/または 3) 確立された末梢動脈疾患 (PAD)。患者は平均 1.6 年間 (最大 3 年間) ランダム化された治療を受けました。
この試験の主な結果は、新しい虚血性脳卒中(致命的かどうか)、新しい心筋梗塞(致命的かどうか)、またはその他の血管死の最初の発生までの時間でした。血管以外の原因に容易に起因しない死亡は、すべて血管に分類されました。
表 6 に示すように、Plavix は転帰イベント、主に MI の発生率の低下と関連していました。全体的な相対リスクの減少 (9.8% 対 10.6%) は 8.7%、p=0.045 でした。血管死亡率と虚血性脳卒中の代わりに、全原因死亡率と全原因脳卒中を数えた場合にも、同様の結果が得られました (リスク低減 6.9%)。研究中の脳卒中または心筋梗塞を生き延びた患者では、その後のイベントの発生率はプラビックス 75 mg グループで低かった.
全体的なイベント率を示す曲線を図 7 に示します。イベント曲線は早期に分離し、3 年間の追跡期間にわたって発散し続けました。
図 7: CAPRIE 研究における致命的または非致命的な血管イベント
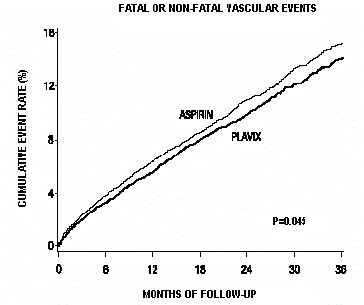
アスピリンよりもプラビックス 75mg を支持する統計的有意性はわずかでした (p=0.045)。しかし、最近心筋梗塞や脳卒中を起こした患者の心血管イベントを減らすのにアスピリン自体が有効であるため、Plavix 75mg の効果は相当なものです。
CAPRIE 試験では、最近心筋梗塞、最近脳卒中、または PAD を発症した集団が登録されました。アスピリンと比較したプラビックス 75mg の有効性は、これらのサブグループ全体で不均一でした (p=0.043) (図 8 を参照)。それにもかかわらず、CAPRIE試験は、個々の患者サブグループにおけるアスピリンに対するPlavix 75mgの相対的な利点を評価するように設計されていないため、この違いは偶然の出来事かもしれません.この利点は、末梢動脈疾患のために登録された患者で最も顕著であり、脳卒中患者ではあまり顕著ではありませんでした。最近の心筋梗塞のみに基づいて試験に登録された患者では、Plavix 75mg は数値的にアスピリンよりも優れていませんでした。
図 8: CAPRIE 研究におけるベースライン サブグループ別のハザード比と 95% CI
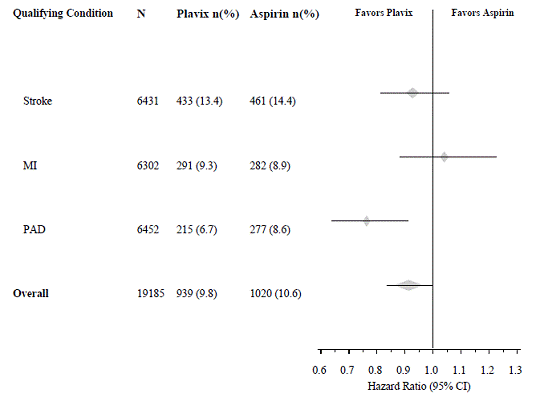
複数の危険因子または確立された血管疾患を有する患者におけるPlavix 75mgとアスピリンの実証された利点はありません
カリスマ
CHARISMA試験は、血管疾患またはアテローム性動脈硬化症の複数の危険因子を有する患者の虚血性イベントの予防について、プラビックス(毎日75mg)とプラセボを比較する15,603人の被験者、無作為化、二重盲検、並行群間試験でした。すべての被験者は、毎日 75 ~ 162 mg のアスピリンで治療されました。平均治療期間は23ヶ月でした。この研究では、主要評価項目である心血管死、MI、または脳卒中の複合体の発生の減少を示すことができませんでした。プラビックス群の合計 534 人 (6.9%) の患者と、プラセボ群の 573 人 (7.4%) の患者が主要転帰イベントを経験しました (p=0.22)。すべての重症度の出血は、プラビックスに無作為に割り付けられた被験者でより一般的でした.
患者情報
プラビックス® (PLAV-iks)(重硫酸クロピドグレル)錠
プラビックスの服用を開始する前、および補充を受けるたびに、この投薬ガイドをお読みください。新しい情報があるかもしれません。この投薬ガイドは、あなたの病状や治療について医師と話すことに代わるものではありません.
Plavix 75mg について知っておくべき最も重要な情報は何ですか?
1. プラビックスは、次の人には効果がない可能性があります。
- 体がプラビックスを分解する方法に影響を与える特定の遺伝的要因があります。 医師は、プラビックスがあなたに適していることを確認するために遺伝子検査を行う場合があります。
- 特定の薬、特にオメプラゾール(Prilosec®)またはエソメプラゾール(Nexium®)を服用してください。 医師は、プラビックスを服用している間、胃酸の問題のために服用する薬を変更する場合があります。
2. プラビックス 75mg は出血を引き起こす可能性があり、これは深刻な場合があり、時には死に至ることもあります。 プラビックスは、体内で血栓が形成される可能性を下げる抗凝血薬です。プラビックスを服用している間:
- あざができて出血しやすくなる
- 鼻血が出る可能性が高くなります
- 出血が止まるまでに時間がかかる
出血のこれらの徴候または症状のいずれかがある場合は、すぐに医師に連絡してください。
- 予期しない出血または長時間続く出血
- 血尿(ピンク、赤、茶色の尿)
- 赤または黒の便(タールのようなもの)
- 原因不明のあざ、または大きくなるあざ
- 血または血の塊を吐き出す
- 血を吐く、または吐いたものがコーヒーかすのように見える
あなたのためにそれを処方する医師に相談せずにプラビックス75mgの服用をやめないでください.プラビックス 75mg の服用をすぐに中止した人は、心臓発作や死亡のリスクが高くなります。出血のためにプラビックスを中止しなければならない場合、心臓発作のリスクが高くなる可能性があります。
プラビックス75mgとは?
プラビックスは、次のいずれかに該当する人の治療に使用される処方薬です。
- 心臓の問題による胸の痛み
- 足の血行不良(末梢動脈疾患)
- 心臓発作
- ストローク
プラビックスは、単独で、またはアスピリンと併用して、心臓発作、脳卒中、または死に至る可能性のある血栓など、心臓または血管に別の深刻な問題が発生する可能性を減らします.
血小板は、血液が正常に凝固するのを助ける血球です。プラビックス 75mg は、血小板がくっついて動脈を塞ぐ可能性のある血栓を形成するのを防ぎます。
Plavix 75mgが子供に安全で効果的かどうかは不明です.
プラビックス 75mg を服用してはいけない人は?
次の場合はプラビックスを服用しないでください。
- 現在、胃潰瘍などの出血を引き起こす状態にある
- クロピドグレルまたはプラビックスの他の成分にアレルギーがある. Plavix の成分の完全なリストについては、このリーフレットの最後を参照してください。
Plavix 75mgを服用する前に医師に何を伝えるべきですか?
Plavix を服用する前に、次の場合は医師に相談してください。
- 腸(胃腸)または胃潰瘍の病歴がある
- 出血の問題の歴史がある
- 手術または歯科治療を受ける予定。見る 「プラビックスはどのように服用すればよいですか?」
- 妊娠している、または妊娠する予定がある。 Plavix 75mgが胎児に害を及ぼすかどうかは不明です
- 授乳中または授乳を計画している。 Plavix 75mg が母乳に移行するかどうかは不明です。プラビックスの継続が必要な場合は、授乳を避けるか中止するか、医療機関と相談して決定する必要があります。
- あなたの病気を治療するために使用される薬に対してアレルギーまたは反応があった。
プラビックスを服用していることをすべての医師と歯科医に伝えてください。手術や侵襲的処置を受ける前に、プラビックス 75mg を処方した医師に相談する必要があります。
服用しているすべての薬について医師に伝えてください。 処方薬、非処方薬、ビタミン、ハーブサプリメントを含みます。
Plavix 75mg は他の薬の作用に影響を与える可能性があり、他の薬は Plavix の作用に影響を与える可能性があります。見る 「Plavix 75mg について知っておくべき最も重要な情報は何ですか?」
Plavix 75mg は、レパグリニド (Prandin®) などの他の医薬品の血中濃度を上昇させる可能性があります。
プラビックスを他の特定の薬と一緒に服用すると、出血のリスクが高まる可能性があります。
特に次の場合は医師に相談してください。
- 特に脳卒中を起こした場合は、アスピリン。あなたの状態を治療するためにプラビックス75mgと一緒にアスピリンを服用すべきかどうかについては、常に医師に相談してください.
- 非ステロイド系抗炎症薬(NSAID)。よくわからない場合は、医師または薬剤師に NSAID 薬のリストを尋ねてください。
- ワルファリン(Coumadin®、Jantoven®)。
- 選択的セロトニン再取り込み阻害剤 (SSRI) およびセロトニン ノルエピネフリン再取り込み阻害剤 (SNRI)。よくわからない場合は、医師または薬剤師に SSRI または SNRI の薬のリストを尋ねてください。
- リファンピン(重度の感染症の治療に使用)
服用している薬を知る。それらのリストを保管して、新しい薬を入手したときに医師または薬剤師に見せてください。
プラビックスはどのように服用すればよいですか?
- 医師の指示どおりにプラビックスを服用してください。
- 最初に医師に相談せずに、用量を変更したり、Plavix 75mg の服用を中止したりしないでください。 Plavix を中止すると、心臓発作や脳卒中のリスクが高まる可能性があります。
- 医師の指示に従って、アスピリンと一緒にプラビックス 75mg を服用してください。
- 飲み忘れた場合は、気がついたらすぐにプラビックスを服用してください。次の服用時間が近い場合は、飲み忘れた分は飛ばしてください。次の1回量をいつもの時間に服用してください。医師の指示がない限り、プラビックス 75mg を同時に 2 回服用しないでください。
- プラビックスを飲みすぎた場合は、すぐに医師に連絡するか、最寄りの緊急治療室に行ってください。
- 手術を受ける前に、プラビックス 75mg の使用を中止することについて医師に相談してください。医師は、手術中の過度の出血を避けるために、手術を受ける少なくとも5日前にPlavix 75mgの服用を中止するように指示する場合があります.
プラビックスの副作用の可能性は何ですか?
プラビックス 75mg は、次のような重大な副作用を引き起こす可能性があります。
- 「プラビックスについて知っておくべき最も重要な情報は何ですか?」を参照してください。
- 血栓性血小板減少性紫斑病 (TTP) と呼ばれる血液凝固の問題。 TTP は Plavix 75mg で、時には短期間 (2 週間未満) 後に発生する可能性があります。 TTP は、血管内で血栓が形成される血液凝固の問題です。そして体のどこにでも起こります。 TTP は死に至る可能性があるため、すぐに病院で治療する必要があります。これらの症状のいずれかがあり、他の病状では説明できない場合は、すぐに医師の診察を受けてください。
- 皮下出血による皮膚または口内(粘膜)の紫がかった斑点(紫斑と呼ばれる)
- 肌や白目が黄色い(黄疸)
- 疲れている、または弱っている
- あなたの肌はとても青白く見えます
- 熱
- 速い心拍数または息切れ
- 頭痛
- スピーチの変化
- 錯乱
- 昏睡
- 脳卒中
- 発作
- 少量の尿、またはピンク色または血が混じった尿
- 胃部(腹部)の痛み
- 吐き気、嘔吐、または下痢
- ビジョンの変化
- 持続する低血糖症状
気になる副作用や治らない副作用がある場合は、医師に相談してください。プラビックスの服用中に皮膚反応を含むアレルギー反応が発生した場合は、医師に相談してください。
これらはプラビックスの考えられるすべての副作用ではありません。詳細については、医師または薬剤師にお尋ねください。
副作用に関する医学的アドバイスについては、医師に連絡してください。 1-800-FDA-1088 で副作用を FDA に報告できます。
Plavix 75mg の保管方法は?
- Plavix 75mg を 59°F から 86°F (15°C から 30°C) で保管してください。
プラビックスとすべての薬は子供の手の届かないところに保管してください。
プラビックスに関する一般情報
医薬品は、医薬品ガイドに記載されている以外の目的で使用されることがあります。処方されていない状態でプラビックス 75mg を服用しないでください。他の人があなたと同じ症状を持っていても、プラビックスを他の人に与えないでください.それらに害を及ぼす可能性があります。
この投薬ガイドは、プラビックスに関する最も重要な情報をまとめたものです。さらに詳しい情報が必要な場合は、医師に相談してください。医療従事者向けに書かれたプラビックスに関する情報については、医師または薬剤師にお尋ねください。
詳細については、www.sanofi-aventis.us または www.bms.com にアクセスするか、1-800-321-1335 までお電話ください。
Plavix 75mgの成分は何ですか?
有効成分: クロピドグレル重硫酸塩
不活性成分:
錠剤:硬化ヒマシ油、ヒドロキシプロピルセルロース、マンニトール、微結晶セルロース、ポリエチレングリコール6000
フィルムコーティング:酸化第二鉄、ヒプロメロース2910、乳糖一水和物、二酸化チタン、トリアセチン、カルナバワックス
この投薬ガイドは、米国食品医薬品局によって承認されています。
