Nimotop 30mg Nimodipine 使用法、副作用および投与量。 オンライン薬局の価格。 処方箋不要のジェネリック医薬品。
Nimotop 30mg とは何ですか? どのように使用されますか?
Nimotop は、動脈瘤 (くも膜下出血) の症状を治療するために使用される処方薬です。 Nimotop は、単独で使用することも、他の薬と併用することもできます。
Nimotop は、カルシウム チャネル遮断薬と呼ばれる薬物のクラスに属します。神経学、その他;カルシウムチャネルブロッカー、ジヒドロフィリジン。
Nimotop 30mgが子供に安全で効果的かどうかは不明です.
ニモトップで起こりうる副作用は何ですか?
Nimotop は、次のような重大な副作用を引き起こす可能性があります。
- 蕁麻疹、
- 呼吸困難、
- 顔、唇、舌、喉の腫れ、
- 立ちくらみ、
- 速いまたは遅い心拍数、および
- むくみや足首や足
上記の症状がある場合は、すぐに医療機関を受診してください。
ニモトップの最も一般的な副作用は次のとおりです。
- 低血圧(ふらつき感)、
- 吐き気、
- 胃のむかつき、
- 心拍が遅くなり、
- 筋肉痛
気になる副作用や治らない副作用がある場合は、医師に相談してください。
これらは、ニモトップの考えられるすべての副作用ではありません。詳細については、医師または薬剤師にお尋ねください。
副作用に関する医学的アドバイスについては、医師に連絡してください。 1-800-FDA-1088 で副作用を FDA に報告できます。
NIMOTOP (ニモジピン) を静脈内または他の非経口経路で投与しないでください。 NIMOTOP(ニモジピン)カプセルの内容物が非経口的に注射された場合、死亡および重篤な生命を脅かす有害事象が発生しました(警告および用法・用量を参照)。
説明
Nimotop® (ニモジピン) は、カルシウム チャネル遮断薬として知られる薬剤のクラスに属します。ニモジピンは、イソプロピル 2 - メトキシエチル 1, 4 - ジヒドロ - 2, 6 - ジメチル - 4 - (m-ニトロフェニル) - 3, 5 - ピリジンジカルボキシレートです。分子量は 418.5、分子式は C21H26N2O7 です。構造式は次のとおりです。
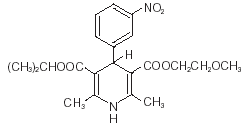
ニモジピンは黄色の結晶性物質で、水にほとんど溶けません。
NIMOTOP® (ニモジピン) カプセルは、経口投与用のソフト ゼラチン カプセルとして処方されます。各液体充填カプセルには、グリセリン、ペパーミント オイル、精製水、およびポリエチレングリコール 400 のビヒクルに 30 mg のニモジピンが含まれています。ソフト ゼラチン カプセル シェルには、ゼラチン、グリセリン、精製水、および二酸化チタンが含まれています。
適応症
Nimotop® (ニモジピン) は、発作後の神経学的状態 (すなわち、ハント アンド ヘス グレード IV) に関係なく、破裂した頭蓋内ベリー動脈瘤によるくも膜下出血患者の虚血性欠損の発生率と重症度を軽減することにより、神経学的転帰を改善することが示されています。
投薬と管理
NIMOTOP (ニモジピン) カプセルを静脈内または他の非経口経路で投与しないでください (警告を参照)。 Nimotop (ニモジピン) が不注意に静脈内投与された場合、臨床的に重大な低血圧には、昇圧剤による心臓血管のサポートが必要になる場合があります。カルシウム チャネル遮断薬の過剰摂取に対する特定の治療法も迅速に実施する必要があります。
Nimotop (ニモジピン) は、クモ膜下出血用に象牙色のソフト ゼラチン 30 mg カプセルの形で経口投与されます。
経口投与量は、4 時間ごとに 60 mg (30 mg カプセル 2 個) を連続 21 日間、できれば食前 1 時間または食後 2 時間以上です。経口 Nimotop® (ニモジピン) 療法は、くも膜下出血の 96 時間以内に開始する必要があります。
手術時などカプセルを飲み込めない場合、または患者が意識を失っている場合は、カプセルの両端に 18 ゲージの針で穴を開け、カプセルの内容物を注射器で抜き取ります。非経口注射器を使用してカプセル内の液体を抽出できますが、液体は常に、針を受け入れることができず、経口または経鼻胃管または PEG を介して投与するように設計された注射器に移す必要があります。投与エラーを最小限に抑えるために、投与に使用する注射器には「Not for IV Use」というラベルを付けることが推奨されます。次に、内容物を患者の胃内チューブに空にし、30 mL の生理食塩水 (0.9%) でチューブを洗い流します。この投与方法の有効性と安全性は、臨床試験で実証されていません。
肝硬変の患者では、クリアランスが大幅に減少し、Cmax が約 2 倍になります。投与量は、血圧と心拍数を注意深く監視しながら、4 時間ごとに 30 mg に減らす必要があります。
供給方法
各アイボリー色のソフトゼラチンNIMOTOP®(ニモジピン)カプセルには、Nimotop 30mgという言葉が刻印されており、30mgのニモジピンが含まれています。 30 mg カプセルは、単位用量のホイル パウチに包装され、100 カプセルを含むカートンで提供されます。この製品は、1 カートンあたり 30 カプセルが入った子供に安全な単位用量安全パック ホイル パウチでも入手できます。カプセルは、製造元のオリジナルのホイル パッケージに入れ、25°C (77°F) で保管する必要があります。
カプセルは、光と凍結から保護する必要があります。
販売元: Bayer Pharmaceuticals Corporation, 400 Morgan Lane, West Haven, CT 06516. 製造元: Catalent Pharma Solutions St. Petersburg, FL 33716. FDA 改訂日: 2006 年 1 月 20 日
副作用
ニモジピンを投与されたクモ膜下出血患者 823 例中 92 例 (11.2%) で有害事象が報告されました。最も頻繁に報告された有害事象は、これらの患者の 4.4% で血圧が低下したことでした。プラセボ治療を受けた患者 479 人中 29 人 (6.1%) も有害な経験を報告しました。 1%を超える頻度で報告されたイベントは、用量別に以下に表示されます。
DOSE q4h 患者数 (%) ニモジピン
0.35 mg/kg q4h、30 mg q4h、または 120 mg q4h を投与された患者によって報告された他の有害な経験はありませんでした。 60 mg q4h 投与群で発生率が 1% 未満の有害な経験は次のとおりです。かゆみ;胃腸出血;血小板減少症;貧血;動悸;嘔吐;フラッシング;発汗;喘鳴;フェニトイン毒性;立ちくらみ;めまい;リバウンド血管痙攣;黄疸;高血圧;血腫。
90 mg q4h 投与群で発生率が 1% 未満の有害事象は次のとおりです。かゆみ、胃腸出血。血小板減少症;神経学的悪化;嘔吐;発汗;うっ血性心不全;低ナトリウム血症;血小板数の減少;播種性血管内凝固症候群;深部静脈血栓症。
表からわかるように、ニモジピンの使用に関連して現れる副作用には、プラセボ対照と比較して高用量または高率での発生率の増加に基づいて、カルシウムチャネル遮断薬の既知の薬理作用である血圧低下、浮腫および頭痛が含まれていました.ただし、SAH にはしばしば意識の変化が伴うため、有害な経験の過少報告につながることに注意する必要があります。他の適応症の臨床試験でニモジピンを投与された患者は、紅潮 (2.1%)、頭痛 (4.1%)、および体液貯留 (0.3%) を報告しました。これは、カルシウム チャネル遮断薬に対する典型的な反応です。カルシウム チャネル遮断薬として、ニモジピンは、影響を受けやすい患者の心不全を悪化させたり、AV 伝導を妨害したりする可能性がありますが、これらのイベントは観察されませんでした。
経口ニモジピンとの因果関係は、血液学的因子、腎機能または肝機能、または炭水化物代謝に対する臨床的に有意な影響ではありません。非絶食時の血清グルコース値の上昇 (0.8%)、LDH 値の上昇 (0.4%)、血小板数の減少 (0.3%)、アルカリホスファターゼ値の上昇 (0.2%)、および SGPT 値の上昇 (0.2%) が報告されています。めったに。

薬物乱用と依存
Nimotop® (ニモジピン) による薬物乱用または依存の事例は報告されていません。
薬物相互作用
Nimotop® (ニモジピン) を追加することで、他のカルシウム チャネル遮断薬の心血管作用が強化される可能性があります。
ヨーロッパでは、Nimotop® (ニモジピン) が、高血圧患者が同時に服用した降圧化合物の効果を時折強化することが観察されました。この現象は、北米の臨床試験では観察されませんでした。
人の健康なボランティアを対象とした研究では、シメチジン 1,000 mg/日とニモジピン 90 mg/日を 1 週間服用した後、平均ピーク ニモジピン血漿濃度が 50% 増加し、平均曲線下面積が 90% 増加したことが示されました。 .この効果は、ニモジピンの初回通過代謝を減少させる可能性がある、シメチジンによる肝臓チトクローム P-450 の既知の阻害によって媒介される可能性があります。
警告
不注意による静脈内投与による死亡: NIMOTOP (ニモジピン) を静脈内または他の非経口経路で投与しないでください。 NIMOTOP(ニモジピン)カプセルの内容物が非経口的に注射された場合、死亡および重篤な生命を脅かす有害事象(心停止、心血管虚脱、低血圧、および徐脈を含む)が発生しました(用量および投与法を参照)。
予防
全般的: 血圧: ニモジピンには、カルシウム チャネル遮断薬に期待される血行動態効果がありますが、一般的には顕著ではありません。しかし、ニモトップ(ニモジピン)カプセルの内容物の静脈内投与は、死亡、心停止、心血管虚脱、低血圧、徐脈などの深刻な悪影響をもたらしました。臨床研究で Nimotop® (ニモジピン) を投与されたくも膜下出血患者では、約 5% が血圧の低下を示し、約 1% がこのために研究をやめたと報告されています (すべてがニモジピンに起因するわけではありません)。それにもかかわらず、既知の薬理学とカルシウムチャネル遮断薬の既知の効果に基づいて、Nimotop® (ニモジピン) による治療中は血圧を注意深く監視する必要があります。 (見る 警告 と 投薬と管理 )
肝疾患: Nimotop® (ニモジピン) の代謝は、肝機能障害のある患者では低下します。そのような患者は、血圧と脈拍数を綿密に監視し、低用量を投与する必要があります( 投薬と管理 )。
ニモジピンで治療された患者では、腸の仮性閉塞およびイレウスがまれに報告されています。因果関係は確立されていません。条件は、保守的な管理に対応しています。
実験室試験の相互作用: 知られていない。
発がん、突然変異誘発、生殖能力の障害: 年間の研究で、1800 ppm のニモジピン (91 ~ 121 mg/kg/日ニモジピンに相当) を含む食事を与えられたラットでは、プラセボ コントロールよりも子宮の腺癌および精巣のライディッヒ細胞腺腫の発生率が高いことが観察されました。 .しかし、その差は統計的に有意ではなく、より高い発生率は、Wistar 株のこれらの腫瘍の歴史的管理範囲内に十分収まっていました。
ニモジピンは 91 週間のマウス研究で発がん性がないことが判明しましたが、飼料中 1800 ppm ニモジピンの高用量 (546 ~ 774 mg/kg/日) は動物の平均余命を短縮しました.エイムス試験、小核試験、優性致死試験を含む変異原性試験は陰性であった。ニモジピンは、オスでは 10 週間以上、メスでは交配前に 3 週間以上、毎日 30 mg/kg/日まで経口投与された後、オスとメスの Wistar ラットの受胎能と一般的な生殖能力を損なわず、継続して投与されました。妊娠7日目まで。ラットにおけるこの用量は、50 kg の患者における 60 mg q4h の同等の臨床用量の約 4 倍です。
妊娠: 妊娠カテゴリー C. ニモジピンは、ヒマラヤウサギで催奇形作用があることが示されています。奇形および発育不全の胎児の発生率は、妊娠 6 日目から 18 日目までの 1 および 10 mg/kg/日の経口投与 (強制経口投与による) で増加したが、2 つの同一のウサギ研究の 1 つで 3.0 mg/kg/日では増加しなかった. 2 番目の研究では発育阻害胎児の発生率の増加が 1.0 mg/kg/日で見られましたが、それ以上の用量では見られませんでした。ニモジピンは胎生毒性があり、妊娠 6 日から 15 日まで 100 mg/kg/日を強制経口投与された Long Evans ラットにおいて、胎児の再吸収および発育不全を引き起こした。他の 2 つのラット研究では、妊娠 16 日から 30 mg/kg/日のニモジピンを胃管強制経口投与し、屠殺 (妊娠 20 日または産後 21 日) するまで続けた場合、骨格変異、発育不全の胎児、および死産ですが、奇形はありません。妊娠中の女性を対象として、ヒト胎児への影響を直接評価するための十分に管理された研究はありません。ニモジピンは、潜在的な利益が胎児への潜在的なリスクを正当化する場合にのみ、妊娠中に使用する必要があります。
授乳中の母親: ニモジピンおよび/またはその代謝物は、母体の血漿よりもはるかに高い濃度でラットのミルクに現れることが示されています.薬剤が母乳中に排泄されるかどうかは不明です。多くの薬物は母乳中に排泄されるため、授乳中の母親は、薬物を服用している間は赤ちゃんに母乳を与えないようにアドバイスされています.
小児科の使用: 小児における安全性と有効性は確立されていません。
高齢者の使用: ニモジピンの臨床試験では、65 歳以上の被験者が若い被験者と異なる反応を示すかどうかを判断するのに十分な数の被験者が含まれていませんでした。他の報告された臨床経験では、年配の患者と若い患者の間の反応の違いは確認されていません。一般に、高齢患者への投与は慎重に行う必要があります。これは、肝臓、腎臓または心機能の低下、および付随する疾患または他の薬物療法の頻度が高いことを反映しています。
過剰摂取
Nimotop® (ニモジピン) の経口投与による過剰摂取の報告はありません。過剰摂取の症状は、顕著な全身性低血圧を伴う過剰な末梢血管拡張などの心血管系への影響に関連していると予想されます. Nimotop® (ニモジピン) の過剰摂取による臨床的に重大な低血圧には、昇圧剤による積極的な心血管サポートが必要な場合があります。カルシウム チャネル遮断薬の過剰摂取に対する特定の治療法も迅速に実施する必要があります。 Nimotop® (ニモジピン) はタンパク質結合性が高いため、透析はあまり役に立ちません。
禁忌
知られていない。
臨床薬理学
作用機序: ニモジピンはカルシウムチャネル遮断薬です。平滑筋細胞の収縮過程はカルシウムイオンに依存しており、カルシウムイオンは脱分極中に遅いイオン膜貫通電流としてこれらの細胞に入ります。ニモジピンは、これらの細胞へのカルシウムイオンの移動を阻害し、血管平滑筋の収縮を阻害します。動物実験では、ニモジピンは体の他の部分の動脈よりも脳動脈に大きな影響を与えました。これはおそらく、親油性が高く、血液脳関門を通過できるためです。ニモジピン治療を受けたクモ膜下出血 (SAH) 患者の脳脊髄液で、12.5 ng/mL もの高濃度のニモジピンが検出されました。ヒトにおけるニモジピンの正確な作用機序は不明です。以下に説明する臨床研究は、SAH 後の脳血管痙攣によって引き起こされる神経障害の重症度に対するニモジピンの好ましい効果を示していますが、ニモジピンがこれらの動脈の痙攣を予防または緩和するという動脈学的証拠はありません。しかし、利用された動脈造影法が血管痙攣に対する臨床的に意味のある効果を検出するのに適切であったかどうかは不明です。
薬物動態と代謝: ヒトでは、ニモジピンは経口投与後急速に吸収され、一般に 1 時間以内に最高濃度に達します。最終排出半減期は約 8 ~ 9 時間ですが、初期の排出率ははるかに速く、1 ~ 2 時間の半減期に相当します。その結果、頻繁に (4 時間ごとに) 投薬する必要があります。ニモジピンを 1 日 3 回、7 日間投与した場合、蓄積の兆候はありませんでした。ニモジピンは 95% 以上が血漿タンパク質に結合しています。結合は、10 ng/mL から 10 µg/mL の範囲で濃度に依存しませんでした。ニモジピンはほとんど代謝物の形で排泄され、未変化の薬物として尿中に回収されるのは 1% 未満です。すべてが不活性であるか、親化合物よりもかなり活性が低い、多数の代謝物が同定されています。初回通過代謝が高いため、経口投与後のニモジピンのバイオアベイラビリティは平均 13% です。肝硬変の患者ではバイオアベイラビリティが大幅に増加し、Cmax は正常者の約 2 倍であり、このグループの患者では用量を下げる必要があります ( 投薬と管理 )。 24 人の健康な男性ボランティアを対象とした研究では、標準的な朝食後にニモジピン カプセルを投与すると、絶食状態での投与に比べてピーク血漿濃度が 68% 低下し、バイオアベイラビリティが 38% 低下しました。
24 人の高齢者 (59 ~ 79 歳) と 24 人の若年者 (22 ~ 40 歳) が参加した単一の並行群間研究では、ニモジピンの観察された AUC と Cmax は、若年者の研究と比較して高齢者集団で約 2 倍高かった経口投与後の被験者(30mgの単回投与として与えられ、30mgを1日3回で6日間定常状態に投与)。しかし、これらの年齢に関連した薬物動態の違いに対する臨床反応は、有意であるとは見なされませんでした。 (見る 予防 高齢者用)
臨床試験: ニモジピンは、4 つのランダム化二重盲検プラセボ対照試験で、最近クモ膜下出血 (SAH) を起こした患者の血管痙攣に起因する神経障害の重症度を軽減することが示されています。試験では、4 時間ごとに 20 ~ 30 mg から 90 mg の範囲の用量が使用され、3 つの試験では 21 日間、他の試験では少なくとも 18 日間、薬物が投与されました。 4 つの試験のうち 3 つでは、患者を 3 ~ 6 か月間追跡しました。試験のうちの 3 件は比較的良好な患者を対象としており、すべてまたは大部分の患者がハント アンド ヘス グレード I ~ III (最初の出血後に局所欠損が本質的にない) の患者を対象としており、4 番目の試験はハント アンド ヘス グレード III ~ V のかなり病状の患者を対象としていた。 、1 つは米国、1 つはフランスで、設計が類似しており、比較的障害のない SAH 患者がニモジピンまたはプラセボに無作為に割り付けられました。それぞれにおいて、遅発性赤字がけいれんまたは他の原因によるものかどうかについて判断が下され、赤字が等級付けされました。どちらの研究でも、ニモジピン群ではけいれんによる重篤な障害が有意に少ないことが示されました。 2番目の(フランスの)研究では、すべての重症度のけいれん関連の障害が少ないことが示されました.けいれんに関係のない赤字には効果が見られませんでした。
つ目の大規模な研究は、英国ですべての重症度の SAH 患者を対象に実施されました (ただし、89% はグレード I ~ III でした)。ニモジピンは 4 時間ごとに 60mg 投与されました。結果は、けいれんに関連するかどうかは定義されませんでしたが、3か月で、全体的な梗塞率が大幅に低下し、神経学的結果が重度に無効になりました。
カナダの研究では、死亡率と障害の割合が高く、4 時間ごとに 90 mg の用量を使用していた、より重症の患者 (ハントとヘスのグレード III-V) が入力されましたが、それ以外は最初の 2 つの研究と同様でした。その多くがけいれんに起因する遅発性虚血障害の分析では、けいれん関連の障害が大幅に減少したことが示されました。分析された患者(ニモジピン 72 例、プラセボ 82 例)には、以下のアウトカムがありました。
カナダと英国の研究のデータを組み合わせると、ハント アンド ヘス グレード IV または V の Glasgow Outcome Scale での成功率 (つまり、良好な回復) の治療差は 25.3% (ニモジピン) 対 10.9% (プラセボ) でした。下の表は、ニモジピンが、発作後の神経学的状態が悪い SAH 患者の良好な回復を改善する傾向があることを示しています。
30、60、および 90 mg の用量を比較した用量範囲研究では、けいれん関連の神経障害の発生率は一般的に低いことがわかりましたが、用量反応関係はありませんでした。
患者情報
情報が提供されていません。を参照してください。 警告 と 予防 セクション。
