Cartia XT 180mg 使用法、副作用および投与量。 オンライン薬局の価格。 処方箋不要のジェネリック医薬品。
カルティアとは何ですか? どのように使用されますか?
Cartia は、胸痛 (狭心症)、高血圧 (高血圧)、発作性上室性頻脈および心房細動 (フラッター) の症状を治療するために使用される処方薬です。カルティアは、単独で使用することも、他の薬と併用することもできます。
Cartia は、抗不整脈 IV と呼ばれるクラスの薬に属しています。カルシウム チャネル遮断薬;カルシウム チャネル ブロッカー、非ジヒドロピリジン。
カルティアの副作用にはどのようなものがありますか?
カルティアは、次のような重大な副作用を引き起こす可能性があります。
- 胸痛、
- 遅い心拍、
- ドキドキする心臓の鼓動、
- 胸の中でときめき、
- 立ちくらみ、
- 腫れ、
- 急激な体重増加、
- 呼吸困難、
- 熱、
- 喉の痛み、
- 燃える目、
- 皮膚の痛みと
- 水ぶくれとはがれを伴う赤または紫の皮膚発疹
上記の症状がある場合は、すぐに医療機関を受診してください。
カルティアの最も一般的な副作用は次のとおりです。
- 軽い頭痛、
- 軽度のめまい、および
- かぜの諸症状(鼻づまり、くしゃみ、のどの痛み)
気になる副作用や治らない副作用がある場合は、医師に相談してください。
これらはカルティアの副作用のすべてではありません。詳細については、医師または薬剤師にお尋ねください。
副作用に関する医学的アドバイスについては、医師に連絡してください。 1-800-FDA-1088 で副作用を FDA に報告できます。
説明
ジルチアゼム塩酸塩は、カルシウムイオン細胞流入阻害剤(スローチャネルブロッカーまたはカルシウムアンタゴニスト)です。化学的には、塩酸ジルチアゼムは、1,5-ベンゾチアゼピン-4(5H)オン,3-(アセチルオキシ)-5-[2-(ジメチルアミノ)エチル]-2,3-ジヒドロ-2-(4-メトキシフェニル)-一塩酸塩です。 ,(+)-cis-.化学構造は次のとおりです。
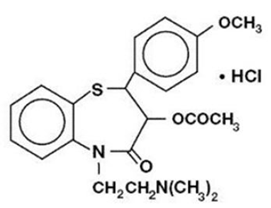
ジルチアゼム塩酸塩は、苦味のある白色からオフホワイトの結晶性粉末です。水、メタノール、クロロホルムに溶けます。分子量は 450.98 です。塩酸ジルチアゼム持続放出カプセル(1日1回投与量)は、120mg、180mg、240mg、または300mgのジルチアゼム塩酸塩を含む1日1回持続放出カプセルとして処方されます。
さらに、各カプセルには次の不活性成分が含まれています: クエン酸アセチルトリブチル、アンモニオメタクリレート コポリマー-NF、D & C レッド #28、D & C イエロー #10、D & C イエロー #10 アルミニウム レーキ、エチルセルロース、FD & C ブルー #1アルミレーキ、FD&Cブルー#2 アルミレーキ、FD&Cレッド#40、FD&Cレッド#40 アルミレーキ、ゼラチン-NF、ステアリン酸マグネシウム、メタクリル酸コポリマー-NF、プロピレングリコール、ポリソルベート80-NF、デンプン、スクロース、タルク USP、および二酸化チタン。 180mgと240mgのカプセルには黄酸化鉄が含まれています。さらに、240mgのカプセルには黒酸化鉄と赤酸化鉄も含まれています。
経口投与用。
この薬は、USP Drug Release 9 を満たしています。
適応症
ジルチアゼム塩酸塩持続放出カプセル USP (1 日 1 回投与) は、高血圧の治療に適応されます。単独で使用することも、他の降圧薬と組み合わせて使用することもできます。
ジルチアゼム塩酸塩持続放出カプセル USP (1 日 1 回投与) は、慢性安定狭心症および冠動脈痙攣による狭心症の管理に適応されます。
投薬と管理
ジルチアゼム単独または他の薬剤との併用で管理されている患者は、最も近い同等の 1 日総用量で塩酸ジルチアゼム持続放出カプセル USP (1 日 1 回投与) に切り替えることができます。一部の患者では、より高用量の塩酸ジルチアゼム持続放出カプセル USP (1 日 1 回投与) が必要になる場合があります。患者を注意深く監視する必要があります。より高いまたはより低い用量へのその後の漸増が必要な場合があり、臨床的に保証されている場合は開始する必要があります。 360mgを超える用量での一般的な臨床経験は限られていますが、臨床試験では540mgまでの用量が研究されています.副作用の発生率は用量が増加するにつれて増加し、第 1 度房室ブロック、めまい、および洞性徐脈が用量と最も強い関係を示します。
高血圧症
投与量は、個々の患者のニーズに合わせて滴定によって調整する必要があります。単剤療法として使用する場合、合理的な開始用量は 1 日 1 回 180 ~ 240 mg ですが、一部の患者はより低い用量で反応する場合があります。最大の降圧効果は、通常、14 日間の慢性治療で観察されます。したがって、投与量の調整はそれに応じてスケジュールする必要があります。臨床試験で研究された通常の投与量範囲は、1 日 1 回 240 ~ 360 mg でした。個々の患者は、1 日 1 回 480 mg までの高用量で反応する可能性があります。
狭心症
狭心症の治療のための投与量は、1 日 1 回 120 または 180 mg の投与量から始めて、各患者のニーズに合わせて調整する必要があります。個々の患者は、1 日 1 回 480 mg までの高用量で反応する可能性があります。必要に応じて、滴定は 7 ~ 14 日間かけて行うことができます。
塩酸ジルチアゼム徐放性カプセルUSP(1日1回投与)
他の心血管薬との併用
供給方法
注: 製品には臭いがある場合があります。
保管条件
20° ~ 25°C (68° ~ 77°F) で保管してください [ USP制御の室温 ]。
過度の湿気を避けてください。
USP で定義されている密閉型の耐光性容器に分注してください。
製造元: Actavis Laboratories FL, Inc., Fort Lauderdale, FL 33314 USA.販売元: Actavis Pharma, Inc., Parsippany, NJ 07054 USA.改訂: 2014 年 12 月
副作用
これまでに実施された研究では重篤な副作用はまれでしたが、心室機能障害や心臓伝導異常のある患者は通常、これらの研究から除外されてきたことを認識しておく必要があります。
次の表は、プラセボ対照の狭心症および高血圧試験で報告された最も一般的な副作用を示しています。比較のために示されているプラセボ患者の率と、最大 360 mg のジルチアゼム塩酸塩持続放出カプセル (1 日 1 回投与) を投与された患者が対象です。
ジルチアゼム塩酸塩持続放出カプセル(1日1回) プラセボ対照狭心症および高血圧試験の併用
3200 人以上の患者を対象とした塩酸ジルチアゼム徐放性カプセル (1 日 1 回投与)、塩酸ジルチアゼム錠剤、および塩酸ジルチアゼム徐放性カプセルの臨床試験で、最も一般的な事象 (すなわち、1% 以上) は浮腫 (4.6%) でした。 、頭痛 (4.6%)、めまい (3.5%)、無力症 (2.6%)、第 1 度房室ブロック (2.4%)、徐脈 (1.7%)、紅潮 (1.4%)、吐き気 (1.4%)、および発疹 ( 1.2%)。
さらに、以下のイベントは、狭心症または高血圧の試験でまれに (1% 未満) 報告されました。
心臓血管: 狭心症、不整脈、房室ブロック (2 度または 3 度)、脚ブロック、うっ血性心不全、心電図異常、低血圧、動悸、失神、頻脈、心室性期外収縮。
神経系: 異常な夢、記憶喪失、うつ病、歩行異常、幻覚、不眠症、神経過敏、感覚異常、人格変化、傾眠、耳鳴り、振戦。
胃腸: 食欲不振、便秘、下痢、口渇、味覚障害、消化不良、SGOT、SGPT、LDH、およびアルカリホスファターゼの軽度の上昇( 警告 、 急性肝障害 )、喉の渇き、嘔吐、体重増加。
皮膚科: 点状出血、光線過敏症、かゆみ、蕁麻疹。
他の: 弱視、CPK 増加、呼吸困難、鼻出血、眼刺激、高血糖、高尿酸血症、インポテンツ、筋肉痙攣、鼻づまり、夜間頻尿、骨関節痛、多尿、性的困難。
ジルチアゼムを投与された患者では、以下の市販後事象がまれに報告されています: 急性全身性発疹性膿疱症、アレルギー反応、脱毛症、血管性浮腫 (顔面または眼窩周囲の浮腫を含む)、心静止、多形性紅斑 (スティーブンス・ジョンソン症候群、中毒性表皮壊死融解症を含む)、剥脱性皮膚炎、錐体外路症状、歯肉過形成、溶血性貧血、出血時間の増加、白血球減少症、光線過敏症(苔癬様角化症および日光にさらされた皮膚領域の色素沈着過剰を含む)、紫斑病、網膜症、ミオパチー、および血小板減少症.さらに、これらの患者の疾患の自然経過と容易に区別できない心筋梗塞などの事象が観察されている。白血球破砕性血管炎として特徴付けられるいくつかの全身性発疹の多くの十分に文書化された症例が報告されています.ただし、これらのイベントとジルチアゼム療法との間の決定的な因果関係はまだ確立されていません。
疑わしい有害反応を報告するには、Actavis (1-800-272-5525) または FDA (1-800-FDA-1088) または www.fda.gov/medwatch に連絡してください。
薬物相互作用
相加効果の可能性があるため、ジルチアゼムを心臓の収縮および/または伝導に影響を与えることが知られている他の薬剤と併用している患者には、注意と慎重な用量調節が必要です ( 警告 )。薬理学的研究は、ジルチアゼムと併用してベータ遮断薬またはジギタリスを使用すると、房室伝導の延長に相加効果がある可能性があることを示しています。 警告 )。
すべての薬と同様に、複数の薬を服用している患者を治療する場合は注意が必要です。ジルチアゼムは、シトクロム P-450 3A4 酵素系の基質であり、阻害剤でもあります。この酵素系の特定の基質、阻害剤、または誘導剤である他の薬物は、ジルチアゼムの有効性と副作用プロファイルに大きな影響を与える可能性があります。 CYP450 3A4 の基質である他の薬剤を服用している患者、特に腎臓および/または肝臓に障害のある患者は、最適な治療血中濃度を維持するために、ジルチアゼムの同時投与を開始または中止する際に用量調節が必要になる場合があります。
麻酔薬
心臓の収縮性、伝導性、および自動性の低下、ならびに麻酔薬に関連する血管拡張は、カルシウム チャネル遮断薬によって増強される可能性があります。併用する場合は、麻酔薬とカルシウム遮断薬を慎重に滴定する必要があります。
ベンゾジアゼピン
研究では、ジルチアゼムは、プラセボと比較して、ミダゾラムとトリアゾラムの AUC を 3 ~ 4 倍、Cmax を 2 倍増加させることが示されました。ミダゾラムとトリアゾラムの消失半減期も、ジルチアゼムとの同時投与中に増加しました (1.5 ~ 2.5 倍)。ジルチアゼムの同時投与中に見られるこれらの薬物動態効果は、ミダゾラムとトリアゾラムの両方の臨床効果の増加(例えば、鎮静の延長)をもたらす可能性があります。
β遮断薬
管理されたおよび管理されていない国内の研究は、ジルチアゼムとベータブロッカーの併用は通常十分に許容されることを示唆していますが、利用可能なデータは、左心室機能障害または心臓伝導異常のある患者における併用治療の効果を予測するには不十分です.
プロプラノロールと同時にジルチアゼム塩酸塩を 5 人の正常なボランティアに投与すると、すべての被験者でプロプラノロール レベルが増加し、プロプラノロールのバイオアベイラビリティが約 50% 増加しました。インビトロでは、プロプラノロールはジルチアゼムによってその結合部位から置換されたように見える。プロプラノロールとの併用療法が開始または中止された場合、プロプラノロールの投与量の調整が必要になる場合があります (以下を参照)。 警告 )。
ブスピロン
9 人の健康な被験者において、ジルチアゼムは、プラセボと比較して平均ブスピロン AUC を 5.5 倍、Cmax を 4.1 倍有意に増加させました。ブスピロンの T½ および Tmax は、ジルチアゼムによって有意な影響を受けませんでした。ブスピロンの効果の増強と毒性の増加は、ジルチアゼムとの併用投与中に可能性があります。その後の用量調整は、同時投与中に必要になる場合があり、臨床評価に基づく必要があります。
カルバマゼピン
ジルチアゼムとカルバマゼピンの併用投与により、カルバマゼピンの血清レベルが上昇し (40% から 72% 増加)、場合によっては毒性が生じることが報告されています。これらの薬を同時に投与されている患者は、潜在的な薬物相互作用について監視する必要があります。
シメチジン
6 人の健康なボランティアを対象とした研究では、1 日あたり 1200 mg のシメチジンを 1 週間服用し、1 回の用量のジルチアゼム60mg。ラニチジンは、より小さく、有意でない増加をもたらしました。この効果は、ジルチアゼムの初回通過代謝に関与する酵素系である肝臓シトクロム P-450 に対するシメチジンの既知の阻害によって媒介される可能性があります。現在ジルチアゼム療法を受けている患者は、シメチジン療法の開始時および中止時に薬理学的効果の変化について注意深く監視する必要があります。ジルチアゼムの投与量の調整が必要な場合があります。
クロニジン
ジルチアゼムとクロニジンの同時使用に関連して、入院およびペースメーカー挿入をもたらす洞性徐脈が報告されている。ジルチアゼムとクロニジンを併用している患者の心拍数を監視します。
シクロスポリン
ジルチアゼムとシクロスポリンの間の薬物動態学的相互作用は、腎臓および心臓移植患者を対象とした研究中に観察されています。腎臓および心臓移植レシピエントでは、ジルチアゼムの添加前と同様のシクロスポリントラフ濃度を維持するために、シクロスポリン用量を 15% から 48% まで減らす必要がありました。これらの薬剤を同時に投与する場合、特にジルチアゼム療法を開始、調整、または中止する場合は、シクロスポリン濃度を監視する必要があります。
ジルチアゼムの血漿中濃度に対するシクロスポリンの効果は評価されていません。
ジギタリス
24 人の健康な男性被験者にジルチアゼムとジゴキシンを投与すると、血漿ジゴキシン濃度が約 20% 増加しました。別の研究者は、冠動脈疾患の患者 12 人でジゴキシンのレベルが上昇していないことを発見しました。ジゴキシンレベルの効果に関して矛盾する結果があったため、ジルチアゼム療法を開始、調整、および中止する際には、ジゴキシンレベルを監視して、過剰または過小デジタル化を回避することをお勧めします。 警告 )。
キニジン
ジルチアゼムは、キニジンの AUC(0-→) を 51%、T½ を 36% 大幅に増加させ、CL 経口を 33% 減少させます。キニジンの副作用の監視が必要であり、それに応じて用量を調整する必要があります。
リファンピン
リファンピンとジルチアゼムの同時投与により、ジルチアゼムの血漿中濃度が検出不可能なレベルまで低下しました。ジルチアゼムとリファンピンまたは既知の CYP3A4 誘導剤との同時投与は可能な限り避け、代替療法を検討する必要があります。
スタチン
ジルチアゼムは CYP3A4 の阻害剤であり、一部のスタチンの AUC を大幅に増加させることが示されています。 CYP3A4 によって代謝されるスタチンによるミオパシーおよび横紋筋融解症のリスクは、ジルチアゼムの併用によって増加する可能性があります。可能であれば、非 CYP3A4 代謝スタチンをジルチアゼムと一緒に使用してください。それ以外の場合は、ジルチアゼムとスタチンの両方の用量調整を検討し、スタチン関連の有害事象の徴候と症状を注意深く監視する必要があります。
健康なボランティアのクロスオーバー研究 (N=10) では、120 mg BID のジルチアゼム SR と 14 日間のレジメンの最後に 20 mg のシンバスタチンを 1 回投与すると、シンバスタチンと比較して平均シンバスタチン AUC が 5 倍増加しました。 1人。ジルチアゼムの定常状態での平均暴露量が増加した被験者は、シンバスタチン暴露量の倍数増加を示しました。コンピューターに基づくシミュレーションでは、ジルチアゼム 480 mg の 1 日用量で、シンバスタチン AUC の平均 8 ~ 9 倍の増加が期待できることが示されました。シンバスタチンとジルチアゼムの同時投与が必要な場合は、シンバスタチンの 1 日量を 10 mg に、ジルチアゼムを 240 mg に制限します。
10 人の無作為化非盲検 4 方向クロスオーバー研究では、ロバスタチン 20 mg 単回投与とジルチアゼム (120 mg BID ジルチアゼム SR を 2 週間) を同時投与すると、平均値が 3 ~ 4 倍増加しました。ロバスタチン AUC およびロバスタチン単独との比較。同じ研究では、プラバスタチン 20 mg 単回投与の AUC とジルチアゼムの同時投与中に有意な変化はありませんでした。ジルチアゼムの血漿レベルは、ロバスタチンまたはプラバスタチンによって有意に影響を受けませんでした。
警告
心臓伝導
ジルチアゼムは、洞不全症候群の患者を除いて、洞結節の回復時間を大幅に延長することなく房室結節の不応期を延長します。この影響により、まれに心拍数が異常に遅くなったり (特に洞不全症候群の患者で)、第 2 度または第 3 度房室ブロック (患者 3,290 人中 13 人または 0.40%) が発生したりすることがあります。ジルチアゼムとベータ遮断薬またはジギタリスを併用すると、心臓伝導に相加効果が生じる可能性があります。プリンツメタル狭心症の患者は、60 mg のジルチアゼムを単回投与した後、心静止期 (2 ~ 5 秒) を発症しました。 有害反応 )。
うっ血性心不全
ジルチアゼムは、単離された動物組織標本において負の変力作用を有するが、正常な心室機能を有するヒトにおける血行力学的研究は、心係数の減少も収縮性(dp/dt)に対する一貫した負の影響も示さなかった。心室機能障害 (駆出率 24% ± 6%) の患者における経口ジルチアゼムの急性試験では、収縮機能 (dp/dt) の有意な低下を伴わずに心室機能指数の改善が示されました。うっ血性心不全の悪化は、心室機能の既存の障害を持つ患者で報告されています。心室機能障害のある患者にベータ遮断薬と併用してジルチアゼム塩酸塩を使用した経験は限られています。この組み合わせを使用する場合は注意が必要です。
低血圧
ジルチアゼム療法に伴う血圧の低下は、時として症候性低血圧を引き起こすことがあります。
急性肝障害
臨床研究では、アルカリホスファターゼとビリルビンの上昇を伴う、または伴わないトランスアミナーゼの軽度の上昇が観察されています。このような上昇は通常一過性であり、ジルチアゼム治療を継続してもしばしば解消されます。まれに、アルカリホスファターゼ、LDH、SGOT、SGPT などの酵素の有意な上昇、および急性肝障害と一致するその他の現象が認められています。これらの反応は、治療開始後早期 (1 ~ 8 週間) に発生する傾向があり、薬物治療を中止すると元に戻ります。ジルチアゼムとの関係は、場合によっては不確かですが、可能性が高い場合もあります ( 予防 )。
予防
全般的
ジルチアゼム塩酸塩は、肝臓で広範囲に代謝され、腎臓と胆汁に排泄されます。長期間にわたって投与される他の薬物と同様に、腎機能と肝機能の検査パラメータを定期的に監視する必要があります。腎機能や肝機能が低下している患者には、慎重に使用する必要があります。毒性を引き起こすように設計された亜急性および慢性の犬とラットの研究では、高用量のジルチアゼムは肝臓の損傷と関連していました.特別な亜急性肝臓研究では、ラットでの 125 mg/kg 以上の経口投与は肝臓の組織学的変化と関連しており、この変化は薬物を中止すると元に戻りました。イヌでは、20 mg/kg の用量でも肝臓の変化が見られました。ただし、これらの変化は、継続的な投与により可逆的でした。
皮膚科のイベント(参照 有害反応 は一過性であり、ジルチアゼムの継続使用にもかかわらず消失する場合があります。ただし、多形紅斑および/または剥脱性皮膚炎に進行する皮膚発疹もまれに報告されています。皮膚反応が持続する場合は、薬剤の使用を中止する必要があります。
発がん、突然変異誘発、生殖能力の障害
100 mg/kg/日までの経口投与レベルでのラットでの 24 か月の研究、および 30 mg/kg/日までの経口投与レベルでのマウスでの 21 か月の研究では、発がん性の証拠は示されませんでした。また、in vitro または in vivo の哺乳動物細胞アッセイ、in vitro のバクテリアでも変異原性は認められませんでした。 100mg/kg/日までの経口投与量で雄と雌のラットで行われた研究では、受精能障害の証拠は観察されませんでした。
妊娠
カテゴリーC. マウス、ラット、およびウサギで生殖試験が実施されています。毎日の推奨治療用量の 5 倍から 10 倍 (mg/kg 基準) の範囲の用量を投与すると、胚および胎児の致死率が生じます。これらの用量は、いくつかの研究で、骨格異常を引き起こすことが報告されています.周産期/出生後の研究では、ヒト用量の 20 倍以上の用量で死産の発生率が増加しました。
妊婦を対象とした十分に管理された研究はありません。したがって、潜在的な利益が胎児への潜在的なリスクを正当化する場合にのみ、妊婦にジルチアゼムを使用してください。
授乳中の母親
ジルチアゼムは母乳中に排泄されます。ある報告では、母乳中の濃度が血清レベルに近似している可能性があることを示唆しています。ジルチアゼムの使用が不可欠であると判断された場合は、代替の乳児栄養法を導入する必要があります。
小児用
小児患者における安全性と有効性は確立されていません。
高齢者の使用
ジルチアゼムの臨床試験には、65 歳以上の被験者が若い被験者と異なる反応を示すかどうかを判断するのに十分な数の被験者が含まれていませんでした。他の報告された臨床経験では、年配の患者と若い患者の間の反応の違いは確認されていません。一般に、高齢患者の用量選択は慎重に行う必要があり、通常は用量範囲の下限から開始します。これは、肝臓、腎臓、または心機能の低下、および付随する疾患または他の薬物療法の頻度が高いことを反映しています。
過剰摂取
マウスおよびラットにおける経口 LD50 は、それぞれ 415 ~ 740 mg/kg および 560 ~ 810 mg/kg の範囲です。これらの種の静脈内 LD50 は、それぞれ 60 および 38 mg/kg でした。イヌの経口 LD50 は 50 mg/kg を超えると考えられていますが、サルでは 360 mg/kg で致死が見られました。
人間の毒性量は知られていません。広範な代謝のために、ジルチアゼムの標準用量の後の血中レベルは10倍以上変動する可能性があり、過剰摂取の場合の血中レベルの有用性が制限されます.
ジルチアゼムの過剰摂取後に観察された事象には、徐脈、低血圧、心臓ブロック、および心不全が含まれていました。過剰摂取のほとんどの報告は、何らかの支持的な医学的措置および/または薬物治療を説明しています。徐脈は、心臓ブロックと同様に、アトロピンに好反応を示すことが多かったが、心臓ブロックの治療には心臓ペーシングも頻繁に利用された。血圧を維持するために輸液と昇圧剤が使用され、心不全の場合には強心薬が投与されました。さらに、一部の患者は、換気補助、胃洗浄、活性炭、および/または静脈内カルシウムによる治療を受けました。
ジルチアゼムの過剰摂取の薬理学的効果を逆転させるための静脈内カルシウム投与の有効性には一貫性がありません。いくつかの報告された症例では、最初はアトロピンに抵抗性であった低血圧および徐脈に関連するカルシウムチャネル遮断薬の過剰摂取が、患者が静脈内カルシウムを受けた後、アトロピンにより反応するようになりました.場合によっては、静脈内カルシウムが 5 分かけて投与され(塩化カルシウム 1 g またはグルコン酸カルシウム 3 g)、必要に応じて 10 ~ 20 分ごとに繰り返されます。グルコン酸カルシウムは、1 時間あたり 2 g の速度で 10 時間、持続注入としても投与されています。 24時間以上のカルシウム注入が必要になる場合があります。高カルシウム血症の兆候がないか、患者を監視する必要があります。
過剰摂取または過大な反応が生じた場合、胃腸の汚染除去に加えて、適切な支持手段を採用する必要があります。ジルチアゼムは、腹膜透析または血液透析では除去されないようです。限られたデータは、プラズマフェレーシスまたは木炭血液灌流が、過剰摂取後のジルチアゼムの排出を促進する可能性があることを示唆しています.ジルチアゼムの既知の薬理学的効果および/または報告された臨床経験に基づいて、以下の対策が考慮される場合があります。
徐脈: アトロピン (0.6 ~ 1 mg) を投与します。迷走神経遮断に対する反応がない場合は、慎重にイソプロテレノールを投与してください。
高度AVブロック: 上記の徐脈と同様に扱う。高度固定房室ブロックは、心臓ペーシングで治療する必要があります。
心不全: 強心薬 (イソプロテレノール、ドーパミン、またはドブタミン) と利尿薬を管理します。
低血圧: 昇圧剤(例、ドーパミンまたはノルエピネフリン)。
実際の治療と投与量は、臨床状況の重症度と、担当医の判断と経験に依存する必要があります。
禁忌
ジルチアゼムは、(1)心室ペースメーカーが機能している場合を除き、洞不全症候群の患者、(2)心室ペースメーカーが機能している場合を除き、2度または3度房室ブロックの患者、(3)低血圧(収縮期血圧90mmHg未満)、(4)薬物に対する過敏症を示した患者、および(5)入院時にX線で記録された急性心筋梗塞および肺うっ血のある患者。
臨床薬理学
ジルチアゼム塩酸塩持続放出カプセル USP (1 日 1 回投与) の治療効果は、心臓および血管平滑筋の膜脱分極中のカルシウムイオンの細胞流入を阻害する能力に関連していると考えられています。
作用機序
高血圧症
ジルチアゼム塩酸塩持続放出カプセル USP (1 日 1 回投与) は、主に血管平滑筋の弛緩とその結果としての末梢血管抵抗の減少によって降圧効果をもたらします。血圧低下の大きさは、高血圧の程度に関連しています。したがって、高血圧の人は降圧効果を経験しますが、正常血圧の人では血圧がわずかに低下するだけです。
狭心症
ジルチアゼム塩酸塩徐放性カプセル USP (1 日 1 回投与) は、おそらく心筋酸素要求量を減少させる能力により、運動耐性を高めることが示されています。これは、最大下および最大作業負荷での心拍数と全身血圧の低下によって達成されます。ジルチアゼムは、心外膜および心内膜下の両方の冠動脈の強力な拡張剤であることが示されています。自然発生的およびエルゴノビン誘発性の冠状動脈痙攣は、ジルチアゼムによって阻害されます。
動物モデルでは、ジルチアゼムは興奮性組織の遅い内向き (脱分極) 電流を妨害します。それは、活動電位の構成を変化させることなく、さまざまな心筋組織で興奮と収縮の分離を引き起こします。ジルチアゼムは、負の強心作用をほとんどまたはまったく引き起こさない薬物レベルで、冠血管平滑筋の弛緩および大小両方の冠動脈の拡張をもたらす。結果として生じる冠動脈血流(心外膜および心内膜下)の増加は、虚血モデルおよび非虚血モデルで発生し、全身血圧の用量依存的な低下と末梢抵抗の低下を伴います。
血行動態および電気生理学的効果
他のカルシウム チャネル拮抗薬と同様に、ジルチアゼムは、摘出組織で洞房および房室伝導を減少させ、摘出標本で負の強心作用を示します。無傷の動物では、高用量で AH 間隔の延長が見られます。
人の場合、ジルチアゼムは自発的およびエルゴノビン誘発性の冠状動脈けいれんを防ぎます。正常血圧者の末梢血管抵抗の減少と血圧のわずかな低下を引き起こし、虚血性心疾患患者の運動耐性研究では、任意のワークロードに対する心拍数と血圧の積を低下させます。主に心室機能が良好な患者を対象としたこれまでの研究では、負の強心作用の証拠は明らかにされていません。心拍出量、駆出率、および左心室拡張末期圧は影響を受けていません。このようなデータは、心室機能が低下している患者への影響に関して予測値がなく、心室機能の既存の障害がある患者では心不全の増加が報告されています。心室機能が低下している患者におけるジルチアゼムとベータ遮断薬の相互作用に関するデータはまだほとんどありません。通常、安静時心拍数はジルチアゼムによってわずかに低下します。
高血圧患者では、ジルチアゼム塩酸塩持続放出カプセル USP (1 日 1 回投与) は、仰臥位と立位の両方で降圧効果をもたらします。 1 日 1 回 90 から 540 mg の範囲の用量を利用した二重盲検並行用量反応研究では、ジルチアゼム塩酸塩徐放性カプセル (1 日 1 回投与) は仰臥位拡張期血圧を明らかに直線的に低下させました。研究された用量範囲。プラセボ、90 mg、180 mg、360 mg、および 540 mg のトラフで測定された拡張期血圧の変化は、それぞれ -2.9、-4.5、-6.1、-9.5、および -10.5 mm Hg でした。姿勢性低血圧は、突然直立姿勢をとったときにまれに認められます。反射性頻脈は、慢性的な降圧効果に関連していません。ジルチアゼム塩酸塩持続放出カプセル USP (1 日 1 回投与) は、血管抵抗を減少させ、心拍出量を増加させます (1 回拍出量の増加による)。心拍数がわずかに減少するか、まったく変化しません。動的な運動中、拡張期血圧の上昇は抑制されますが、達成可能な最大収縮期血圧は通常低下します。ジルチアゼム塩酸塩持続放出カプセル USP (1 日 1 回投与) による慢性治療では、血漿カテコールアミンの変化または増加は見られません。レニン-アンギオテンシン-アルドステロン軸の活性の増加は観察されていません。ジルチアゼム塩酸塩持続放出カプセル USP (1 日 1 回投与) は、アンギオテンシン II の腎臓および末梢への影響を軽減します。高血圧の動物モデルは、血圧の低下と尿量の増加、および尿中のナトリウム/カリウム比の変化を伴わないナトリウム利尿を伴うジルチアゼムに反応します。
日 1 回 60 mg から 480 mg までの用量の二重盲検並行用量反応研究では、ジルチアゼム塩酸塩徐放性カプセル (1 日 1 回用量) は、全用量にわたって直線的に運動終了までの時間を増加させました。研究した範囲。プラセボ、60 mg、120 mg、240 mg、360 mg、および 480 mg のトラフで測定されたブルース運動プロトコルを利用した運動終了までの時間の改善は、29、40、56、51、69、および 68 秒でした。 、 それぞれ。ジルチアゼム塩酸塩徐放性カプセル(1日1回投与)の用量が増加するにつれて、全体的な狭心症の頻度は減少しました。ジルチアゼム塩酸塩持続放出カプセル (1 日 1 回投与)、180 mg 1 日 1 回、またはプラセボが二重盲検試験で、長時間作用型硝酸塩および/またはベータ遮断薬による併用治療を受けている患者に投与されました。運動終了までの時間の大幅な増加と、全体的な狭心症の頻度の大幅な減少が観察されました。この試験では、塩酸ジルチアゼム持続放出カプセル(1日1回投与)治療群における有害事象の全体的な頻度は、プラセボ群と同じでした。
ジルチアゼム 20 mg の静脈内投与により、AH 伝導時間と房室結節の機能的および有効な不応期が約 20% 延長されます。 6 人の正常なボランティアに 300 mg のジルチアゼム塩酸塩を 1 回経口投与した研究では、平均最大 PR 延長は 14% であり、第 1 度以上の AV ブロックの例はありませんでした。ジルチアゼムに関連する AH 間隔の延長は、第 1 度心ブロックの患者ではそれほど顕著ではありません。洞不全症候群の患者では、ジルチアゼムは洞周期の長さを大幅に延長します (場合によっては最大 50%)。
塩酸ジルチアゼムを 1 日 540 mg までの用量で患者に慢性的に経口投与すると、PR 間隔がわずかに増加し、場合によっては異常な延長が生じることがあります ( 警告 )。
薬物動態と代謝
ジルチアゼムは胃腸管から十分に吸収され、広範な初回通過効果を受けやすく、約 40% の絶対バイオアベイラビリティ (静脈内投与と比較して) が得られます。ジルチアゼムは広範囲に代謝され、変化していない薬物のわずか 2% から 4% が尿中に現れます。肝ミクロソーム酵素を誘導または阻害する薬物は、ジルチアゼムの性質を変える可能性があります。
健康な志願者における短い IV 投与後の総放射能測定値は、ジルチアゼムよりも高濃度に達し、よりゆっくりと排出される他の未確認の代謝物の存在を示唆しています。総放射能の半減期は、ジルチアゼムの 2 ~ 5 時間と比較して約 20 時間です。
インビトロ結合研究は、ジルチアゼムが血漿タンパク質に70%から80%結合することを示しています。競合する in vitro リガンド結合研究では、ジゴキシン、ヒドロクロロチアジド、フェニルブタゾン、プロプラノロール、サリチル酸、またはワルファリンの治療濃度によってジルチアゼム結合が変化しないことも示されています。単回または複数回の薬物投与後の血漿消失半減期は、約 3.0 ~ 4.5 時間です。デスアセチルジルチアゼムはまた、親薬物の 10% から 20% のレベルで血漿中に存在し、ジルチアゼムと同じ冠血管拡張剤として 25% から 50% の効力があります。最小治療血漿ジルチアゼム濃度は、50 から 200 ng/mL の範囲にあるようです。線量強度が増加すると、直線性からの逸脱があります。半減期は用量とともにわずかに増加します。肝機能が正常な患者と肝硬変の患者を比較した研究では、肝障害のある患者の半減期が長くなり、バイオアベイラビリティが 69% 増加することがわかりました。重度の腎機能障害を持つ 9 人の患者を対象とした 1 件の研究では、腎機能が正常な患者と比較して、ジルチアゼムの薬物動態プロファイルに違いは見られませんでした。
ジルチアゼム塩酸塩持続放出カプセル(1日1回投与)
定常状態でのジルチアゼム錠剤のレジメンと比較すると、塩酸ジルチアゼム持続放出カプセル (1 日 1 回投与) 製剤からは 95% 以上の薬物が吸収されます。 360 mg のカプセルを 1 回服用すると、2 時間以内に血漿レベルが検出可能になり、10 ~ 14 時間で血漿レベルがピークになります。吸収は投与間隔を通して起こります。ジルチアゼム塩酸塩徐放性カプセル(1日1回投与)を高脂肪の朝食と併用した場合、ジルチアゼムの吸収の程度は影響を受けませんでした。用量ダンピングは発生しません。単回または複数回投与後の見かけの消失半減期は 5 ~ 8 時間です。ジルチアゼム錠剤およびジルチアゼム塩酸塩カプセル (1 日 2 回) で見られるものと同様の直線性からの逸脱が観察されます。ジルチアゼム塩酸塩徐放性カプセル(1日1回投与)は、1日120mgから240mgに増量すると、曲線下面積が2.7倍に増加します。用量が 240 mg から 360 mg に増加すると、曲線下面積が 1.6 倍に増加します。
患者情報
情報が提供されていません。を参照してください。 警告 と 予防 セクション。
