Lasix 40mg, 100mg 使用法、副作用および投与量。 オンライン薬局の価格。 処方箋不要のジェネリック医薬品。
ラシックスとは何ですか?
ラシックスは、うっ血性心不全、肝疾患、または腎障害を持つ個人の体液貯留 (浮腫) の症状を治療するために使用される処方薬です。ラシックスは、単独で使用することも、他の薬と併用することもできます。
ラシックスは、利尿薬、ループと呼ばれる薬のクラスに属しています。
ラシックス 40mg が 1 歳未満の子供に難治性高血圧症の治療に使用された場合、安全で効果があるかどうかはわかっていません。
ラシックス 40mg の副作用の可能性は何ですか?
Lasix 40mg は、次のような重大な副作用を引き起こす可能性があります。
- 立ちくらみ、
- あなたの耳に鳴り響く、
- 難聴、
- 筋肉の痙攣または収縮、
- 薄い肌、
- あざができやすい、
- 不正出血、
- 喉の渇きが増し、
- 排尿の増加、
- 口渇、
- フルーティーな口臭、
- 排尿がほとんどまたはまったくない、
- 足や足首のむくみ、
- 疲労感、
- 息を切らして、
- 食欲減少、
- 上腹部の痛み、
- 吐き気、
- 嘔吐、
- 暗い尿、
- 皮膚や目の黄変(黄疸)、
- 眠気、
- ぎくしゃくした感じ、
- 気持ちが不安定になり、
- 不規則な心拍、
- 胸の中でときめき、
- しびれやうずき、
- 筋肉のけいれん、および
- 筋力低下またはぐったり感
上記の症状がある場合は、すぐに医療機関を受診してください。
Lasix 40mg の最も一般的な副作用は次のとおりです。
- 下痢、
- 便秘、
- 食欲減少、
- しびれやうずき、
- 頭痛、
- めまい、および
- ぼやけた視界
気になる副作用や治らない副作用がある場合は、医師に相談してください。
これらは、ラシックスの考えられるすべての副作用ではありません。詳細については、医師または薬剤師にお尋ねください。
副作用に関する医学的アドバイスについては、医師に連絡してください。 1-800-FDA-1088 で副作用を FDA に報告できます。
警告
LASIX® (フロセミド) は強力な利尿剤であり、過剰に投与すると、水分と電解質の枯渇を伴う深刻な利尿を引き起こす可能性があります。したがって、慎重な医学的監督が必要であり、用量と用量スケジュールは個々の患者のニーズに合わせて調整する必要があります. (用法・用量を参照。)
説明
LASIX® は、アントラニル酸誘導体である利尿薬です。経口投与用の LASIX 100mg 錠剤には、有効成分としてフロセミドと次の不活性成分が含まれています。化学的には、4-クロロ-N-フルフリル-5-スルファモイルアントラニル酸です。 LASIX は、20、40、および 80 mg の投与量で、経口投与用の白い錠剤として入手できます。フロセミドは白色からオフホワイトの無臭の結晶性粉末です。水にはほとんど溶けず、アルコールにはほとんど溶けず、希アルカリ溶液には溶けやすく、希酸には溶けません。
CAS登録番号は54-31-9です。
構造式は次のとおりです。
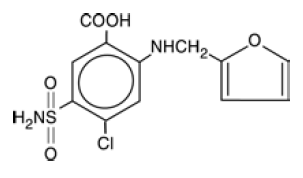
適応症
浮腫
LASIX は、うっ血性心不全、肝硬変、およびネフローゼ症候群を含む腎疾患に関連する浮腫の治療のために、成人および小児患者に適用されます。 LASIX 100mg は、利尿作用の高い薬剤が必要な場合に特に有用です。
高血圧症
経口ラシックス 40mg は、成人の高血圧症の治療に単独で、または他の降圧薬と組み合わせて使用できます。サイアザイドで十分にコントロールできない高血圧患者は、おそらく、LASIX だけでも十分にコントロールできないでしょう。
投薬と管理
浮腫
治療は、患者の反応に応じて個別化して、最大の治療反応を得て、その反応を維持するために必要な最小用量を決定する必要があります。
大人
LASIX の通常の初回投与量は、1 回 20 ~ 80 mg です。通常、迅速な利尿が続く。必要に応じて、同じ用量を 6 ~ 8 時間後に投与するか、用量を増やすことができます。用量は 20 または 40 mg ずつ増やされ、望ましい利尿効果が得られるまで、前の用量から 6 ~ 8 時間以内に投与されます。個別に決定された単回投与量は、1 日 1 回または 2 回 (たとえば、午前 8 時と午後 2 時に) 投与する必要があります。 LASIX 100mg の用量は、臨床的に重度の浮腫状態の患者では、1 日 600mg まで慎重に滴定することができます。
浮腫は、毎週 2 ~ 4 日間連続して LASIX 100mg を投与することによって、最も効率的かつ安全に動員される可能性があります。
80 mg/日を超える用量を長期間投与する場合は、注意深い臨床観察と実験室でのモニタリングが特に推奨されます。 (見る 予防 : 臨床検査 .)
高齢患者
一般に、高齢患者の用量選択は慎重に行う必要があり、通常は用量範囲の下限から始めます( 予防 : 高齢者の使用 )。
小児患者
小児患者における経口ラシックス 40mg の通常の初回投与量は、単回投与として 2mg/kg 体重です。初回投与後に利尿反応が不十分な場合は、前回の投与から 6 ~ 8 時間以内に 1 ~ 2 mg/kg ずつ増量してください。 6 mg/kg 体重を超える用量は推奨されません。小児患者の維持療法では、用量を最小有効レベルに調整する必要があります。
高血圧症
治療は、患者の反応に応じて個別化し、最大の治療反応を得て、治療反応を維持するために必要な最小用量を決定する必要があります。
大人
高血圧に対するラシックスの通常の初回投与量は 80 mg で、通常は 1 日 2 回 40 mg に分割されます。その後、反応に応じて投与量を調整する必要があります。反応が不十分な場合は、他の降圧薬を追加します。
LASIX 40mg を他の降圧薬と併用する場合、特に初期治療中は、血圧の変化を注意深く監視する必要があります。血圧の過度の低下を防ぐために、LASIX 100mg をレジメンに追加する場合は、他の薬剤の投与量を少なくとも 50% 減らす必要があります。血圧はラシックス 100mg の増強効果で低下するため、さらなる減量または他の降圧薬の中止が必要になる場合があります。
高齢患者
一般に、高齢患者の用量選択と用量調整は慎重に行う必要があり、通常は用量範囲の下限から始めます( 予防 : 高齢者の使用 )。
供給方法
ラシックス(フロセミド)錠20mg 100 個入りのボトルに入った白い楕円形のモノグラム錠として提供されます ( NDC 0039-0067-10) および 1000 ( NDC 0039-0067-70)。 20mg錠の片面に「Lasix®」と刻印されています。
ラシックス錠40mg 100 個入りのボトルに入った、白く、丸く、モノグラムが入った、スコアリングされた錠剤として提供されます ( NDC 0039-0060-13)、500( NDC 0039-0060-50)、および 1000 ( NDC 0039-0060-70)。 40mgの錠剤は片面に「Lasix® 40」と刻印されています。
ラシックス錠80mg 50 個入りのボトルに入った、白色の丸いモノグラムのファセット エッジ タブレットとして提供されます ( NDC 0039-0066-05) および 500 ( NDC 0039-0066-50)。 80mgの錠剤は片面に「Lasix® 80」と刻印されています。
ノート: 十分に密閉された耐光性容器に分注してください。光に当たると、わずかに変色する場合があります。変色した錠剤は調剤しないでください。
USP 溶出試験 2 で試験済み
25° C (77° F) で保管してください。 15 -30° C (59 -86° F) まで許容されるエクスカーション。 [見る USP制御の室温 .]
製造元: sanofi-aventis US LLC Bridgewater, NJ 08807. A Sanofi Company.. 改訂: 2016 年 3 月
副作用
有害反応は臓器系によって以下に分類され、重症度の降順でリストされています。
消化器系の反応
全身性過敏反応
中枢神経系の反応
血液反応
皮膚科過敏症反応
心血管反応
その他の反応
副作用が中等度または重度の場合はいつでも、LASIX の投与量を減らすか、治療を中止する必要があります。
薬物相互作用
LASIX 100mg は、特に腎機能障害がある場合、アミノグリコシド系抗生物質の聴器毒性を高める可能性があります。生命を脅かす状況を除いて、この組み合わせは避けてください。
LASIX は耳毒性の可能性があるため、エタクリン酸と併用してはいけません。リウマチ性疾患のように、LASIX と同時に高用量のサリチル酸を投与されている患者は、競合する腎排泄部位のために、低用量でサリチル酸の毒性を経験する可能性があります。
シスプラチンと LASIX を併用すると、聴器毒性のリスクがあります。さらに、シスプラチン治療中に強制利尿を達成するために使用された場合、LASIX 100mg が低用量で与えられず、体液バランスが正である場合、シスプラチンなどの腎毒性薬の腎毒性が増強される可能性があります。
LASIX は、ツボクラリンの骨格筋弛緩効果に拮抗する傾向があり、サクシニルコリンの作用を増強する可能性があります。
利尿薬はリチウムの腎クリアランスを減少させ、リチウム毒性のリスクを高めるため、一般にリチウムは利尿薬と一緒に投与すべきではありません。
アンギオテンシン変換酵素阻害剤またはアンギオテンシン II 受容体遮断薬と組み合わせた LASIX 40mg は、重度の低血圧および腎不全を含む腎機能の低下を引き起こす可能性があります。 LASIX、アンギオテンシン変換酵素阻害剤、またはアンギオテンシン受容体遮断薬の投与の中断または減量が必要になる場合があります。
増強は、神経節または末梢のアドレナリン遮断薬で起こります。
LASIX 40mg は、ノルエピネフリンに対する動脈の反応性を低下させる可能性があります。ただし、ノルエピネフリンは効果的に使用される可能性があります。
スクラルファートと LASIX 100mg 錠を同時に投与すると、LASIX のナトリウム利尿作用と降圧作用が低下する可能性があります。両方の薬を服用している患者は、LASIX 40mg の望ましい利尿作用および/または降圧作用が達成されているかどうかを判断するために、注意深く観察する必要があります。 LASIX 100mg とスクラルファートの摂取は、少なくとも 2 時間離してください。
孤立したケースでは、抱水クロラールを服用してから 24 時間以内に LASIX を静脈内投与すると、顔面紅潮、発汗発作、落ち着きのなさ、吐き気、血圧の上昇、および頻脈を引き起こす可能性があります。したがって、LASIX 40mg と抱水クロラールを併用することは推奨されません。
フェニトインは、LASIX の腎作用を直接妨害します。フェニトインによる治療が LASIX の腸管吸収を減少させ、その結果、ピーク血清フロセミド濃度を低下させるという証拠があります。
メトトレキサートや、LASIX のように腎尿細管分泌が著しい他の薬剤は、LASIX の効果を低下させる可能性があります。逆に、LASIX 100mg は、尿細管分泌を受ける他の薬物の腎排泄を減少させる可能性があります。 LASIX とこれらの他の薬剤の両方を高用量で治療すると、これらの薬剤の血清レベルが上昇する可能性があり、LASIX の毒性だけでなく、これらの薬剤の毒性も増強する可能性があります。
LASIX は、軽度または一過性の腎障害の設定においても、セファロスポリンによる腎毒性のリスクを高める可能性があります。
シクロスポリンと LASIX 40mg の併用は、LASIX 誘発性高尿酸血症および腎尿酸排泄のシクロスポリン障害に続発する痛風性関節炎のリスク増加と関連しています。
高用量 ( > 80 mg) のフロセミドは、甲状腺ホルモンの担体タンパク質への結合を阻害し、遊離甲状腺ホルモンの一時的な増加を引き起こし、続いて総甲状腺ホルモンレベルの全体的な減少をもたらす可能性があります.
6人の被験者を対象とした1件の研究では、フロセミドとアセチルサリチル酸の組み合わせが、慢性腎不全患者のクレアチニンクリアランスを一時的に減少させることが実証されました.フロセミドを NSAIDs と併用した場合、BUN、血清クレアチニンおよび血清カリウム値の上昇、体重増加を発症した患者の症例報告があります。
文献報告によると、インドメタシンの同時投与は、プロスタグランジン合成を阻害することにより、一部の患者で LASIX (フロセミド) のナトリウム利尿作用および降圧作用を低下させる可能性があります。インドメタシンは、血漿レニンレベル、アルドステロン排泄、およびレニンプロファイル評価にも影響を与える可能性があります.インドメタシンと LASIX の両方を投与されている患者は、LASIX 100mg の望ましい利尿作用および/または降圧作用が達成されているかどうかを判断するために、注意深く観察する必要があります。
警告
肝硬変および腹水の患者では、LASIX 100mg 療法は病院で開始するのが最善です。肝性昏睡および電解質枯渇状態では、基本的な状態が改善されるまで治療を開始しないでください。肝硬変患者における体液と電解質のバランスの突然の変化は、肝性昏睡を引き起こす可能性があります。したがって、利尿期間中は厳重な観察が必要です。塩化カリウムの補充と、必要に応じてアルドステロン拮抗薬は、低カリウム血症と代謝性アルカローシスの予防に役立ちます。
重度の進行性腎疾患の治療中に高窒素血症および乏尿が増加した場合は、LASIX 100mg を中止する必要があります。
耳鳴りおよび可逆的または不可逆的な聴覚障害および難聴の症例が報告されています。報告によると、通常、LASIX の耳毒性は、急速な注射、重度の腎障害、推奨用量よりも高い用量の使用、低タンパク血症、またはアミノグリコシド系抗生物質、エタクリン酸、またはその他の耳毒性のある薬物との併用療法に関連していることが示されています。医師が高用量の非経口療法を使用することを選択した場合は、制御された静脈内注入が推奨されます (成人の場合、1 分あたり 4 mg の LASIX を超えない注入速度が使用されています)。 (見る 予防 : 薬物相互作用 )
予防
全般的
過度の利尿は、循環虚脱を伴う脱水および血液量の減少を引き起こす可能性があり、特に高齢の患者では、血管血栓症および塞栓症の可能性があります。効果的な利尿薬と同様に、特に高用量および制限された塩分摂取量を摂取している患者では、LASIX 100mg 治療中に電解質の枯渇が起こる可能性があります。低カリウム血症は、特に活発な利尿、不十分な経口電解質摂取、肝硬変が存在する場合、またはコルチコステロイド、ACTH、大量の甘草の同時使用、または下剤の長期使用中に、LASIX で発生する可能性があります。ジギタリス療法は、低カリウム血症の代謝効果、特に心筋への影響を誇張する可能性があります。
LASIX 療法を受けているすべての患者は、体液または電解質の不均衡 (低ナトリウム血症、低塩素性アルカローシス、低カリウム血症、低マグネシウム血症または低カルシウム血症) の徴候または症状について観察する必要があります。筋肉疲労、低血圧、乏尿、頻脈、不整脈、または吐き気や嘔吐などの胃腸障害。血糖値の上昇と耐糖能試験の変化(空腹時と食後2時間の糖の異常を伴う)が観察されており、まれに真性糖尿病の発症が報告されています.
尿閉の重篤な症状 (膀胱排出障害、前立腺肥大症、尿道狭窄による) を有する患者では、フロセミドの投与により、尿の産生および貯留の増加に関連する急性尿閉を引き起こす可能性があります。したがって、これらの患者は、特に治療の初期段階で、注意深く監視する必要があります。
放射線造影剤腎症のリスクが高い患者では、放射線造影剤を受ける前に静脈内水分補給のみを受けた高リスク患者と比較して、放射線造影剤を受けた後の腎機能の悪化の発生率が高くなる可能性があります。
低タンパク血症(例、ネフローゼ症候群に関連する)の患者では、LASIX 40mg の効果が弱まり、耳毒性が増強される可能性があります。
無症候性高尿酸血症が発生する可能性があり、まれに痛風が誘発されることがあります。
スルホンアミドにアレルギーのある患者は、LASIX にもアレルギーがある可能性があります。全身性エリテマトーデスの増悪または活性化の可能性があります。
他の多くの薬物と同様に、血液障害、肝臓または腎臓の損傷、またはその他の特異な反応の発生の可能性について、患者を定期的に観察する必要があります。
臨床検査
血清電解質 (特にカリウム)、CO2、クレアチニン、および BUN は、LASIX 100mg 治療の最初の数か月間は頻繁に測定し、その後は定期的に測定する必要があります。血清および尿電解質の測定は、患者が大量に嘔吐している場合、または静脈注射を受けている場合に特に重要です。異常を是正するか、薬剤を一時的に中止する必要があります。他の薬も血清電解質に影響を与える可能性があります。
BUN の可逆的な上昇が発生する可能性があり、特に腎不全の患者では脱水を避ける必要があります。
LASIX 100mgを服用している糖尿病患者では、潜在的な糖尿病が疑われる場合でも、尿と血糖を定期的にチェックする必要があります.
LASIX 40mg は、カルシウム (テタニーのまれなケースが報告されています) とマグネシウムの血清レベルを低下させる可能性があります。したがって、これらの電解質の血清レベルを定期的に測定する必要があります。
未熟児では、LASIX 100mg は腎石灰沈着症/腎結石症を引き起こす可能性があるため、腎機能を監視し、腎超音波検査を実施する必要があります。 (見る 予防 : 小児用 )
発がん、突然変異誘発、生殖能力の障害
フロセミドの発がん性は、1 系統のマウスと 1 系統のラットで経口投与によって試験されました。乳腺癌の発生率は小さいが有意に増加し、メスのマウスではヒトの最大用量 600 mg の 17.5 倍の用量で発生した。 15 mg/kg の用量 (ヒトの最大用量よりわずかに多い) では雄ラットのまれな腫瘍のわずかな増加がありましたが、30 mg/kg では増加しませんでした。
フロセミドは、in vitro 代謝活性化系の存在下または非存在下で試験した場合、サルモネラ チフィムリウムのさまざまな株で変異原活性を欠いており、試験した最高用量のラット肝臓 S9 の存在下でマウスリンパ腫細胞の遺伝子変異に対して疑わしい陽性を示しました。フロセミドは in vitro でヒト細胞の姉妹染色分体交換を誘発しませんでしたが、in vitro でのヒト細胞の染色体異常に関する他の研究では相反する結果が得られました。チャイニーズハムスター細胞では染色体損傷を誘発したが、疑わしいことに姉妹染色分体交換が陽性であった.フロセミドによるマウスの染色体異常の誘発に関する研究は決定的ではなかった。この薬剤で処理されたラットの尿は、Saccharomyces cerevisiae の遺伝子変換を誘発しませんでした。
LASIX (フロセミド) は、100 mg/kg/日 (ラットの最大有効利尿薬用量であり、ヒトの最大用量である 600 mg/日の 8 倍) で、雄または雌のラットに受精能の障害を生じませんでした。
妊娠
妊娠区分 C - フロセミドは、人間の最大推奨用量の 2、4、8 倍で、原因不明の妊産婦死亡と流産をウサギに引き起こすことが示されています。妊娠中の女性を対象とした、十分に管理された研究はありません。潜在的な利点が胎児への潜在的なリスクを正当化する場合にのみ、妊娠中に LASIX を使用する必要があります。
妊娠中の治療では、出生時体重が増加する可能性があるため、胎児の成長を監視する必要があります。
マウス、ラット、およびウサギを用いて、胚および胎児の発育ならびに妊娠中の母動物に対するフロセミドの効果を調べた。
フロセミドは、最低用量の 25 mg/kg (人間の最大推奨用量 600 mg/日の 2 倍) で、ウサギに原因不明の妊産婦死亡と流産を引き起こしました。別の研究では、妊娠12日から17日の間にウサギに50mg/kgの用量(人間の最大推奨用量600mg/日の4倍)を投与した場合、母体の死亡と流産も引き起こしました. 3 番目の研究では、100 mg/kg の用量で生き残った妊娠ウサギはいませんでした。上記の研究からのデータは、母体の死亡に先行する可能性がある胎児の致死率を示しています。
マウスの研究と 3 つのウサギの研究の 1 つの結果は、発生率と比較して、処理された母動物に由来する胎児の水腎症 (腎盂と、場合によっては尿管の拡張) の発生率と重症度の増加も示しました。対照群の胎児。
授乳中の母親
母乳に含まれるため、授乳中の母親にラシックスを投与する場合は注意が必要です。
LASIX 40mg は授乳を阻害する可能性があります。
小児用
未熟児では、LASIX は腎石灰化症/腎結石症を引き起こす可能性があります。腎石灰化症/腎結石症は、LASIX で慢性的に治療された、未熟児の病歴のない 4 歳未満の子供にも観察されています。 LASIX を投与されている小児患者では、腎機能を監視し、腎超音波検査を考慮する必要があります。
生後数週間の未熟児に LASIX 40mg を投与すると、動脈管開存症が持続するリスクが高まる可能性があります。
高齢者の使用
LASIX 100mg の対照臨床研究には、65 歳以上の被験者が若い被験者と異なる反応を示すかどうかを判断するのに十分な数の被験者が含まれていませんでした。他の報告された臨床経験では、年配の患者と若い患者の間の反応の違いは確認されていません。一般に、高齢患者の用量選択は慎重に行う必要があり、通常は用量範囲の下限から開始します。これは、肝機能、腎機能、心機能の低下、および付随する疾患または他の薬物療法の頻度が高いことを反映しています。
この薬は腎臓から実質的に排泄されることが知られており、腎機能が低下している患者では、この薬に対する毒性反応のリスクが高くなる可能性があります。高齢患者は腎機能が低下している可能性が高いため、投与量の選択には注意が必要であり、腎機能のモニタリングが役立つ場合があります。 (見る 予防 : 全般的 と 投薬と管理 .)
過剰摂取
LASIX 40mgの過剰摂取の主な兆候と症状は、脱水、血液量の減少、低血圧、電解質の不均衡、低カリウム血症、低塩素性アルカローシスであり、利尿作用の延長です.
LASIX 100mg の急性毒性は、マウス、ラット、イヌで確認されています。 3 つすべてで、経口 LD50 は 1000 mg/kg 体重を超えましたが、静脈内 LD50 は 300 から 680 mg/kg の範囲でした。新生児ラットの急性胃内毒性は、成体ラットの 7 ~ 10 倍です。
毒性または死に関連する体液中の LASIX の濃度は不明です。
過剰摂取の治療は支持的であり、過剰な水分と電解質の損失の補充で構成されています.血清電解質、二酸化炭素濃度、血圧を頻繁に測定する必要があります。膀胱出口が閉塞している患者(前立腺肥大症など)では、適切なドレナージを確保する必要があります。
血液透析はフロセミドの排泄を促進しません。
禁忌
LASIX 40mg は、無尿症の患者およびフロセミドに対する過敏症の病歴のある患者には禁忌です。
臨床薬理学
LASIX の作用機序の調査では、ラットでの微小穿刺研究、犬でのストップ フロー実験、およびヒトと実験動物の両方でのさまざまなクリアランス研究が利用されています。 LASIX は主に近位尿細管と遠位尿細管だけでなく、ヘンレのループでもナトリウムと塩化物の吸収を阻害することが実証されています。高い有効性は、主に独自の作用部位によるものです。遠位尿細管に対する作用は、炭酸脱水酵素およびアルドステロンに対する阻害効果とは無関係です。
最近の証拠は、フロセミド グルクロニドが、ヒトにおけるフロセミドの唯一の、または少なくとも主要な生体内変換産物であることを示唆しています。フロセミドは血漿タンパク質、主にアルブミンに広範囲に結合します。 1 ~ 400 μg/mL の範囲の血漿濃度は、健康な個人では 91 ~ 99% 結合しています。非結合画分は、治療濃度で平均 2.3 ~ 4.1% です。
経口投与後の利尿の開始は1時間以内です。ピーク効果は、最初または 2 時間以内に発生します。利尿効果の持続時間は6~8時間です。
絶食した正常な男性では、ラシックス錠とラシックス経口溶液からのフロセミドの平均バイオアベイラビリティは、薬物の静脈内注射からのバイオアベイラビリティのそれぞれ 64% と 60% です。フロセミドは、経口溶液 (50 分) の方が錠剤 (87 分) よりも速く吸収されますが、ピーク血漿レベルと血漿濃度-時間曲線の下の面積に大きな違いはありません。ピーク血漿濃度は用量の増加とともに増加しますが、ピーク到達時間は用量によって異なりません。フロセミドの半減期は約 2 時間です。
IV注射後は、錠剤または経口溶液後よりもはるかに多くのフロセミドが尿中に排泄されます.尿中に排泄される未変化体の量は、2 つの経口製剤間で有意差はありません。
高齢者人口
アルブミンへのフロセミドの結合は、高齢患者では減少する可能性があります。フロセミドは、主に未変化のまま尿中に排泄されます。高齢の健康な男性被験者 (60 ~ 70 歳) における静脈内投与後のフロセミドの腎クリアランスは、若い健康な男性被験者 (20 ~ 35 歳) よりも統計的に有意に小さい。高齢者におけるフロセミドの初期利尿効果は、若年者に比べて低下している。 (見る 予防 : 高齢者の使用 .)
患者情報
LASIX を服用している患者は、過度の水分および/または電解質の喪失による症状を経験する可能性があることを通知する必要があります。時々発生する起立性低血圧は、通常、ゆっくり起き上がることで管理できます。低カリウム血症を制御または回避するために、カリウムのサプリメントおよび/または食事療法が必要になる場合があります。
真性糖尿病患者は、フロセミドが血糖値を上昇させ、それによって尿糖検査に影響を与える可能性があることを伝えておく必要があります。一部の患者の皮膚は、フロセミドを服用している間、日光の影響に対してより敏感になる場合があります.
高血圧患者は、食欲抑制や風邪症状のための市販薬など、血圧を上昇させる可能性のある薬を避ける必要があります。
