Aldactone 25mg, 100mg Spironolactone 使用法、副作用および投与量。 オンライン薬局の価格。 処方箋不要のジェネリック医薬品。
アルダクトンとは何ですか?また、どのように使用されますか?
アルダクトン 25 mg は、高血圧 (高血圧)、低カリウム レベル (低カリウム血症)、および心不全の症状を治療するために使用される処方薬です。 Aldactone 100mg は、単独で使用することも、他の薬と併用することもできます。
- アルダクトン 25mg は、アルドステロン拮抗薬、選択的、利尿薬、カリウム節約と呼ばれる薬のクラスに属します。
アルダクトン 100mg の副作用の可能性は何ですか?
アルダクトンは、次のような重大な副作用を引き起こす可能性があります。
- 立ちくらみ、
- 排尿がほとんどまたはまったくない、
- 血便またはタール便
- コーヒーかすのような吐血や吐血、
- 不均一な心拍数、
- 極度の喉の渇き、
- 排尿の増加、
- 足の不快感、
- 筋力低下またはぐったり感、
- 嘔吐、
- 筋肉のけいれん、
- しびれやチクチク感、
- 心拍数が遅く、
- 弱い脈、
- 頭痛、
- 錯乱、
- ろれつが回らない、
- 調整の喪失、および
- 不安定な感じ
上記の症状がある場合は、すぐに医療機関を受診してください。
アルダクトンの最も一般的な副作用は次のとおりです。
- 軽い吐き気、
- 嘔吐、
- 下痢、
- 乳房の腫れや圧痛、
- めまい、
- 頭痛、
- 軽い眠気、
- 脚のけいれん、および
- インポテンツまたは勃起困難
気になる副作用や治らない副作用がある場合は、医師に相談してください。
これらは、Aldactone の考えられるすべての副作用ではありません。詳細については、医師または薬剤師にお尋ねください。
副作用に関する医学的アドバイスについては、医師に連絡してください。 1-800-FDA-1088 で副作用を FDA に報告できます。
警告
ALDACTONE 100mg は、ラットの慢性毒性試験で発がん性物質であることが示されています (以下を参照)。 予防 )。 ALDACTONE 100mg は、適応症および使用法に記載されている条件でのみ使用してください。この薬の不必要な使用は避けるべきです。
説明
ALDACTONE 100mg経口錠剤には、アルドステロン拮抗薬スピロノラクトン、17-ヒドロキシ-7α-メルカプト-3-オキソ-17α-プレグン-4-エン-21-カルボン酸γ-ラクトンアセテートが25mg、50mg、または100mg含まれています。次の構造式があります。
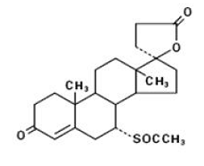
スピロノラクトンは水にほとんど溶けず、アルコールに溶け、ベンゼンとクロロホルムに溶けやすい。
不活性成分には、硫酸カルシウム、コーンスターチ、フレーバー、ヒプロメロース、酸化鉄、ステアリン酸マグネシウム、ポリエチレングリコール、ポビドン、および二酸化チタンが含まれます。
適応症
ALDACTONE (スピロノラクトン) は、以下の管理に適応されます。
原発性高アルドステロン症
治療試験による原発性高アルドステロン症の診断の確立。
原発性高アルドステロン症患者の短期術前治療。
アルドステロン産生副腎腺腫で手術のリスクが低いと判断された患者、または手術を辞退する患者に対する長期維持療法。
両側の微小結節性または大結節性副腎過形成(特発性アルドステロン症)患者に対する長期維持療法。
以下の患者の浮腫状態:
うっ血性心不全
患者が他の治療手段に部分的にしか反応しないか、または不耐性である場合の浮腫およびナトリウム貯留の管理。 ALDACTONE 100mg は、他の治療法が不適切と考えられる場合に、ジギタリスを服用しているうっ血性心不全患者にも適応となります。
浮腫および/または腹水を伴う肝硬変
この状態では、アルドステロン値が非常に高くなることがあります。 ALDACTONE は、安静と水分とナトリウムの制限を伴う維持療法に適応されます。
ネフローゼ症候群
基礎疾患の治療、水分とナトリウム摂取の制限、および他の利尿薬の使用が適切な反応をもたらさない場合のネフローゼ患者。
本態性高血圧
ALDACTONE 25mg は、血圧を下げるために高血圧の治療に適応されます。血圧を下げると、主に脳卒中や心筋梗塞などの致命的および非致命的な心血管イベントのリスクが低下します。これらの利点は、さまざまな薬理学的クラスの降圧薬の対照試験で見られました。
高血圧の管理は、必要に応じて、脂質管理、糖尿病管理、抗血栓療法、禁煙、運動、およびナトリウム摂取制限を含む包括的な心血管リスク管理の一部であるべきです。多くの患者は、血圧目標を達成するために複数の薬を必要とします。目標と管理に関する具体的なアドバイスについては、国立高血圧教育プログラムの高血圧の予防、検出、評価、および治療に関する合同全国委員会 (JNC) のガイドラインなど、公開されているガイドラインを参照してください。
さまざまな薬理学的クラスから、作用機序の異なる多数の降圧薬が無作為対照試験で示され、心血管疾患の罹患率と死亡率を低下させることが示されています。これらの利点の大部分を担っているのは薬です。最大かつ最も一貫した心血管転帰の利点は、脳卒中のリスクの低下ですが、心筋梗塞と心血管死亡率の低下も定期的に見られています.
収縮期圧または拡張期圧の上昇は心血管リスクの増加を引き起こし、mmHg あたりの絶対リスク増加は血圧が高いほど大きくなるため、重度の高血圧をわずかに低下させるだけでもかなりの利益が得られます。血圧低下による相対リスク低下は、絶対リスクが異なる集団全体で類似しているため、高血圧とは無関係にリスクが高い患者 (たとえば、糖尿病や高脂血症の患者) では絶対的利益が大きくなり、そのような患者は、より積極的な治療により、より低い血圧の目標を達成することができます。
一部の降圧薬は、黒人患者では(単剤療法として)血圧への影響が小さく、多くの降圧薬には追加の承認された適応症と効果があります(例、狭心症、心不全、または糖尿病性腎疾患)。これらの考慮事項は、治療法の選択の指針となる場合があります。
通常、他の薬剤と組み合わせて使用される ALDACTONE は、他の薬剤では十分に治療できない患者、または他の薬剤が不適切であると考えられる患者に適応されます。
低カリウム血症
他の手段が不適切または不十分であると考えられる場合の低カリウム血症患者の治療用。 ALDACTONE 100mg は、他の手段が不十分または不適切であると考えられるジギタリスを服用している患者の低カリウム血症の予防にも適応されます。
重度の心不全 (NYHA クラス III - IV)
標準治療に加えて使用することで、生存率を高め、心不全による入院の必要性を減らす。
妊娠中の使用
それ以外は健康な女性に利尿薬を日常的に使用することは不適切であり、母親と胎児を不必要な危険にさらします.利尿薬は妊娠中毒症の発症を予防するものではなく、発症する中毒症の治療に利尿薬が有用であるという十分な証拠はありません。
妊娠中の浮腫は、病理学的原因から、または妊娠の生理学的および機械的結果から生じる可能性があります。
ALDACTONE は、浮腫が妊娠していない場合と同様に病理学的原因による場合、妊娠中に適応となります (ただし、 予防 : 妊娠 )。拡張した子宮による静脈還流の制限に起因する妊娠中の依存性浮腫は、下肢の持ち上げとサポートホースの使用によって適切に治療されます。この場合、血管内容積を下げるために利尿薬を使用することはサポートされておらず、不必要です。正常な妊娠中は血液量増加があり、これは胎児にも母親にも (心血管疾患がない場合) 有害ではありませんが、大部分の妊婦では全身性浮腫を含む浮腫に関連しています。この浮腫によって不快感が生じた場合は、横臥を増やすと軽減されることがよくあります。まれに、この浮腫が極度の不快感を引き起こし、休んでも解消されないことがあります。これらの場合、利尿薬の短期コースは緩和を提供する可能性があり、適切な場合があります.
投薬と管理
原発性高アルドステロン症
ALDACTONE は、患者が通常の食事をしている間に原発性高アルドステロン症の推定証拠を提供するための初期診断手段として採用される場合があります。
ロングテスト
ALDACTONE 100mg は、1 日 400mg を 3 週間から 4 週間投与します。低カリウム血症と高血圧の矯正は、原発性高アルドステロン症の診断の推定証拠を提供します。
ショートテスト
ALDACTONE は、1 日 400 mg を 4 日間投与します。アルダクトン 25mg の投与中に血清カリウム値が上昇し、アルダクトン 25mg の投与を中止すると血清カリウム値が低下する場合は、原発性高アルドステロン症の推定診断を考慮する必要があります。
高アルドステロン症の診断がより決定的な検査手順によって確立された後、アルダクトーンは手術の準備として毎日100から400 mgの用量で投与されることがあります.手術に適さないと考えられる患者には、アルダクトン 100mg を、個々の患者に決定された最低有効用量で長期維持療法に使用することができます。
成人の浮腫(うっ血性心不全、肝硬変、ネフローゼ症候群)
ALDACTONE の 1 日 100 mg の初回投与量を単回または分割投与することをお勧めしますが、1 日あたり 25 ~ 200 mg の範囲で投与することもできます。利尿剤として単独で投与する場合、ALDACTONE は最初の用量レベルで少なくとも 5 日間継続する必要があります。 5 日後に ALDACTONE に対する適切な利尿反応が起こらない場合は、腎尿細管のより近位で作用する 2 つ目の利尿薬をレジメンに追加することができます。このような利尿薬と同時に投与された場合のALDACTONEの相加効果のため、通常、併用治療の初日に増強された利尿が始まります。併用療法は、より迅速な利尿が望まれる場合に適応となります。他の利尿剤療法を追加する場合、ALDACTONE の投与量は変更しないでください。
本態性高血圧
成人の場合、ALDACTONE 100mg として 1 日 50~100mg を初回または分割して服用することをお勧めします。 ALDACTONE は、尿細管のより近位で作用する利尿薬や他の降圧薬と併用することもできます。 ALDACTONE による治療は、少なくとも 2 週間継続する必要があります。これまでは最大の反応が得られない可能性があるためです。その後、患者の反応に応じて投与量を調整する必要があります。
低カリウム血症
1 日 25 mg から 100 mg の範囲の用量の ALDACTONE は、利尿薬による低カリウム血症の治療に有用であり、経口カリウム サプリメントまたはその他のカリウム節約レジメンが不適切であると考えられます。
標準療法と組み合わせた重度の心不全 (NYHA クラス III - IV)
患者の血清カリウムが≦5.0mEq/Lで、患者の血清クレアチニンが≦2.5mg/dLの場合、治療はALDACTONE 25mgを1日1回から開始する必要があります。 1 日 1 回 25 mg に耐えられる患者は、臨床的に示されているように、1 日 1 回 50 mg に用量を増やすことができます。 1 日 1 回 25 mg に耐えられない患者は、1 日おきに 25 mg に減量することができます。見る 警告 : 血清カリウムと血清クレアチニンのモニタリングに関するアドバイスのための重度の心不全患者の高カリウム血症 .
供給方法
ALDACTONE 25 mg 錠剤は円形で、薄黄色で、フィルムコーティングされており、片面に SEARLE と 1001 がデボス加工され、もう片面に ALDACTONE と 25 が刻印されています。次のように供給されます。
ALDACTONE 50 mg 錠剤は、楕円形、明るいオレンジ色、刻み目があり、フィルム コーティングされており、刻み目のある側に SEARLE と 1041 がデボス加工され、反対側に ALDACTONE と 50 がデボス加工されています。次のように供給されます。
ALDACTONE 100 mg 錠剤は円形、ピーチ色、刻み目があり、フィルム コーティングされており、刻み目のある側に SEARLE と 1031 がデボス加工され、反対側に ALDACTONE と 100 がデボス加工されており、次のように供給されます。
77°F (25°C) 以下で保管してください。
配布元: GD Searle LLC, Division of Pfizer Inc, NY, NY 10017. 改訂: 2016 年 10 月
副作用
以下の副作用が報告されており、各カテゴリー(身体システム)内で、重症度の低い順にリストされています.
消化器: 胃出血、潰瘍、胃炎、下痢およびけいれん、吐き気、嘔吐。
生殖: 女性化乳房(を参照 予防 )、勃起を達成または維持できない、月経不順または無月経、閉経後の出血、乳房の痛み。 ALDACTONE 25mgを服用している患者で乳房の癌が報告されていますが、因果関係は確立されていません.
血液学: 白血球減少症(無顆粒球症を含む)、血小板減少症。
過敏症: 発熱、蕁麻疹、斑状丘疹または紅斑性皮膚発疹、アナフィラキシー反応、血管炎。
代謝: 高カリウム血症、電解質障害(参照 警告 と 予防 )。
筋骨格: 脚のけいれん。
神経系・精神科: 無気力、精神錯乱、運動失調、めまい、頭痛、眠気。
肝臓・胆道: ALDACTONE の投与により、胆汁うっ滞性/肝細胞性毒性が混在し、死亡例が 1 例報告されています。
腎臓: 腎機能障害(腎不全を含む)。
肌: スティーブンス・ジョンソン症候群 (SJS)、中毒性表皮壊死融解症 (TEN)、好酸球増多症および全身症状を伴う薬物発疹 (DRESS)、脱毛症、そう痒症。
薬物相互作用
ACE阻害剤
ACE阻害薬とカリウム保持性利尿薬の併用投与は、重度の高カリウム血症と関連しています。
アンギオテンシン II 拮抗薬、アルドステロン遮断薬、ヘパリン、低分子量ヘパリン、および高カリウム血症を引き起こすことが知られているその他の薬物
同時投与は、重度の高カリウム血症を引き起こす可能性があります。
アルコール、バルビツレート、または麻薬
起立性低血圧の増強が起こることがある。
コルチコステロイド、ACTH
強化された電解質枯渇、特に低カリウム血症が起こることがあります。

昇圧アミン(例、ノルエピネフリン)
ALDACTONE は、ノルエピネフリンに対する血管の反応性を低下させます。したがって、ALDACTONE による治療中に局所麻酔または全身麻酔を受けた患者の管理には注意が必要です。
骨格筋弛緩剤、非脱分極剤(例、ツボクラリン)
筋弛緩剤に対する反応性が高まる可能性があります。
リチウム
リチウムは一般に利尿薬と一緒に投与すべきではありません。利尿剤は、リチウムの腎クリアランスを低下させ、リチウム毒性のリスクを高めます。
非ステロイド系抗炎症薬(NSAID)
一部の患者では、NSAID の投与により、ループ利尿薬、カリウム保持薬、およびサイアザイド利尿薬の利尿作用、ナトリウム利尿作用、および降圧作用が低下する可能性があります。インドメタシンなどの NSAID とカリウム保持性利尿薬の併用は、重度の高カリウム血症と関連しています。したがって、ALDACTONE 100mg と NSAIDs を併用する場合は、患者を注意深く観察して、利尿剤の望ましい効果が得られるかどうかを判断する必要があります。
ジゴキシン
ALDACTONE は、ジゴキシンの半減期を延長することが示されています。これにより、血清ジゴキシンレベルが上昇し、その後ジギタリス毒性が生じる可能性があります。 ALDACTONE 100mg を投与する場合は、維持量とデジタル化量を減らす必要があるかもしれません。デジタル化の過剰または不足を避けるために、患者を注意深く監視する必要があります。
コレスチラミン
コレスチラミンと同時にALDACTONEを投与された患者では、高カリウム血症性代謝性アシドーシスが報告されています。
薬物/実験室試験の相互作用
ALDACTONE またはその代謝産物によるジゴキシン ラジオイムノアッセイへの干渉の可能性に関するいくつかの報告が文献に登場しています。その干渉の程度も潜在的な臨床的重要性 (アッセイに特異的である可能性があります) も完全には確立されていません。
警告
カリウム補給
薬の形またはカリウムが豊富な食事としてのカリウム補給は、通常、ALDACTONE療法に関連して与えられるべきではありません.過度のカリウム摂取は、ALDACTONE を投与されている患者に高カリウム血症を引き起こす可能性があります ( 予防 : 全般的 )。
ALDACTONE 25mg を次の薬剤またはカリウム源と併用すると、重度の高カリウム血症を引き起こす可能性があります。
- その他のカリウム保持性利尿薬
- ACE阻害薬
- アンギオテンシン II 拮抗薬
- アルドステロン遮断薬
- インドメタシンなどの非ステロイド系抗炎症薬(NSAID)
- ヘパリンおよび低分子量ヘパリン
- 高カリウム血症を引き起こすことが知られている他の薬物または状態
- カリウムサプリメント
- カリウムが豊富な食事
- カリウムを含む塩代替物
ALDACTONE 25mg は、他のカリウム保持性利尿薬と同時に投与すべきではありません。 ALDACTONE 25mg を ACE 阻害剤またはインドメタシンと併用した場合、利尿剤の存在下であっても、重度の高カリウム血症と関連しています。 ALDACTONE をこれらの薬剤と同時に投与する場合は、細心の注意を払う必要があります。
重度の心不全患者における高カリウム血症
高カリウム血症は致命的となる場合があります。 ALDACTONE を投与されている重度の心不全患者の血清カリウムを監視および管理することが重要です。他のカリウム保持性利尿薬の使用は避けてください。血清カリウム値が 3.5 mEq/L を超える患者では、経口カリウム サプリメントの使用を避ける。 RALES は、血清クレアチニンが 2.5 mg/dL を超える患者、または血清クレアチニンが最近 25% を超える上昇を示した患者を除外しました。推奨されるカリウムとクレアチニンのモニタリングは、ALDACTONE の開始または用量の増加後 1 週間で、最初の 3 か月間は毎月、その後 1 年間は四半期ごと、その後は 6 か月ごとです。
血清カリウム > 5 mEq/L または血清クレアチニン > 4 mg/dL の場合は、治療を中止または中断します。 (見る 臨床研究 : 重度の心不全 、 と 投薬と管理 : 重度の心不全 .) ALDACTONE は、肝機能障害のある患者には注意して使用する必要があります。これは、体液と電解質のバランスのわずかな変化が肝性昏睡を引き起こす可能性があるためです。
リチウムは一般に利尿薬と一緒に投与すべきではありません( 薬物相互作用 )。
予防
全般的
利尿薬療法を受けているすべての患者は、体液または電解質の不均衡、例えば、低マグネシウム血症、低ナトリウム血症、低塩素性アルカローシス、および高カリウム血症の兆候がないか観察する必要があります。
血清および尿電解質の測定は、患者が過度に嘔吐している場合や静脈注射を受けている場合に特に重要です。原因に関係なく、水分と電解質の不均衡の警告兆候または症状には、口の乾燥、喉の渇き、脱力感、無気力、眠気、落ち着きのなさ、筋肉痛またはけいれん、筋肉疲労、低血圧、乏尿、頻脈、および吐き気などの胃腸障害が含まれます。そして嘔吐。高カリウム血症は、腎機能障害または過剰なカリウム摂取のある患者に発生する可能性があり、致命的な心臓の不規則性を引き起こす可能性があります.したがって、通常、ALDACTONE と一緒にカリウムのサプリメントを投与するべきではありません。
高カリウム血症が疑われる場合(感覚異常、筋力低下、疲労、四肢の弛緩性麻痺、徐脈、ショックなどの警告サイン)、心電図(ECG)を取得する必要があります。ただし、軽度の高カリウム血症は心電図の変化と関連していない可能性があるため、血清カリウム値を監視することが重要です。
高カリウム血症が存在する場合は、ALDACTONE を直ちに中止する必要があります。重度の高カリウム血症では、臨床状況によって採用される手順が決まります。これらには、塩化カルシウム溶液、重炭酸ナトリウム溶液の静脈内投与、および/または即効型インスリン製剤によるグルコースの経口または非経口投与が含まれる場合があります。これらは、必要に応じて繰り返される一時的な措置です。ポリスチレンスルホン酸ナトリウムなどの陽イオン交換樹脂は、経口または直腸投与することができる。高カリウム血症が持続すると、透析が必要になる場合があります。
通常は高カリウム血症に伴う可逆性高塩素血症性代謝性アシドーシスが、腎機能が正常な場合でも非代償性肝硬変の一部の患者で発生することが報告されています。
希釈性低ナトリウム血症は、口の乾燥、喉の渇き、無気力、および眠気によって現れ、血清ナトリウム濃度の低下によって確認され、特にALDACTONEを他の利尿薬と組み合わせて投与した場合に引き起こされるか、または悪化する可能性があり、浮腫性患者では希釈性低ナトリウム血症が発生する可能性があります。暑い季節の患者;低ナトリウム血症が生命を脅かすまれな場合を除いて、適切な治療法はナトリウムの投与ではなく水分制限です。
ALDACTONE 療法は、特に既存の腎障害のある患者で、BUN の一時的な上昇を引き起こす可能性があります。アルダクトンは軽度のアシドーシスを引き起こす可能性があります。
ALDACTONE の使用に関連して女性化乳房が発生することがあります。医師は発症の可能性に注意する必要があります。女性化乳房の発症は、投与量と治療期間の両方に関連しているようであり、ALDACTONE 100mg を中止すると通常は元に戻ります。まれに、ALDACTONE を中止しても胸の肥大が持続することがあります。
一部の患者では、傾眠やめまいが起こると報告されています。初期治療に対する反応が確認されるまでは、機械の運転や操作には注意が必要です。
臨床検査
電解質の不均衡の可能性を検出するための血清電解質の定期的な測定は、適切な間隔で行う必要があります。特に、高齢者や重大な腎障害または肝障害のある人では重要です。
発がん、突然変異誘発、生殖能力の障害
経口投与された ALDACTONE は、ラットで実施された混餌投与研究で発癌物質であることが示されており、その増殖効果は内分泌器官と肝臓に現れています。約 50、150、および 500 mg/kg/日の用量を使用した 18 か月の研究では、甲状腺および精巣の良性腺腫が統計的に有意に増加し、雄ラットでは、用量に関連して増殖性変化が増加しました。肝臓(肝細胞腫大および過形成結節を含む)。同じ系統のラットに約 10、30、100、および 150 mg ALDACTONE/kg/日の用量を投与した 24 か月の研究では、増殖効果の範囲には、肝細胞腺腫および精巣間質細胞腫瘍の有意な増加が含まれていました。男性、および甲状腺濾胞細胞腺腫および癌腫の有意な増加が男女ともに見られます。また、統計的に有意ではあるが、用量とは関係のない雌の良性子宮内膜間質ポリープの増加がありました。
用量依存性(20 mg/kg/日以上)の骨髄性白血病の発生率が、カンレノ酸カリウム(アルダクトン 25 mg と化学的に類似した化合物であり、その一次代謝産物であるカンレノンもアルダクトン 25 mg の主要生成物でもある化合物)の毎日の用量を与えられたラットで観察されました。男性の場合)1年間。ラットでの 2 年間の研究では、カンレノ酸カリウムの経口投与は、骨髄性白血病、肝臓、甲状腺、精巣、および乳腺の腫瘍と関連していました。
ALDACTONE 25mg もカンレノ酸カリウムも、細菌または酵母を使用した試験で変異原性を生じませんでした。代謝活性化がない場合、ALDACTONE 25mg もカンレノ酸カリウムも in vitro の哺乳動物試験で変異原性を示さなかった.代謝活性化の存在下で、ALDACTONE は in vitro でのいくつかの哺乳動物変異原性試験で陰性であると報告されており、in vitro での他の哺乳動物試験での変異原性については決定的ではありません (ただしわずかに陽性)。代謝活性化の存在下で、カンレノ酸カリウムは in vitro でのいくつかの哺乳動物試験で変異原性が陽性であることが報告されており、他の試験では決定的ではなく、さらに他の試験では陰性である.
雌ラットに 15 および 50 mg/kg/日のアルダクトンを混餌投与した 3 腹繁殖試験では、交配および受胎能に影響はありませんでしたが、50 mg/kg では死産児の発生率がわずかに増加しました。 /日。雌ラットに注射した場合 (100 mg/kg/日、7 日間、腹腔内)、ALDACTONE は、治療中に発情期を延長し、治療後 2 週間の観察期間中に一定の発情期を誘発することにより、発情周期の長さを増加させることがわかりました。これらの影響は、卵胞発育の遅延と循環エストロゲンレベルの低下に関連しており、交尾、生殖能力、および繁殖力を損なうと予想されます。 ALDACTONE (100 mg/kg/日) を未処理のオスと 2 週間の同居期間中にメスのマウスに腹腔内投与すると、受胎した交配マウスの数が減少し (排卵の阻害によって引き起こされることが示されている効果)、その数が減少しました。妊娠した胚における着床胚の増加 (着床の阻害によって引き起こされることが示されている効果)、および 200 mg/kg では、交配までの潜伏期間も増加しました。
妊娠
催奇形性効果
ALDACTONE を使用した奇形学研究は、マウスとウサギで最大 20 mg/kg/日の用量で実施されています。体表面積に基づいて、マウスにおけるこの用量は、ヒトの最大推奨用量を大幅に下回り、ウサギでは、ヒトの最大推奨用量に近い.マウスでは催奇形性またはその他の胚毒性効果は観察されなかったが、20 mg/kg の用量は、ウサギの再吸収率の増加と生きている胎児の数の減少を引き起こした.その抗アンドロゲン活性と雄の形態形成のためのテストステロンの必要性のために、ALDACTONE は胚形成中に雄の性分化に悪影響を与える可能性があります。ラットに 200 mg/kg/日を妊娠 13 日から 21 日 (後期胚形成および胎児発育) に投与すると、雄胎児の女性化が観察された。妊娠後期に 50 および 100 mg/kg/日用量の ALDACTONE に曝露された子孫は、雄の腹側前立腺および精嚢の重量の用量依存的な減少、雌の卵巣および子宮の肥大を含む生殖管の変化を示しました。成人期まで持続する内分泌機能障害の他の徴候。妊娠中の女性を対象とした ALDACTONE の十分に管理された研究はありません。 ALDACTONE は、黄体ホルモン作用や抗アンドロゲン作用など、動物における内分泌作用が知られています。抗アンドロゲン効果は、女性化乳房など、ヒトに明らかなエストロゲン様副作用をもたらす可能性があります。したがって、妊婦に ALDACTONE 25mg を使用するには、予想される利益と胎児への危険の可能性を比較検討する必要があります。
授乳中の母親
ALDACTONE 25mg の主要な (かつ活性な) 代謝産物であるカンレノンは、ヒトの母乳に含まれています。 ALDACTONE 100mg はラットで腫瘍原性があることがわかっているため、母親にとっての薬物の重要性を考慮して、薬物を中止するかどうかを決定する必要があります。薬物の使用が不可欠であると判断された場合は、代替の乳児栄養法を導入する必要があります。
小児用
小児患者における安全性と有効性は確立されていません。
過剰摂取
ALDACTONE の経口 LD50 は、マウス、ラット、およびウサギで 1000 mg/kg を超えています。
ALDACTONE の急性過剰摂取は、眠気、精神錯乱、黄斑丘疹または紅斑性発疹、吐き気、嘔吐、めまい、または下痢によって現れることがあります。まれに、低ナトリウム血症、高カリウム血症、または肝性昏睡が重度の肝疾患の患者に発生することがありますが、これらは急性の過剰摂取によるものではありません.特に腎機能障害のある患者では、高カリウム血症が起こることがあります。
処理
嘔吐を誘発するか、洗浄によって胃を避難させます。特定の解毒剤はありません。治療は、水分補給、電解質バランス、および重要な機能を維持するのに役立ちます。
腎障害のある患者は、スピロノラクトン誘発性高カリウム血症を発症する可能性があります。このような場合、ALDACTONE は直ちに中止する必要があります。重度の高カリウム血症では、臨床状況によって採用される手順が決まります。これらには、塩化カルシウム溶液、重炭酸ナトリウム溶液の静脈内投与、および/または即効型インスリン製剤によるグルコースの経口または非経口投与が含まれる場合があります。これらは、必要に応じて繰り返される一時的な措置です。ポリスチレンスルホン酸ナトリウムなどの陽イオン交換樹脂は、経口または直腸投与することができる。高カリウム血症が持続すると、透析が必要になる場合があります。
禁忌
ALDACTONE 100mg は、無尿症、急性腎不全、腎排泄機能の著しい障害、高カリウム血症、アジソン病、エプレレノン併用患者には禁忌です。
臨床薬理学
作用機序
ALDACTONE (スピロノラクトン) は、アルドステロンの特異的な薬理学的アンタゴニストであり、主に遠位尿細管のアルドステロン依存性ナトリウム-カリウム交換部位での受容体の競合結合を介して作用します。 ALDACTONE はナトリウムと水の排出量を増加させますが、カリウムは保持されます。 ALDACTONE は、このメカニズムにより、利尿薬と降圧薬の両方として作用します。単独で、または腎尿細管のより近位で作用する他の利尿剤と一緒に投与することができます。
アルドステロンアンタゴニスト活性
ミネラルコルチコイド、アルドステロンのレベルの増加は、原発性および続発性アルドステロン症に見られます。二次アルドステロン症が通常関与する浮腫状態には、うっ血性心不全、肝硬変、およびネフローゼ症候群が含まれます。受容体部位でアルドステロンと競合することにより、ALDACTONE 25mgは、これらの状態の浮腫と腹水の効果的な治療法を提供します. ALDACTONE は、能動的利尿療法によって引き起こされる体液量の枯渇および関連するナトリウム損失によって引き起こされる二次性アルドステロン症に対抗します。
ALDACTONE 25mg は、原発性高アルドステロン症患者の収縮期および拡張期血圧を下げるのに効果的です。良性の本態性高血圧症ではアルドステロン分泌が正常範囲内であるにもかかわらず、本態性高血圧症のほとんどの場合にも有効です。
ALDACTONE は、アルドステロンの作用に拮抗する作用を通じて、遠位尿細管でのナトリウムとカリウムの交換を阻害し、カリウムの損失を防ぐのに役立ちます。
ALDACTONE 25mg が血清尿酸値を上昇させたり、痛風を誘発したり、炭水化物代謝を変化させたりすることは実証されていません。
薬物動態
ALDACTONE は迅速かつ広範囲に代謝されます。硫黄含有製品は主要な代謝産物であり、ALDACTONE とともに、薬物の治療効果の主な原因であると考えられています。以下の薬物動態データは、100 mg のスピロノラクトン (ALDACTONE フィルムコーティング錠) を 15 日間毎日投与した後、12 人の健康なボランティアから得られました。 15日目、低脂肪の朝食の直後にスピロノラクトンを投与し、その後採血を行った。
ヒトにおけるスピロノラクトン代謝物の薬理活性は知られていない。しかし、副腎摘出ラットでは、スピロノラクトンに対する代謝産物 C、TMS、および HTMS の抗ミネラルコルチコイド活性は、それぞれ 1.10、1.28、および 0.32 でした。スピロノラクトンと比較して、ラット腎臓切片におけるアルドステロン受容体への結合親和性は、それぞれ 0.19、0.86、および 0.06 でした。
ヒトでは、TMS と 7-α-チオスピロラクトンの尿中電解質組成に対する合成ミネラルコルチコイド、フルドロコルチゾンの影響を逆転させる効力は、スピロノラクトンと比較して、それぞれ 0.33 と 0.26 でした。しかし、これらのステロイドの血清濃度は測定されていないため、生体内活性の低下の理由として、それらの不完全な吸収および/または初回通過代謝を除外することはできませんでした。
スピロノラクトンとその代謝物は 90% 以上が血漿タンパク質に結合しています。代謝産物は、主に尿に排泄され、次に胆汁に排泄されます。
スピロノラクトンの吸収に対する食物の影響 (2 つの 100 mg ALDACTONE 錠剤) は、9 人の健康で薬物を使用していないボランティアの単回投与試験で評価されました。食物は、代謝されていないスピロノラクトンのバイオアベイラビリティをほぼ 100% 増加させました。この所見の臨床的重要性は不明です。
臨床研究
重度の心不全
Randomized Aldactone 100mg Evaluation Study (RALES) は、駆出率が 35% 以下で、6 か月以内にニューヨーク心臓協会 (NYHA) のクラス IV の心不全の病歴があり、クラス III の患者を対象とした多国籍二重盲検試験でした - -無作為化時のIV心不全。すべての患者は、ループ利尿薬を服用する必要があり、忍容性がある場合は ACE 阻害剤を服用する必要がありました。ベースラインの血清クレアチニンが 2.5 mg/dL を超える患者、または最近 25% 増加した患者、またはベースラインの血清カリウムが 5.0 mEq/L を超える患者は除外されました。
患者は、スピロノラクトン 25 mg を 1 日 1 回経口投与するか、一致するプラセボに 1:1 で無作為に割り付けられました。経過観察と臨床検査(血清カリウムとクレアチニンを含む)は、最初の 12 週間は 4 週間ごと、最初の 1 年間は 3 か月ごと、その後は 6 か月ごとに実施されました。重度の高カリウム血症の場合、または血清クレアチニンが 4.0 mg/dL を超える場合は、投与を控えることができます。最初の投薬レジメンに耐えられなかった患者は、1週間から4週間で1日おきに1錠に減量されました. 8 週間で 1 日 1 錠に耐えられた患者は、治験責任医師の裁量で 1 日 2 錠に増量された可能性があります。
RALES は、1995 年 3 月 24 日から 1996 年 12 月 31 日までの間に 15 か国の 195 のセンターで 1663 人の患者 (3% が米国) を登録しました。研究集団は主に白人でした (87%、7% が黒人、2% がアジア人、4% がその他)。 、男性(73%)、および高齢者(中央値67歳)。駆出率の中央値は 0.26 でした。 70% が NYHA クラス III で、29% がクラス IV でした。心不全の推定病因は、55%が虚血性で、45%が非虚血性でした。 28%に心筋梗塞、24%に高血圧、22%に糖尿病の病歴がありました。ベースラインの血清クレアチニンの中央値は 1.2 mg/dL で、ベースラインのクレアチニンクリアランスの中央値は 57 mL/分でした。スピロノラクトンに無作為に割り付けられた患者の試験終了時の平均 1 日量は 26 mg でした。
併用薬には、患者の 100% にループ利尿薬、97% に ACE 阻害剤が含まれていました。研究中にいつでも使用された他の薬には、ジゴキシン(78%)、抗凝固薬(58%)、アスピリン(43%)、ベータ遮断薬(15%)が含まれていました.
RALES の主要評価項目は、全死因死亡までの時間でした。計画された中間解析で有意な死亡率の改善が検出されたため、平均 24 か月のフォローアップの後、RALES は早期に中止されました。治療群別の生存曲線を図 1に示します。
図 1: RALES における治療群別の生存率
スピロノラクトンは、プラセボと比較して死亡リスクを 30% 低下させました (p
スピロノラクトンはまた、心臓の原因 (心不全、狭心症、心室性不整脈、または心筋梗塞の悪化と定義) による入院のリスクを 30% 低減しました (p
一部のサブグループの死亡率ハザード比を図 2 に示します。死亡率に対するスピロノラクトンの好ましい効果は、55 歳未満の患者を除くすべての性別およびすべての年齢層で類似しているように見えました。 RALES には非白人が少なすぎて、人種による影響の違いについて結論を出すことができませんでした。スピロノラクトンの効果は、ベースラインの血清カリウム値が低い患者ほど大きく、駆出率が 0.2 未満の患者では小さかったようです。これらのサブグループ分析は慎重に解釈する必要があります。
図 2: RALES におけるサブグループ別の全死因死亡率のハザード比
図 2: 各ボックスのサイズは、サンプル サイズとイベント レートに比例します。 LVEF は左心室駆出率、Ser Creatinine は血清クレアチニン、Cr Clearance はクレアチニンクリアランス、ACEI はアンギオテンシン変換酵素阻害剤を表します。
患者情報
ALDACTONE を投与されている患者は、カリウムのサプリメントや、塩の代替物を含む高レベルのカリウムを含む食品を避けるようにアドバイスされるべきです.
