Brand Temovate 15g Clobetasol 使用法、副作用および投与量。 オンライン薬局の価格。 処方箋不要のジェネリック医薬品。
Temovate とは何ですか?また、どのように使用されますか?
Temovate は、歯垢および頭皮乾癬およびコルチコステロイド反応性皮膚病の症状を治療するために使用される処方薬です。テモベートは、単独で使用することも、他の薬と併用することもできます。
Temovate は、コルチコステロイド、局所と呼ばれる薬物のクラスに属します。
Temovate が 12 歳未満の子供に安全で有効であるかどうかはわかっていません。
Temovate の副作用の可能性は何ですか?
Temovate は、次のような重大な副作用を引き起こす可能性があります。
- 肌状態の悪化、
- 治療を受けた皮膚の発赤、熱感、腫れ、にじみ、または重度の刺激、
- ぼやけた視界、
- 視野狭窄、
- 眼の痛み、
- ライトの周りにハローが見える
- 喉の渇きが増し、
- 口渇、
- フルーティーな口臭、
- 顔と肩の体重増加、
- 傷の治りが遅く、
- 皮膚の変色、
- 皮膚が薄くなる、
- 体毛が増え、
- 疲れ、
- 気分の変化、
- 月経の変化、および
- 性的変化
上記の症状がある場合は、すぐに医療機関を受診してください。
Temovate の最も一般的な副作用は次のとおりです。
- 治療した皮膚の灼熱感、かゆみ、腫れ、刺激、
- 肌の乾燥やひび割れ、
- 毛包の周りの赤みや痂皮、
- 蜘蛛の巣、
- ストレッチマーク、
- 皮膚が薄くなる、
- 発疹や蕁麻疹、
- にきび、および
- 一時的な脱毛
気になる副作用や治らない副作用がある場合は、医師に相談してください。
これらは Temovate の考えられるすべての副作用ではありません。詳細については、医師または薬剤師にお尋ねください。
副作用に関する医学的アドバイスについては、医師に連絡してください。 1-800-FDA-1088 で副作用を FDA に報告できます。
説明
TEMOVATE® (プロピオン酸クロベタゾール クリームおよび軟膏) クリームおよび軟膏、0.05% には、局所皮膚科用の合成コルチコステロイドである活性化合物プロピオン酸クロベタゾールが含まれています。プレドニゾロンの類似体であるクロベタゾールは、高度のグルココルチコイド活性とわずかなミネラルコルチコイド活性を持っています。
化学的に、プロピオン酸クロベタゾールは (11β,16β)-21-クロロ-9-フルオロ-11-ヒドロキシ-16-メチル-17-(1-オキソプロポキシ)-プレグナ-1,4-ジエン-3,20-ジオンであり、次の構造式があります。
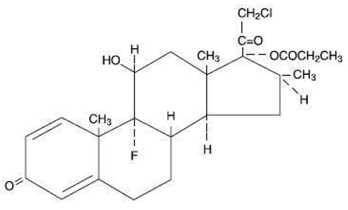
プロピオン酸クロベタゾールの分子式は C25H32CIFO5 で、分子量は 467 です。白色からクリーム色の結晶性粉末で、水に不溶です。
TEMOVATE®クリームには、プロピレングリコール、モノステアリン酸グリセリル、セトステアリルアルコール、ステアリン酸グリセリル、ステアリン酸PEG 100、ホワイトワックス、クロロクレゾール、クエン酸ナトリウム、クエン酸一水和物、および精製水のクリームベースに、プロピオン酸クロベタゾール0.5mg/gが含まれています。
TEMOVATE® 軟膏には、プロピレングリコール、セスキオレイン酸ソルビタン、および白色ワセリンをベースにプロピオン酸クロベタゾール 0.5 mg/g が含まれています。
適応症
TEMOVATE® クリームと軟膏は、コルチコステロイド反応性皮膚疾患の炎症性およびそう痒症状の緩和を目的とした超高効能のコルチコステロイド製剤です。連続 2 週間を超える治療は推奨されず、薬物が視床下部-下垂体-副腎 (HPA) 軸を抑制する可能性があるため、総投与量は 50 g/週を超えてはなりません。 12 歳未満の小児患者への使用は推奨されません。
他の高活性コルチコステロイドと同様に、コントロールが達成されたら治療を中止する必要があります。 2 週間以内に改善が見られない場合は、診断の再評価が必要になる場合があります。
投薬と管理
テモベート® クリームまたは軟膏を 1 日 2 回、患部の皮膚に薄く塗り、やさしく完全になじませます (参照)。 適応症と使用法 )。
TEMOVATE® クリームと軟膏は、超高効能の局所用コルチコステロイドです。したがって、 治療は連続 2 週間に制限する必要があり、50 g/週を超える量は使用しないでください。
他の高活性コルチコステロイドと同様に、コントロールが達成されたら治療を中止する必要があります。 2 週間以内に改善が見られない場合は、診断の再評価が必要になる場合があります。
TEMOVATE® クリームおよび軟膏は、閉塞性包帯には使用しないでください。
高齢者の使用
高齢患者(65 歳以上)を対象とした研究では、 予防 TEMOVATE® クリームまたは軟膏で治療された場合、安全性は若い患者と変わらなかった。したがって、投与量の調整は推奨されません。
供給方法
TEMOVATE® (プロピオン酸クロベタゾールクリーム) クリーム、0.05% で提供されます:
30gチューブ( NDC 10337-163-30)、および 60 g チューブ ( NDC 10337-163-60)。
TEMOVATE® (プロピオン酸クロベタゾール軟膏) 軟膏、0.05% は以下で供給されます。
15gチューブ( NDC 10337-162-15)、および 30 g チューブ ( NDC 10337-162-30)。
15°~30°C (59°~86°F) で保管してください。 TEMOVATE® Cream は冷蔵しないでください。ファーマダーム
Fougera Pharmaceuticals Inc.、Melville、NY 11747 USAの一部門。改訂: 2012 年 1 月
副作用
対照臨床試験では、テモベイト® クリームについて報告された最も頻繁な副作用は、治療を受けた患者の 1% での灼熱感と刺痛感でした。頻度の低い有害反応は、かゆみ、皮膚萎縮、および皮膚のひび割れおよび亀裂であった.
対照臨床試験では、テモベート軟膏について報告された最も頻繁な有害事象は、治療を受けた患者の 0.5% で灼熱感、刺激感、かゆみでした。頻度の低い副作用は、ヒリヒリ感、ひび割れ、紅斑、毛嚢炎、指のしびれ、皮膚萎縮、毛細血管拡張症でした。
クッシング症候群は、局所プロピオン酸クロベタゾール製剤の長期使用の結果として、乳児および成人で報告されています。
次の追加の局所副反応は、局所コルチコステロイドで報告されており、密閉包帯やより強力なコルチコステロイドを使用すると、より頻繁に発生する可能性があります.これらの反応は、おおよそ発生の少ない順にリストされています: 乾燥、座瘡様発疹、色素沈着低下、口周囲皮膚炎、アレルギー性接触皮膚炎、二次感染、炎症、線条、粟粒。

薬物相互作用
情報が提供されていません。
警告
情報が提供されていません。参照してください 注意事項 以下のセクション。
予防
全般的
テモベイト® クリームおよび軟膏は、酒さまたは口囲皮膚炎の治療には使用しないでください。また、顔、鼠径部、または腋窩には使用しないでください。
局所コルチコステロイドの全身吸収は、治療からの離脱後にグルココルチコステロイド不足の可能性を伴う、可逆的な HPA 軸抑制を引き起こす可能性があります。一部の患者では、治療中の局所コルチコステロイドの全身吸収によって、クッシング症候群、高血糖症、および糖尿病の症状が生じることもあります。
広い表面積または閉塞下の領域に局所ステロイドを適用している患者は、HPA 軸抑制の証拠について定期的に評価する必要があります。これは、ACTH 刺激、AM プラズマ コルチゾール、および尿中遊離コルチゾール テストを使用して行うことができます。超強力なコルチコステロイドを投与されている患者は、一度に 2 週間を超えて治療するべきではなく、HPA 抑制のリスクが高まるため、一度に小さな領域のみを治療する必要があります。
TEMOVATE® クリームおよび軟膏は、湿疹患者に 1 週間 2 g/日の低用量で使用した場合、HPA 軸の抑制をもたらしました。
HPA 軸の抑制が認められた場合は、薬剤の使用を中止するか、使用頻度を減らすか、より効果の低いコルチコステロイドに置き換えることを試みる必要があります。 HPA 軸機能の回復は、通常、局所コルチコステロイドの中止により迅速に行われます。まれに、グルココルチコステロイド不足の徴候や症状が発生し、全身性コルチコステロイドの補充が必要になることがあります。全身補充に関する情報については、それらの製品の処方情報を参照してください。
小児患者は、皮膚表面と体重の比率が大きいため、同等の用量からの全身毒性の影響を受けやすくなる可能性があります( 予防 : 小児用 )。
刺激が生じた場合は、TEMOVATE® クリームと軟膏の使用を中止し、適切な治療を開始する必要があります。コルチコステロイドによるアレルギー性接触皮膚炎は、通常、コルチコステロイドを含まないほとんどの局所用製品のように臨床的増悪に注意するのではなく、治癒の失敗を観察することによって診断されます.このような観察結果は、適切な診断パッチ テストで裏付けられる必要があります。
付随する皮膚感染症が存在するか発症した場合は、適切な抗真菌剤または抗菌剤を使用する必要があります。良好な反応がすぐに得られない場合は、感染が適切に制御されるまで、テモベイト® クリームおよび軟膏の使用を中止する必要があります。
臨床検査
以下の検査は、患者の HPA 軸抑制の評価に役立つ場合があります。
ACTH 刺激試験 AM 血漿コルチゾール試験 尿中遊離コルチゾール試験
発がん、突然変異誘発、生殖能力の障害
プロピオン酸クロベタゾールの発がん性を評価するための長期動物実験は実施されていません。
50 mcg/kg/日までの用量レベルでの皮下投与後のラットでの研究は、雌が最高用量で吸収胚の数の増加と生きている胎児の数の減少を示したことを明らかにした。
プロピオン酸クロベタゾールは、Ames 試験、Saccharomyces cerevisiae 遺伝子変換試験、および E. coli B WP2 変動試験の 3 つの異なる試験系で非変異原性でした。
妊娠
催奇形性効果
妊娠カテゴリーC。 コルチコステロイドは、比較的低用量レベルで全身投与された場合、実験動物で催奇形性があることが示されています。いくつかのコルチコステロイドは、実験動物への皮膚適用後に催奇形性であることが示されています.
プロピオン酸クロベタゾールは、局所適用した場合の催奇形性についてテストされていません。しかし、それは経皮的に吸収され、皮下投与された場合、ウサギとマウスの両方で重大な催奇形物質でした.プロピオン酸クロベタゾールは、効力の弱いステロイドよりも催奇形性の可能性が高い.
皮下経路を用いたマウスの催奇形性試験では、試験した最高用量 (1 mg/kg) で胎仔毒性が生じ、0.03 mg/kg まで試験したすべての用量レベルで催奇形性が生じました。これらの用量は、それぞれヒトの TEMOVATE® クリームおよび軟膏の局所用量の約 1.4 倍および 0.04 倍です。見られた異常には、口蓋裂および骨格異常が含まれていました。
ウサギでは、プロピオン酸クロベタゾールは 3 および 10 mcg/kg の用量で催奇形性を示した。これらの用量は、それぞれヒトの TEMOVATE® クリームおよび軟膏の局所用量の約 0.02 倍および 0.05 倍です。見られた異常には、口蓋裂、頭蓋分離症、およびその他の骨格異常が含まれていました。
妊娠中の女性におけるプロピオン酸クロベタゾールの催奇形性の可能性に関する十分に管理された研究はありません。 TEMOVATE® クリームおよび軟膏は、潜在的な利益が胎児への潜在的なリスクを正当化する場合にのみ、妊娠中に使用する必要があります。
授乳中の母親
全身投与されたコルチコステロイドは母乳に含まれており、成長を抑制したり、内因性のコルチコステロイド産生を妨害したり、その他の有害な影響を引き起こす可能性があります.コルチコステロイドの局所投与が、母乳で検出可能な量を生成するのに十分な全身吸収をもたらすかどうかは不明です.多くの薬物が母乳中に排泄されるため、授乳中の女性に TEMOVATE® クリームまたは軟膏を投与する場合は注意が必要です。
小児用
小児患者における TEMOVATE® クリームおよび軟膏の安全性と有効性は確立されていません。 12 歳未満の小児患者への使用は推奨されません。体重に対する皮膚表面積の比率が高いため、小児患者は、局所コルチコステロイドで治療されている場合、成人よりも HPA 軸抑制およびクッシング症候群のリスクが高くなります。したがって、治療中または治療中止後に副腎不全になるリスクも高くなります。乳児および小児における局所コルチコステロイドの不適切な使用により、線条を含む悪影響が報告されています。
HPA 軸抑制、クッシング症候群、線形成長遅延、体重増加の遅延、および頭蓋内圧亢進が、局所コルチコステロイドを受けている小児で報告されています。小児における副腎抑制の徴候には、血漿コルチゾール値の低下と ACTH 刺激に対する反応の欠如が含まれます。頭蓋内圧亢進症の症状には、泉門の隆起、頭痛、および両側性乳頭浮腫が含まれます。
高齢者の使用
65 歳以上の限られた数の患者が、米国および米国以外の臨床試験で TEMOVATE® クリーム (n = 231) および TEMOVATE® 軟膏 (n = 101) で治療されています。有効性と安全性を個別に分析するには患者数が少なすぎますが、この集団で報告された副作用は、若い患者で報告されたものと同様でした。利用可能なデータに基づくと、高齢患者における TEMOVATE® クリームおよび軟膏の投与量の調整は保証されていません。
過剰摂取
局所的に適用された TEMOVATE® クリームおよび軟膏は、全身効果を生み出すのに十分な量で吸収されます ( 予防 )。
禁忌
TEMOVATE® (プロピオン酸クロベタゾール クリームおよび軟膏) クリームおよび軟膏、0.05% は、製剤のいずれかの成分に対する過敏症の既往歴のある患者には禁忌です。
臨床薬理学
他の局所コルチコステロイドと同様に、プロピオン酸クロベタゾールには、抗炎症、鎮痒、および血管収縮の特性があります。一般に、局所ステロイドの抗炎症活性の機序は不明である。しかし、コルチコステロイドは、総称してリポコルチンと呼ばれるホスホリパーゼ A2 阻害タンパク質の誘導によって作用すると考えられています。これらのタンパク質は、共通の前駆体であるアラキドン酸の放出を阻害することにより、プロスタグランジンやロイコトリエンなどの炎症の強力なメディエーターの生合成を制御すると考えられています。アラキドン酸は、ホスホリパーゼ A2 によって膜リン脂質から放出されます。
薬物動態
局所コルチコステロイドの経皮吸収の程度は、ビヒクルや表皮バリアの完全性など、多くの要因によって決まります。最大 24 時間のヒドロコルチゾンによる閉塞包帯は、浸透を増加させることが実証されていません。しかし、ヒドロコルチゾンを 96 時間閉塞させると、浸透が著しく促進されます。局所コルチコステロイドは、正常な無傷の皮膚から吸収できます。皮膚の炎症および/またはその他の疾患プロセスにより、経皮吸収が増加する場合があります。
TEMOVATE®クリームと軟膏で行われた研究は、他の局所コルチコステロイドと比較して、それらが非常に高い範囲の効能にあることを示しています.
患者情報
局所コルチコステロイドを使用している患者は、次の情報と指示を受ける必要があります。
