Uniphyl 400mg Theophylline 使用法、副作用および投与量。 オンライン薬局の価格。 処方箋不要のジェネリック医薬品。
ユニフィル400mgとは?
Uniphyl は、喘息、気管支炎、肺気腫、およびその他の呼吸障害 (急性気管支痙攣) の症状を治療するために使用される処方薬です。ユニフィル 400mg は、単独で使用することも、他の薬と併用することもできます。
ユニフィルは、キサンチン誘導体と呼ばれる薬物のクラスに属しています。ホスホジエステラーゼ酵素阻害剤、非選択的。
Uniphyl 400mg が生後 1.5 か月未満の子供に安全で効果的かどうかはわかっていません。
ユニフィルの副作用は?
ユニフィルは、次のような重大な副作用を引き起こす可能性があります。
- 蕁麻疹、
- 呼吸困難、
- 顔、唇、舌、喉の腫れ、
- 重度または進行中の嘔吐、
- 継続する頭痛、
- 寝られない、
- 急速な心拍、
- 発作、
- 熱、
- 足のけいれん、
- 便秘、
- 不規則な心拍、
- 胸の中でときめき、
- 喉の渇きや排尿の増加、
- しびれやうずき、
- 筋力低下、
- ぐったり感、
- 喉の渇きが増し、
- 排尿の増加、
- ドライマウスと
- フルーティーな口臭
上記の症状がある場合は、すぐに医療機関を受診してください。
ユニフィルの最も一般的な副作用は次のとおりです。
- 吐き気、
- 嘔吐、
- 下痢、
- 頭痛、
- 睡眠障害(不眠症)、
- 震え、
- 発汗、
- 落ち着きのなさ、そして
- 過敏性
気になる副作用や治らない副作用がある場合は、医師に相談してください。
これらは、Uniphyl の考えられるすべての副作用ではありません。詳細については、医師または薬剤師にお尋ねください。
副作用に関する医学的アドバイスについては、医師に連絡してください。 1-800-FDA-1088 で副作用を FDA に報告できます。
説明
Uniphyl (テオフィリン無水錠) ® (テオフィリン、無水) 制御放出システムの錠剤は、適切な患者に対して 24 時間の投与間隔を可能にします。
テオフィリンは構造的にメチルキサンチンに分類されます。白色、無臭、苦味のある結晶性の粉末です。
無水テオフィリンは、1H-プリン-2,6-ジオン、3,7-ジヒドロ-1,3-ジメチル-という化学名を持ち、次の構造式で表されます。
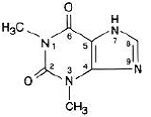
無水テオフィリンの分子式は C7H8N4O2 で、分子量は 180.17 です。
経口投与用の各制御放出錠剤には、400 mg または 600 mg の無水テオフィリンが含まれています。
不活性成分:セトステアリルアルコール、ヒドロキシエチルセルロース、ステアリン酸マグネシウム、ポビドン、タルク。
適応症
テオフィリンは、慢性喘息および他の慢性肺疾患、例えば肺気腫および慢性気管支炎に関連する症状および可逆的な気流閉塞の治療に適応される。
投薬と管理
ユニフィル(テオフィリン無水錠) ® 400mgまたは600mg錠 1日1回朝晩服用できます。ユニフィル(テオフィリン無水錠剤)は食事と一緒に服用することをお勧めします。 Uniphyl (テオフィリン無水錠剤) を食物と一緒に摂取することを選択した場合、一貫して食物と一緒に摂取する必要があり、絶食状態で摂取する場合は、定期的に絶食して摂取する必要があることを患者にアドバイスする必要があります。製品を服用するときはいつでも、食物の有無にかかわらず一貫して服用することが重要です.
Uniphyl (テオフィリン無水錠剤) ® 錠剤は、毒性の可能性があるテオフィリンが急速に放出される可能性があるため、噛んだり、砕いたりしないでください。スコアリングされたタブレットは分割される場合があります。まれに、Uniphyl (テオフィリン無水錠剤) 400 mg または 600 mg 錠剤を投与されている患者は、便中または人工肛門を介して無傷のマトリックス錠剤を排出することがあります。これらのマトリックス錠剤には通常、残留テオフィリンがほとんどまたはまったく含まれていません。
即時放出または制御放出テオフィリン製品を服用している 12 歳以上の安定した患者は、400 mg または 600 mg の Uniphyl (テオフィリン無水錠剤) の 1 日 1 回投与に移行することができます。 mgベース。
1 日 1 回の投与で得られる血清テオフィリン レベルのピークとトラフは、以前の製品やレジメンで得られたものとは異なる可能性があることを認識しておく必要があります。
一般的な考慮事項
定常状態のピーク血清テオフィリン濃度は、個々の患者における用量、投与間隔、およびテオフィリンの吸収とクリアランスの速度の関数です。テオフィリンクリアランスの速度には著しい個人差があるため、テオフィリンクリアランスを変化させることが知られている因子(例、 60 歳未満の成人では 400 ~ 1600 mg/日、1 ~ 9 歳の子供では 10 ~ 36 mg/kg/日)。特定の集団に対して、すべての患者に安全かつ効果的な血清濃度の両方を提供する単一のテオフィリン用量はありません.特定の集団で治療的血清テオフィリン濃度を達成するために必要なテオフィリン用量の中央値を投与すると、個々の患者の血清テオフィリン濃度が治療量以下または潜在的に毒性のいずれかになる可能性があります。たとえば、60 歳未満の成人で 900 mg/日、1 ~ 9 歳の子供で 22 mg/kg/日の用量では、約 30% の患者で定常状態のピーク血清テオフィリン濃度が テオフィリンの用量は、副作用のリスクを最小限に抑えて最大の潜在的利益をもたらす用量を達成するために、ピーク血清テオフィリン濃度の測定値に基づいて個別化する必要があります.
ほとんどの患者では、十分に低い用量から始めて、臨床的に必要であると判断された場合は少しずつ用量を徐々に増やしていくことで、一過性のカフェイン様の有害作用および代謝の遅い患者における過剰な血清濃度を回避することができます (参考文献を参照)。用量の増加は、以前の用量が十分に許容され、血清テオフィリン濃度が新しい定常状態に達するのを可能にするために3日以上の間隔で行われる場合にのみ行われるべきです.投与量の調整は、血清テオフィリン濃度の測定によってガイドする必要があります。 予防 、 臨床検査 と 投薬と管理 、 )。医療提供者は、患者と介護者に、副作用を引き起こす投与を中止し、これらの症状がなくなるまで投薬を中止し、その後、以前に許容されたより低い投与量で治療を再開するように指示する必要があります。 警告 )。
患者の症状が十分に管理されている場合、明らかな悪影響はなく、投与量の要件を変更する可能性のある介入要因もありません (以下を参照)。 警告 と 予防 )、血清テオフィリン濃度は、急速に成長している子供については6か月間隔で、その他のすべての子供については1年間隔で監視する必要があります.急性疾患の患者では、血清テオフィリン濃度を頻繁に、たとえば 24 時間ごとに監視する必要があります。
テオフィリンは体脂肪にほとんど分布しないため、mg/kg の用量は理想体重に基づいて計算する必要があります。
表 V には、さまざまな年齢層および臨床状況の患者に推奨されるテオフィリンの用量調節スキーマが含まれています。
表 VI には、血清テオフィリン濃度に基づいたテオフィリン用量調整の推奨事項が含まれています。 これらの一般的な推奨用量を個々の患者に適用するには、各患者に固有の臨床的特徴を考慮に入れる必要があります。一般に、これらの推奨事項は、血清テオフィリン濃度の予想外の大幅な増加に関連する潜在的に深刻な有害事象のリスクを減らすために、用量調整の上限として役立つはずです.
B.クリアランス障害の危険因子を持つ患者、高齢者(> 60歳)、および血清テオフィリン濃度を監視することが現実的でない患者:
12~15 歳の小児では、テオフィリンクリアランス低下の危険因子が存在する場合、テオフィリンの用量は 16 mg/kg/日を超えてはならず、最大 400 mg/日までとする必要があります (以下を参照)。 警告 )または血清テオフィリン濃度を監視することが現実的でない場合。
16 歳以上の青年および高齢者を含む成人では、テオフィリン クリアランス低下の危険因子がある場合、テオフィリンの用量は 400 mg/日を超えてはならない( 警告 )または血清テオフィリン濃度を監視することが現実的でない場合。
*代謝が速く、臨床的に必要な用量が平均より多い患者は、次の用量の前に低トラフ濃度に起因する突出症状を防ぐために、より少ない用量をより頻繁に (12 時間ごとに) 受ける必要があります。
表VI.血清テオフィリン濃度に基づいた用量調整。
供給方法
Uniphyl® (テオフィリン、無水) 放出制御錠 400 mg 100錠( NDC 67781-251-01) または 500 錠 ( NDC 67781-251-05)。 400 mg の丸型の白い錠剤には、スコアのある面に PF の記号、反対側に U400 の記号が付いています。
Uniphyl® (テオフィリン、無水) 放出制御錠 600 mg 100錠( NDC 67781-252-01)。長方形の凹型の白い 600 mg 錠剤はそれぞれ、刻線のある面に PF の記号、反対側に U 600 の記号が付いています。
25°C (77°F) で保管してください。 15° ~ 30°C (59° ~ 86°F) の間で許容されます。
遮光性の密閉容器に分注してください。
Purdue Pharmaceutical Products LP、ディストリクト。 by: Purdue Pharmaceutical Products LP、スタンフォード、CT 06901-3431。 2004 年 3 月 17 日。
副作用
テオフィリンに関連する副作用は、ピーク血清テオフィリン濃度が 20 mcg/mL 未満の場合は一般に軽度であり、主に吐き気、嘔吐、頭痛、不眠症などの一時的なカフェイン様の副作用で構成されます。しかし、最高血清テオフィリン濃度が 20 mcg/mL を超えると、テオフィリンは、持続的な嘔吐、心不整脈、および致死的な難治性発作など、さまざまな有害反応を引き起こします。 過剰摂取 )。一過性のカフェイン様の有害反応は、テオフィリン療法が推奨される初期用量よりも高い用量で開始された患者の約 50% で発生します (例、成人では > 300 mg/日、> 1 歳以上の子供では > 12 mg/kg/日)。 )。テオフィリン療法の開始時に、特に学齢期の子供では、カフェインのような副作用が一時的に患者の行動を変える可能性がありますが、この反応が持続することはめったにありません.低用量でテオフィリン療法を開始し、続いて所定の年齢に応じた最大用量までゆっくりと漸増することで、これらの一過性の副作用の頻度が大幅に減少します( 投薬と管理 、 )。ごく一部の患者 (小児の 3% 未満、成人の 10% 未満) では、治療範囲 (すなわち、10-20 mcg/mL) 内のピーク血清テオフィリン濃度でも、カフェイン様の副作用が維持療法中に持続します。 .用量を減らすことで、これらの患者のカフェイン様の副作用が緩和される可能性がありますが、副作用が持続する場合は、継続的なテオフィリン療法の必要性と、代替治療の潜在的な治療効果を再評価する必要があります。
血清テオフィリン濃度が 20 mcg/mL 未満で報告されているその他の副作用には、下痢、過敏症、落ち着きのなさ、細かい骨格筋の振戦、一過性の利尿などがあります。 COPD に続発する低酸素症の患者では、血清テオフィリン濃度 ≥ 15 mcg/mL で多発性心房性頻脈および粗動が報告されています。基礎に神経疾患を有する患者または高齢患者において、血清テオフィリン濃度が 20 mcg/mL 未満で発作が発生したという報告がいくつかあります。血清テオフィリン濃度が 20 mcg/mL 未満の高齢患者における発作の発生は、タンパク質結合の減少に続発する可能性があり、その結果、薬理学的に活性な非結合型の総血清テオフィリン濃度の割合が高くなります。血清テオフィリン濃度が 20 mcg/mL 未満の患者で報告された発作の臨床的特徴は、過剰摂取による過剰な血清テオフィリン濃度に関連する発作よりも一般的に軽度でした (すなわち、それらは一般に一過性であり、しばしば抗けいれん療法なしで停止し、神経学的遺残には至らなかった)。
表 IV。テオフィリン中毒の症状。 *
薬物相互作用
テオフィリンは、さまざまな薬物と相互作用します。相互作用は、薬力学的、すなわち、テオフィリンまたは別の薬物に対する治療応答の変化、または血清テオフィリン濃度の変化を伴わない副作用の発生であり得る。しかしながら、より頻繁には、相互作用は薬物動態的である。すなわち、テオフィリンクリアランスの速度が別の薬物によって変化し、血清テオフィリン濃度が上昇または低下する。テオフィリンが他の薬物の薬物動態を変化させることはめったにありません。表 II に挙げた薬剤は、テオフィリンとの臨床的に重要な薬力学的または薬物動態学的相互作用を生み出す可能性があります。表IIの「効果」列の情報は、相互作用する薬物が定常状態のテオフィリンレジメンに追加されていることを前提としています。テオフィリンクリアランスを阻害する薬(シメチジン、エリスロマイシンなど)をすでに服用している患者にテオフィリンを開始する場合、治療血清テオフィリン濃度を達成するために必要なテオフィリンの用量は少なくなります。逆に、テオフィリンクリアランスを高める薬(リファンピンなど)をすでに服用している患者にテオフィリンを開始する場合、治療血清テオフィリン濃度を達成するために必要なテオフィリンの用量はより多くなります。テオフィリンクリアランスを増加させる併用薬を中止すると、テオフィリンの用量を適切に減らさない限り、テオフィリンが潜在的に毒性のレベルまで蓄積することになります。テオフィリンのクリアランスを阻害する併用薬を中止すると、テオフィリンの用量を適切に増量しない限り、血清中のテオフィリン濃度が低下します。表 III に挙げた薬剤は、テオフィリンと相互作用しないことが証明されているか、臨床的に有意な相互作用を生じない (すなわち、テオフィリン クリアランスの変化が 15% 未満) ことが証明されています。
表 II と表 III の薬物リストは、1995 年 2 月 9 日現在のものです。テオフィリン、特に新しい化学物質との新しい相互作用が継続的に報告されています。 医療従事者は、表 II に記載されていない薬剤がテオフィリンと相互作用しないと想定すべきではありません。 テオフィリンを投与されている患者に新たに入手可能な薬を追加する前に、新薬の添付文書および/または医学文献を参照して、新薬とテオフィリンとの相互作用が報告されているかどうかを判断する必要があります。
表 II.テオフィリンとの臨床的に重要な薬物相互作用*
表 III.テオフィリンと相互作用しないことが実証されている薬物、またはテオフィリンと臨床的に有意な相互作用を生じない薬物。 *
薬と食物の相互作用
Uniphyl® 錠 (テオフィリン、無水) のバイオアベイラビリティは、食物との同時投与で研究されています。 3 つの単回投与研究では、Uniphyl (テオフィリン無水錠剤) 400 mg または 600 mg 錠剤と標準化された高脂肪食を与えられた被験者が絶食状態と比較されました。給餌条件下では、ピーク血漿濃度とバイオアベイラビリティが増加しました。しかし、吸収の速度と程度の急激な増加は明らかではありませんでした( 薬物動態、吸収 )。摂食条件下での吸収のピークと範囲の増加は、理想的には、食物の有無にかかわらず一貫して投与する必要があることを示唆しています。
テオフィリン血清濃度測定値に対する他の薬剤の影響
臨床で使用されているほとんどの血清テオフィリンアッセイは、テオフィリンに特異的なイムノアッセイです。カフェイン、ジフィリン、ペントキシフィリンなどの他のキサンチンは、これらのアッセイでは検出されません。ただし、一部の薬物 (例、セファゾリン、セファロチン) は、特定の HPLC 技術に干渉する可能性があります。新生児または腎機能障害のある患者のカフェインおよびキサンチン代謝物は、一部の乾燥試薬オフィスメソッドからの読み取り値が実際の血清テオフィリン濃度よりも高くなる可能性があります.
警告
併発疾患
テオフィリンは、併発する状態の悪化のリスクが高いため、次の臨床状態を持つ患者には細心の注意を払って使用する必要があります。
活動性消化性潰瘍疾患 発作性疾患 不整脈(徐脈性不整脈を除く)
テオフィリンクリアランスを低下させる条件
テオフィリンクリアランスの低下には、容易に特定できる原因がいくつかあります。 これらの危険因子が存在する状態で 1 日総投与量を適切に減らさないと、重度で致命的なテオフィリン中毒が発生する可能性があります。 テオフィリン使用の利点とリスク、および以下の危険因子を持つ患者における血清テオフィリン濃度のより集中的なモニタリングの必要性について慎重に検討する必要があります。
年
新生児 (正期産および未熟児) 1 歳未満の子供 高齢者 ( > 60 歳)
併発疾患
急性肺水腫 うっ血性心不全 肺性心熱; ≥ 102°で 24 時間以上;甲状腺機能低下症 肝臓病。肝硬変、急性肝炎 生後3ヶ月未満の乳児における腎機能の低下 多臓器不全を伴う敗血症 ショック
禁煙
薬物相互作用
テオフィリン代謝を阻害する薬剤(例,シメチジン,エリスロマイシン,タクリン)を追加するか,テオフィリン代謝を亢進する薬剤(例,カルバマゼピン,リファンピン)の同時投与を中止する。 (見る 注意事項: 薬物相互作用 、 )。
テオフィリン中毒の徴候または症状がある場合
テオフィリンを投与されている患者が吐き気や嘔吐、特に反復性の嘔吐、またはテオフィリン毒性と一致するその他の徴候や症状を発症した場合はいつでも (別の原因が疑われる場合でも)、テオフィリンの追加投与を差し控え、血清テオフィリン濃度を直ちに測定する必要があります。 副作用を引き起こす用量を継続しないように患者に指示し、症状が治まるまで次の用量を差し控えるように指示する必要があります。 投薬と管理 、 投与ガイドライン、表 VI )。
投与量の増加
慢性肺疾患の症状の急性増悪に対応してテオフィリンの用量を増やすべきではありません。この状況では、テオフィリンはベータ 2 選択的アゴニストの吸入と全身投与のコルチコステロイドにほとんど追加の利益をもたらさず、副作用のリスクを高めるからです。持続的な慢性症状に応じて用量を増加させる前に、定常状態の血清テオフィリン濃度のピークを測定して、用量の増加が安全かどうかを確認する必要があります。血清濃度が低いことに基づいてテオフィリンの用量を増やす前に、医療従事者は、血液サンプルが用量に関連して適切な時期に採取されたかどうか、および患者が処方されたレジメンを順守しているかどうかを検討する必要があります。 予防 、 臨床検査 )。
テオフィリンクリアランスの速度は用量依存的である可能性があるため(すなわち、定常状態の血清濃度は用量の増加に不釣り合いに増加する可能性がある)、治療量以下の血清濃度測定に基づく用量の増加は保守的であるべきである.一般に、用量の増加を以前の 1 日総用量の約 25% に制限すると、血清テオフィリン濃度が意図せず過剰に上昇するリスクが軽減されます ( 投薬と管理 、 )。
予防
全般的
テオフィリン治療の開始前、テオフィリン用量の増加前、およびフォローアップ中に、テオフィリンクリアランスを変更し、用量調整を必要とするさまざまな相互作用する薬物および生理学的状態を慎重に検討する必要があります。 警告 )。治療を開始するために選択するテオフィリンの用量は低くすべきであり、忍容性がある場合は、血清テオフィリン濃度と患者の臨床反応を監視することによって最終用量を導きながら、1週間以上にわたってゆっくりと増加させる必要があります。 投薬と管理 、 )。
血清テオフィリン濃度のモニタリング
血清テオフィリン濃度の測定値は容易に入手でき、投与量が適切かどうかを判断するために使用する必要があります。具体的には、血清テオフィリン濃度は次のように測定する必要があります。
用量の増加を導くために、予想される血清テオフィリン濃度のピーク時に血液サンプルを採取する必要があります。定常状態での夕方の投与の 12 時間後または朝の投与の 9 時間後。ほとんどの患者は、3 日間の投薬後に定常状態に達し、飲み忘れがなく、追加の投薬がなく、どの投薬も不均等な間隔で服用されていません。トラフ濃度 (すなわち、投与間隔の最後) は追加の有用な情報を提供せず、最高血清テオフィリン濃度が即時放出製剤のトラフ濃度よりも 2 倍以上高くなる可能性があるため、不適切な用量増加につながる可能性があります。 .夕方の投与から 12 時間以上、または朝の投与から 9 時間以上経過してから血清サンプルを採取した場合、濃度はピーク濃度を反映していない可能性があるため、結果は慎重に解釈する必要があります。対照的に、テオフィリン毒性の徴候または症状が存在する場合、血清サンプルをできるだけ早く採取し、直ちに分析し、結果を遅滞なく医療専門家に報告する必要があります。血清タンパク結合の低下が疑われる患者(肝硬変、妊娠後期の女性など)では、結合していないテオフィリンの濃度を測定し、結合していない濃度が 6~12 mcg/mL になるように投与量を調整する必要があります。テオフィリンの唾液濃度は、特別な技術なしに投与量を調整するために確実に使用することはできません.
臨床検査への影響
その薬理学的効果の結果として、血清濃度が 10 ~ 20 mcg/mL の範囲内のテオフィリンは、血漿グルコース (平均 88 mg% から 98 mg% へ)、尿酸 (平均 4 mg/dL から) を適度に増加させます。から 6 mg/dL)、遊離脂肪酸 (平均 451 μEq/L から 800 μEq/L まで)、総コレステロール (平均 140 対 160 mg/dL から)、HDL (平均 36 から 50 mg まで) /dL)、HDL/LDL 比 (平均 0.5 ~ 0.7)、および尿中遊離コルチゾール排泄 (平均 44 ~ 63 mcg/24 時間) 10 ~ 20 mcg/mL 範囲内の血清濃度でのテオフィリンまた、トリヨードチロニンの血清濃度を一時的に低下させる可能性があります (テオフィリンの前に 144、1 週間後に 131、4 週間後に 142 ng/dL). これらの変化の臨床的重要性は、個々の患者におけるテオフィリンの潜在的な治療上の利点と比較検討する必要があります.
発がん、突然変異誘発、および生殖能力の障害
長期発がん性試験は、マウス (経口投与量 30-150 mg/kg) およびラット (経口投与量 5-75 mg/kg) で実施されています。結果は保留中です。
テオフィリンは、エイムズ サルモネラ菌、in vivo および in vitro 細胞遺伝学、小核およびチャイニーズハムスター卵巣試験系で研究されており、遺伝毒性は示されていません。
14 週間の連続繁殖研究では、交配ペアの B6C3F1 マウスに 120、270、および 500 mg/kg の経口用量 (mg/m² ベースでヒトの用量の約 1.0 ~ 3.0 倍) を投与されたテオフィリンは、受胎能を損ないました。産仔あたりの生存児数の減少、受精ペアあたりの平均産仔数の減少、高用量での妊娠期間の増加、および中用量および高用量での生児出生率の減少。 13 週間の毒性試験では、テオフィリンを F344 ラットおよび B6C3F1 マウスに 40 ~ 300 mg/kg の経口用量で投与しました (mg/m² ベースでヒト用量の約 2.0 倍)。高用量では、両方の種で精巣重量の減少を含む全身毒性が観察された。
妊娠
催奇形性:カテゴリーC
器官形成期に妊娠中のマウス、ラット、ウサギに投与した研究では、テオフィリンは催奇形作用を引き起こしました。
マウスを用いた研究では、器官形成中の 100 mg/kg (mg/m² ベースで成人に推奨される最大経口投与量にほぼ等しい) を 1 回腹腔内投与すると、口蓋裂と指の異常が生じました。小顎症、小顎症、内反足、皮下血腫、開いたまぶた、および胚致死性が、mg/m² ベースで成人の最大推奨経口用量の約 2 倍の用量で観察されました。
受胎から器官形成まで投与されたラットを用いた研究では、150mg/kg/日(mg/m²ベースで成人の最大推奨経口投与量の約2倍)の経口投与で指の異常が生じました。胎児死亡率は、200 mg/kg/日の皮下投与量で観察されました (mg/m² ベースで成人の最大推奨経口投与量の約 4 倍)。妊娠中のウサギに器官形成全体にわたって投与した研究では、60 mg/kg/日の静脈内投与 (mg/m² ベースで成人の最大推奨経口投与量の約 2 倍) で、1 頭の雌が死亡し、臨床的に他の徴候は、口蓋裂を引き起こし、胚致死でした。 15 mg/kg/日以上の用量 (mg/m² ベースで成人の最大推奨経口用量未満) では、骨格変異の発生率が増加しました。
妊娠中の女性を対象とした、十分に管理された研究はありません。テオフィリンは、潜在的な利益が胎児への潜在的なリスクを正当化する場合にのみ、妊娠中に使用する必要があります。
授乳中の母親
テオフィリンは母乳に排泄され、授乳中の乳児に過敏性またはその他の軽度の毒性の兆候を引き起こす可能性があります.母乳中のテオフィリンの濃度は、母体の血清濃度とほぼ同じです。テオフィリン 10 ~ 20 mcg/mL を含む母乳 1 リットルを 1 日あたり摂取する乳児は、1 日あたり 10 ~ 20 mg のテオフィリンを摂取する可能性があります。母親が有毒な血清テオフィリン濃度を持っていない限り、乳児に深刻な悪影響が及ぶ可能性は低い.
小児用
テオフィリンは、小児患者の承認された適応症に対して安全で効果的です。小児患者では、テオフィリンのクリアランス率が小児の年齢範囲全体で大きく変動するため、テオフィリンの維持用量は慎重に選択する必要があります (以下を参照)。 臨床薬理学 、 、 警告 、 と 投薬と管理 、 )。
高齢者の使用
高齢患者は、加齢に伴う薬物動態および薬力学的変化により、若い患者よりもテオフィリンによる深刻な毒性を経験するリスクが大幅に高くなります。テオフィリンのクリアランスは、健康な若年成人と比較して、健康な高齢者 (> 60 歳) では平均 30% 減少します。テオフィリンクリアランスは、高齢者に蔓延する付随疾患によってさらに低下する可能性があり、この疾患はこの薬物のクリアランスをさらに損ない、血清レベルと潜在的な毒性を増加させる可能性があります。これらの状態には、腎機能障害、慢性閉塞性肺疾患、うっ血性心不全、肝疾患、および特定の医薬品の使用率の増加が含まれます( 予防 : 薬物相互作用 薬物動態学的および薬力学的相互作用の可能性があります。高齢者ではタンパク質結合が低下し、その結果、薬理学的に活性な非結合型の総血清テオフィリン濃度の割合が増加する可能性があります。高齢患者は、若い患者よりも慢性的な過剰摂取後のテオフィリンの毒性効果に対してより敏感であるようにも思われる.高齢患者では、減量と血清テオフィリン濃度の頻繁なモニタリングに注意が必要です( 予防 、 血清テオフィリン濃度のモニタリング 、 と 投薬と管理 )。
60 歳以上の患者のテオフィリンの 1 日最大用量は、患者が引き続き症状を示し、定常状態のピーク血清テオフィリン濃度が 投薬と管理 )。 400 mg/日を超えるテオフィリンの用量は、高齢患者には注意して処方する必要があります。
過剰摂取
全般的
テオフィリンの過剰摂取の慢性性とパターンは、毒性、管理、および結果の臨床症状に大きく影響します。 2 つの一般的な症状があります: (1) 急性の過剰摂取、すなわち、自殺未遂または孤立した投薬ミスの状況で発生するような、1 回の大量過剰摂取 (> 10 mg/kg)、および (2) 慢性的な過剰摂取、すなわち、患者のテオフィリンクリアランス率に対して過剰な反復投与の摂取。慢性的なテオフィリンの過剰摂取の最も一般的な原因には、患者または介護者の投薬ミス、テオフィリンクリアランスの速度を低下させることが知られている要因の存在下での過剰な用量または通常の用量の医療専門家の処方、および増悪に応じた用量の増加が含まれます。最初に血清テオフィリン濃度を測定して用量の増加が安全かどうかを判断することなく、症状を緩和します。
テオフィリンの過剰摂取による重度の毒性は、比較的まれな出来事です。ある健康維持組織では、テオフィリンの慢性的な過剰摂取による入院の頻度は、曝露 1000 人年当たり約 1 でした。別の研究では、何らかの理由で救急部門で治療を受けた患者から血清テオフィリン濃度の測定のために採取された 6000 の血液サンプルのうち、7% が 20 ~ 30 mcg/mL の範囲にあり、3% が > 30 mcg/mL でした。血清テオフィリン濃度が 20 ~ 30 mcg/mL の範囲にある患者の約 3 分の 2 は、1 つまたは複数の毒性症状を示しましたが、血清テオフィリン濃度が 30 mcg/mL を超える患者の > 90% は臨床的に中毒状態でした。同様に、他の報告では、テオフィリンによる重篤な毒性は、主に血清濃度 > 30 mcg/mL で見られます。
いくつかの研究は、テオフィリンの過剰摂取の臨床症状を説明し、生命を脅かす毒性を予測する要因を決定しようとしました.一般に、ピーク血清テオフィリン濃度が > 100 mcg/mL でない限り、急性過剰摂取を経験した患者は、慢性過剰摂取を経験した患者よりも発作を経験する可能性が低くなります。慢性的な過剰摂取の後、血清テオフィリン濃度が 30 mcg/mL を超えると、全身発作、生命を脅かす心不整脈、および死亡が発生する可能性があります。慢性的な過剰摂取後の毒性の重症度は、血清テオフィリン濃度のピークよりも患者の年齢と強く相関しています。 60 歳以上の患者は、慢性的な過剰摂取による重度の毒性と死亡のリスクが最も高くなります。既存疾患または併発疾患も、特定の毒性症状に対する患者の感受性を有意に高める可能性があります。たとえば、神経障害のある患者は発作のリスクが高く、心疾患の患者は一定の血清テオフィリン濃度に対して心不整脈のリスクが高くなります。基礎疾患のない患者さんへ。
過剰摂取の様式に応じたテオフィリン過剰摂取の様々な報告された発現の頻度を表IVに列挙する。テオフィリン毒性のその他の徴候には、血清カルシウム、クレアチンキナーゼ、ミオグロビンおよび白血球数の増加、血清リン酸およびマグネシウムの減少、急性心筋梗塞、および閉塞性尿路疾患の男性における尿閉が含まれます。血清テオフィリン濃度が 30 mcg/mL を超える発作は、しばしば抗けいれん療法に耐性があり、迅速に制御しないと不可逆的な脳損傷を引き起こす可能性があります。テオフィリン中毒による死亡は、ほとんどの場合、心肺停止および/または長期にわたる全身性発作または血行動態障害を引き起こす難治性心不整脈に続く低酸素性脳症に続発します。
過剰摂取管理
テオフィリンの過剰摂取または血清テオフィリン濃度 > 30 mcg/mL の症状を有する患者に対する一般的な推奨事項 (注: 血清テオフィリン濃度は、患者が医療機関を受診した後も上昇し続ける可能性があります。)
治療を開始すると同時に、地域の毒物センターに連絡して、最新の情報と以下の推奨事項を個別化するためのアドバイスを入手してください。
静脈アクセスの確立、気道の維持、心電図モニタリングなどの支持療法を開始します。
発作の治療
テオフィリン誘発発作に関連する罹患率と死亡率が高いため、治療は迅速かつ積極的に行う必要があります。抗けいれん療法は、発作が止まるまで、1~3 分ごとに 0.1~0.2 mg/kg ずつ増加するジアゼパムなどのベンゾジアゼピンの静脈内投与で開始する必要があります。反復発作は、負荷量のフェノバルビタール (20 mg/kg を 30 ~ 60 分かけて注入) で治療する必要があります。ヒトおよび動物研究におけるテオフィリンの過剰摂取の症例報告は、フェニトインがテオフィリン誘発性の発作を止めるのに効果がないことを示唆しています.テオフィリンによる発作を止めるのに必要なベンゾジアゼピンとフェノバルビタールの投与量は、重度の呼吸抑制または呼吸停止を引き起こす可能性のある投与量に近いです。したがって、医療従事者は補助換気を提供する準備をしておく必要があります。高齢者や COPD 患者は、抗けいれん薬の呼吸抑制効果の影響を受けやすい可能性があります。バルビツレートによる昏睡または全身麻酔の投与は、反復発作またはてんかん重積を終結させるために必要となる場合があります。フッ素化揮発性麻酔薬は、テオフィリンによって放出される内因性カテコールアミンに対して心筋を過敏にする可能性があるため、テオフィリン過剰摂取の患者では全身麻酔を慎重に使用する必要があります。エンフルランは、ハロタンよりもこの効果に関連する可能性が低く、したがってより安全である可能性があります.神経筋遮断薬は、脳内の発作活動を停止させることなく筋骨格症状を消失させるため、発作を停止させるために単独で使用すべきではありません。
抗けいれん薬の必要性を予測する
テオフィリン誘発性発作のリスクが高いテオフィリン過剰摂取患者、例えば、急性過剰摂取で血清テオフィリン濃度が 100 mcg/mL を超える患者、または血清テオフィリン濃度が 30 mcg/mL を超える年齢が 60 歳を超える患者の慢性過剰摂取、抗けいれん療法の必要性を予測する必要があります。ジアゼパムなどのベンゾジアゼピンを注射器に吸い込み、患者のベッドサイドに保管し、発作を治療する資格のある医療関係者をすぐに利用できるようにする必要があります。テオフィリン誘発発作のリスクが高い選択された患者では、予防的抗けいれん療法の投与を考慮する必要があります。ハイリスク患者で予防的抗けいれん療法を考慮すべき状況には、テオフィリンの体外除去のための方法の確立の遅れが予想される場合 (例えば、体外除去のためにハイリスク患者をある医療施設から別の医療施設に移送する場合)、および治療を著しく妨げる臨床状況が含まれます。テオフィリンクリアランスを高めるため(例えば、透析が技術的に実行できない可能性がある新生児、または複数回投与の経口活性炭に耐えられず、制吐薬に反応しない嘔吐患者)。動物実験では、フェニトインではなくフェノバルビタールの予防的投与が、テオフィリン誘発性全身発作の発症を遅らせ、発作を誘発するのに必要なテオフィリンの用量を増加させることが示されています (すなわち、LD50 を著しく増加させます)。ヒトでの対照研究はありませんが、静脈内フェノバルビタールの負荷量 (20 mg/kg を 60 分かけて注入) は、テオフィリン クリアランスを強化するための努力が続けられている間、ハイリスク患者の生命を脅かす発作を遅らせたり予防したりする可能性があります。フェノバルビタールは、特に高齢患者や COPD 患者で呼吸抑制を引き起こす可能性があります。
不整脈の治療
洞性頻脈および単純な心室期外収縮は、生命を脅かす不整脈の前兆ではなく、血行動態が損なわれていなければ治療を必要とせず、血清テオフィリン濃度の低下で解消します。他の不整脈、特に血行動態の障害に関連する不整脈は、不整脈のタイプに適した抗不整脈療法で治療する必要があります。
胃腸の除染
経口活性炭 (0.5 g/kg を 20 g まで、最初の投与から 1 ~ 2 時間後に少なくとも 1 回繰り返す) は、摂取から数時間後に投与した場合でも、胃腸管全体でのテオフィリンの吸収をブロックするのに非常に効果的です。患者が嘔吐している場合は、鼻胃管を介して、または制吐剤の投与後に木炭を投与する必要があります。プロクロルペラジンやペルフェナジンなどのフェノチアジン系制吐薬は、発作閾値を下げ、頻繁にジストニー反応を引き起こす可能性があるため、避ける必要があります。ソルビトールの単回投与は、消化管から炭に結合したテオフィリンの除去を促進する排便を促進するために使用することができます。ただし、ソルビトールは強力な下剤であり、特に複数回の投与後には、深刻な体液と電解質の異常を引き起こす可能性があるため、注意して投与する必要があります.液体チャコールとソルビトールの市販の固定配合剤は、チャコールとソルビトールの投与量を個別に調整できないため、幼い子供、青年および成人の最初の投与後は避ける必要があります。トコンシロップは、テオフィリンの過剰摂取では避けるべきです.トコンは嘔吐を誘発しますが、摂取後 5 分以内に投与しない限りテオフィリンの吸収を低下させず、経口活性炭よりも効果が低くなります。さらに、トコン誘発性嘔吐は、単回投与後数時間持続し、経口活性炭の保持と有効性を著しく低下させる可能性があります.
血清テオフィリン
濃度モニタリング 血清テオフィリン濃度は、受診直後、2~4 時間後に測定し、その後は 4 時間ごとなどの十分な間隔で測定して、治療の決定を導き、治療の有効性を評価する必要があります。血清テオフィリン濃度は、胃腸管からのテオフィリンの継続的な吸収の結果として、患者が診療を受けた後も増加し続ける可能性があります。血清テオフィリン血清濃度の連続モニタリングは、濃度がもはや上昇せず、非毒性レベルに戻ることが明らかになるまで継続する必要があります。
一般的なモニタリング
手順 心電図モニタリングは、受診時に開始し、血清テオフィリン レベルが非毒性レベルに戻るまで継続する必要があります。血清電解質とグルコースは、診察時に、臨床状況によって示される適切な間隔で測定する必要があります。体液および電解質の異常は速やかに是正する必要があります。 血清濃度が 20 mcg/mL を下回るまで、モニタリングと治療を継続する必要があります。
テオフィリンのクリアランスを高める
経口活性炭の複数回投与(例えば、0.5 mg/kg を 20 g まで、2 時間ごと)は、胃腸液に分泌されたテオフィリンの吸着により、テオフィリンのクリアランスを少なくとも 2 倍増加させます。木炭が有効であるためには、消化管に保持され、消化管を通過する必要があります。したがって、適切な制吐剤の投与によって嘔吐を制御する必要があります。あるいは、木炭は、適切な制吐剤と組み合わせて経鼻胃管を通して連続的に投与することができる。吸着されたテオフィリンの胃腸管からのクリアランスを容易にするために、排便を促進するために活性炭と共にソルビトールの単回投与を投与することができる。ソルビトール単独ではテオフィリンのクリアランスを高めることはできず、過度の排便を防ぐために注意して投与する必要があります。液体チャコールとソルビトールの市販の固定配合剤は、チャコールとソルビトールの投与量を個別に調整できないため、幼い子供、青年および成人の最初の投与後は避ける必要があります。難治性嘔吐の患者では、体外からテオフィリンを除去する方法を導入する必要があります(以下を参照)。 過剰摂取 、 体外除去 )。
具体的な推奨事項
急性過剰摂取
慢性的な過剰摂取
体外除去
体外法によるテオフィリンクリアランス率の増加は、血清濃度を急速に低下させる可能性がありますが、この処置のリスクと潜在的な利益を比較検討する必要があります。炭血液灌流は体外除去の最も効果的な方法であり、テオフィリンクリアランスを最大6倍に増加させますが、低血圧、低カルシウム血症、血小板消費、出血素因などの深刻な合併症が発生する可能性があります.血液透析は、複数回投与の経口活性炭とほぼ同じくらい効率的であり、炭血液灌流よりも深刻な合併症のリスクが低くなります。チャコール血液灌流が不可能で、難治性嘔吐のために複数回投与の経口チャコールが効果がない場合、代替手段として血液透析を考慮する必要があります。血清テオフィリン濃度は、組織コンパートメントからのテオフィリンの再分布により、チャコール血液灌流または血液透析の中止後に 5 ~ 10 mcg/mL に回復することがあります。腹膜透析はテオフィリン除去には効果がありません。新生児の交換輸血はほとんど効果がありません。
禁忌
ユニフィル(テオフィリン無水錠) ® は、テオフィリンまたは製品中の他の成分に対する過敏症の病歴のある患者には禁忌です。
臨床薬理学
作用機序
テオフィリンには、可逆性閉塞患者の気道で 2 つの異なる作用があります。平滑筋弛緩(すなわち、気管支拡張)および刺激に対する気道の反応の抑制(すなわち、非気管支拡張予防効果)。テオフィリンの作用メカニズムは確実にはわかっていませんが、動物での研究では、気管支拡張はホスホジエステラーゼの 2 つのアイソザイム (PDE III と、程度は低いものの PDE IV) の阻害によって媒介されることが示唆されています。 PDE III の阻害またはアデノシン受容体の拮抗作用を伴わない、1 つまたは複数の異なる分子メカニズムを介して媒介されます。テオフィリンに関連する副作用のいくつかは、PDE III の阻害 (低血圧、頻脈、頭痛、嘔吐など) およびアデノシン受容体拮抗作用 (脳血流の変化など) によって媒介されるようです。
テオフィリンは、横隔膜筋の収縮力を増加させます。この作用は、アデノシン媒介チャネルを介したカルシウム取り込みの増強によるものと思われます。
血清濃度と効果の関係
気管支拡張は、5 ~ 20 mcg/mL の血清テオフィリン濃度範囲で発生します。臨床的に重要な症状管理の改善には、ほとんどの研究で、血清テオフィリンのピーク濃度が 10 mcg/mL を超えることが必要であることがわかっていますが、軽度の疾患の患者は低濃度で恩恵を受ける可能性があります。血清テオフィリン濃度が 20 mcg/mL を超えると、副作用の頻度と重症度の両方が増加します。一般に、テオフィリンの最高血清濃度を 10 ~ 15 mcg/mL に維持することで、重篤な有害事象のリスクを最小限に抑えながら、薬剤の潜在的な治療効果を最大限に引き出すことができます。
薬物動態
概要
テオフィリンは、溶液または即時放出固体経口剤形での経口投与後、迅速かつ完全に吸収されます。テオフィリンは、かなりの全身前排泄を受けず、無脂肪組織に自由に分布し、肝臓で広範囲に代謝されます.
テオフィリンの薬物動態は、同様の患者間で大きく異なり、年齢、性別、体重、またはその他の人口統計学的特徴によって予測することはできません。さらに、特定の併発疾患および正常な生理機能の変化 (表 I を参照)、および他の薬物の同時投与 (表 II を参照) は、テオフィリンの薬物動態特性を著しく変化させる可能性があります。被験者内の代謝の変動性も、いくつかの研究で、特に急性疾患患者で報告されています。したがって、血清テオフィリン濃度は、急性疾患患者では頻繁に (たとえば 24 時間間隔で) 測定し、長期治療を受けている患者では定期的に (たとえば 6 ~ 12 か月間隔で) 測定することをお勧めします。テオフィリンクリアランスを大幅に変化させる可能性のある状態が存在する場合は、より頻繁に測定を行う必要があります。 注意事項、実験室試験 )。
表 I. 年齢および生理学的状態の変化に関連するテオフィリンの全身クリアランスおよび半減期の平均および範囲¶
ノート: 上記の要因に加えて、低炭水化物/高タンパク食、非経口栄養、および炭火焼き牛肉の毎日の消費によって、テオフィリンクリアランスが増加し、半減期が減少します.高炭水化物/低タンパク質の食事は、クリアランスを減少させ、テオフィリンの半減期を延ばすことができます.
吸収
ユニフィル(テオフィリン無水錠) ® は、摂食状態で投与し、経口投与後は完全に吸収されます。
単回投与のクロスオーバー研究では、2 つの 400 mg Uniphyl (テオフィリン無水錠剤) 錠剤が、同じ標準化された食事 (炭水化物 97 グラム、タンパク質 33 グラム、および 27 グラムからなる 769 カロリー) の直後に、朝または夕方に 19 人の正常なボランティアに投与されました。太い)。用量ダンピングの証拠はなく、薬物投与の時間に起因する薬物動態パラメータの有意差もありませんでした。朝のアームの薬物動態パラメーターは、AUC = 241.9 ± 83.0 mcg hr/mL、Cmax = 9.3 ± 2.0 mcg/mL、Tmax = 12.8 ± 4.2 時間でした。イブニング アームの薬物動態パラメーターは、AUC = 219.7 ± 83.0 mcg hr/mL、Cmax = 9.2 ± 2.0 mcg/mL、Tmax = 12.5 ± 4.2 時間でした。
Uniphyl (テオフィリン無水錠剤) 400 mg 錠剤を 17 人の摂食成人喘息患者に投与した研究では、朝または夕方に投与した場合と同様のテオフィリン レベル-時間曲線が得られました。血清レベルは一般的に夕方のレジメンの方が高かったが、2 つのレジメン間で統計的に有意な差はなかった。
テオフィリン固有の平均消失半減期が液体テオフィリン製品によって 6.9 ± 2.5 (SD) 時間であることが確認された 15 人の通常の絶食男性ボランティアを対象とした単回投与試験では、400 mg Uniphyl (テオフィリン無水錠剤) ® 錠を 2 つか 3 つ投与しました。 .即時放出製品と比較して絶食状態で与えられた Uniphyl (テオフィリン無水錠剤) の相対的バイオアベイラビリティは 59% でした。ピーク血清テオフィリン レベルは 6.9 ± 5.2 (SD) 時間で発生し、正規化された (800 mg までの) ピーク レベルは 6.2 ± 2.1 (SD) でした。 400 mg Uniphyl (テオフィリン無水錠剤) 錠剤の見かけの消失半減期は、17.2 ± 5.8 (SD) 時間でした。
定常状態の薬物動態は、慢性可逆性閉塞性肺疾患の 12 人の絶食患者を対象とした研究で決定されました。すべての被験者に、朝に 1 日 1 回 400 mg Uniphyl (テオフィリン無水錠剤) 錠剤 2 錠を投与し、参照制御放出 BID 製品を 200 mg 錠剤 2 錠として 12 時間間隔で投与しました。 1 日 1 回朝に 800 mg の用量で投与された Uniphyl (テオフィリン無水錠剤) 錠剤について得られた薬物動態パラメータは、400 mg BID として投与された場合の参照薬の対応するパラメータと実質的に同一でした。特に、この研究で得られた AUC、Cmax および Cmin 値は次のとおりです。
投与前の 12 時間と投与後 4 時間は被験者を絶食させた単回投与試験では、食事による投与と比較してバイオアベイラビリティが低下することが示されました。 20 人の正常なボランティアを対象に、朝に 2 つの 400 mg 錠剤を投与した 1 回の単回投与研究では、これらの絶食条件下での投与と、標準化された朝食の直前の投与 (769 カロリー、97 グラムの炭水化物、33 グラムのタンパク質、および27グラムの脂肪)。摂食条件下での薬物動態パラメータは、AUC = 231.7 ± 92.4 mcg hr/mL、Cmax = 8.4 ± 2.6 mcg/mL、Tmax = 17.3 ± 6.7 時間でした。絶食条件下では、これらのパラメーターは AUC = 141.2 ± 6.53 mcg hr/mL、Cmax = 5.5 ± 1.5 mcg/mL、Tmax = 6.5 ± 2.1 時間でした。
21人の正常な男性ボランティアを対象とした別の単回投与研究では、夕方に投与され、空腹時と標準化された高カロリー、高脂肪の食事(870〜1,020カロリー、33グラムのタンパク質、55〜75グラムの脂肪、58グラムの炭水化物からなる)と比較されました.絶食群の被験者は、8時間の断食とそれに続くさらに4時間の絶食の後、午後8時にUniphyl (テオフィリン無水錠剤) ® 400mg錠を1錠服用しました。摂食群では、被験体は 400 mg ユニフィル (テオフィリン無水錠剤) 錠剤 1 個を再び投与されましたが、上記の高脂肪含量の標準化された食事の直後の午後 8 時に投与されました。薬物動態パラメーター (800 mg に標準化) は、AUC = 221.8 ± 40.9 mcg hr/mL、Cmax = 10.9 ± 1.7 mcg/mL、Tmax = 11.8 ± 2.2 時間でした。絶食群では、薬物動態パラメーター (800 mg に正規化) は、AUC = 146.4 ± 40.9 mcg hr/mL、Cmax = 6.7 ± 1.7 mcg/mL、Tmax = 7.3 ± 2.2 時間でした。
したがって、健康で正常なボランティアに Uniphyl (テオフィリン無水錠剤) を 1 回投与すると、長期間絶食状態 (投与前に少なくとも 10 時間は一晩絶食し、投与後はさらに 4 時間絶食) でバイオアベイラビリティが低下します。しかし、高脂肪、高カロリーの食事と一緒に投与された場合でも、Uniphyl (テオフィリン無水錠剤) 錠剤で大量のテオフィリンが突然かつ予期せず放出されるというこの送達システムの失敗はありませんでした.
同様の研究が 600 mg ユニフィル (テオフィリン無水錠剤) 錠剤で実施されました。確立されたテオフィリン クリアランスが 4 L/hr 以下である 24 人の被験者を対象とした単回投与試験では、1 つの 600 mg Uniphyl (テオフィリン無水錠剤) 錠剤と 1.5 の 400 mg Uniphyl (テオフィリン無水錠剤) 錠剤の薬物動態評価が比較されました。給餌(標準的な高脂肪食を使用)および絶食条件下で。この 4 通りの無作為クロスオーバー研究の結果は、400 mg と 600 mg のユニフィル (テオフィリン無水錠剤) 錠剤の生物学的同等性を示しています。摂食条件下で、400 mg 錠剤の 1.5 錠の薬物動態の結果は、AUC = 214.64 ± 55.88 mcg hr/mL、Cmax = 10.58 ± 2.21 mcg/mL、Tmax = 9.00 ± 2.64 時間、600 mg 錠剤ではAUC = 207.85 ± 48.9 mcg hr/mL、Cmax = 10.39 ± 1.91 mcg/mL、Tmax = 9.58 ± 1.86 時間でした。絶食条件下での 1.5 錠 400 mg の薬物動態の結果は、AUC = 191.85 ± 51.1 mcg hr/mL、Cmax = 7.37 ± 1.83 mcg/mL、Tmax = 8.08 ± 4.39 時間でした。 600 mg 錠剤の場合、AUC = 199.39 ± 70.27 mcg hr/mL、Cmax = 7.66 ± 2.09 mcg/mL、Tmax = 9.67 ± 4.89 時間でした。
この研究では、400 mg の 1.5 錠と 600 mg の錠剤の摂食/絶食の平均比率は、それぞれ約 112% と 104% でした。
別の研究では、600 mg Uniphyl (テオフィリン無水錠剤) 錠剤のバイオアベイラビリティが、朝と夜の投与で調べられました。 22 人の健康な男性を対象としたこの単回投与クロスオーバー研究は、給餌 (標準的な高脂肪食) 条件下で実施されました。結果は、朝または夕方に投与された 600 mg Uniphyl (テオフィリン無水錠剤) 錠剤のバイオアベイラビリティーに臨床的に有意な差がないことを示しました。結果は次のとおりです。AUC = 233.6 ± 45.1 mcg hr/mL、Cmax = 10.6 ± 1.3 mcg/mL、および Tmax = 12.5 ± 3.2 時間、朝の投与で。 AUC = 209.8 ± 46.2 mcg hr/mL、Cmax = 9.7 ± 1.4 mcg/mL、および Tmax = 13.7 ± 3.3 時間、夕方の投与。 PM/AM比率は89.3%でした。
ユニフィル®錠(テオフィリン、無水)の吸収特性は、広く研究されています。正常な男性 22 人を対象とした定常状態のクロスオーバー バイオアベイラビリティ研究では、2 つの Uniphyl (テオフィリン無水錠剤) 400 mg 錠剤を朝食直後の午前 8 時に 24 時間ごとに投与し、参照制御放出テオフィリン製品を朝食直後の午前 8 時に摂食被験者に BID 投与し、夕食直後の午後 8 時 (769 カロリー、炭水化物 97 グラム、タンパク質 33 グラム、脂質 27 グラム)。
この定常状態におけるユニフィル(テオフィリン無水錠)400mg錠の薬物動態パラメータは、AUC=203.3±87.1mcg・hr/mL、Cmax=12.1±3.8mcg/mL、Cmin=4.50±3.6、Tmax=8.8±4.6であった。時間。参照 BID 製品の薬物動態パラメータは、AUC = 219.2 ± 88.4 mcg hr/mL、Cmax = 11.0 ± 4.1 mcg/mL、Cmin = 7.28 ± 3.5、Tmax = 6.9 ± 3.4 時間でした。変動率の平均 [(Cmax-Cmin/Cmin)x100] = 1 日 1 回のレジメンで 169%、参照製品の BID レジメンで 51%。
600 mg Uniphyl (テオフィリン無水錠剤) 錠剤のバイオアベイラビリティは、26 人の健康な男性を対象とした複数回投与の定常状態研究でさらに評価され、600 mg 錠剤と 400 mg Uniphyl (テオフィリン無水錠剤) 錠剤の 1.5 倍が比較されました。すべての被験者は、テオフィリン クリアランスが 4 L/hr 以下に設定されており、摂食条件下で 1 日 1 回、6 日間投与されました。結果は、600 mg と 1.5 400 mg Uniphyl (テオフィリン無水錠剤) 錠剤レジメンの間に臨床的に有意な差がないことを示しました。定常状態の結果は次のとおりです。
600/400 mg 錠剤のバイオアベイラビリティ比は 98.8% でした。したがって、すべての試験条件下で、600 mg 錠剤は 400 mg 錠剤の 1.5 倍と生物学的に同等です。
研究によると、被験者が一貫して摂食または一貫して断食している限り、Uniphyl (テオフィリン無水錠剤) 錠剤の 1 日 1 回投与と同様のバイオアベイラビリティーが、朝または夕方に投与されるかどうかにかかわらず存在することが示されています。
分布
テオフィリンが体循環に入ると、約 40% が血漿タンパク質、主にアルブミンに結合します。結合していないテオフィリンは体の水分全体に分布しますが、体脂肪にはあまり分布しません。テオフィリンの見かけの分布体積は、理想体重に基づいて約 0.45 L/kg (範囲 0.3 ~ 0.7 L/kg) です。テオフィリンは、胎盤、母乳、脳脊髄液 (CSF) を自由に通過します。唾液テオフィリン濃度は非結合血清濃度に近似していますが、特別な技術が使用されない限り、ルーチンまたは治療のモニタリングには信頼できません。主に血漿タンパク質結合の減少によるテオフィリンの分布量の増加は、未熟児、肝硬変の患者、未矯正のアシデミア、高齢者、および妊娠第 3 期の女性で発生します。このような場合、患者は、薬理学的に活性な未結合薬物の濃度上昇により、テオフィリンの総 (結合 + 非結合) 血清濃度が治療範囲 (10-20 mcg/mL) で毒性の徴候を示すことがあります。同様に、テオフィリン結合が減少した患者は、薬理学的に活性な非結合濃度が治療範囲内にあるにもかかわらず、治療下の総薬物濃度を有する可能性があります。総血清テオフィリン濃度のみを測定すると、不必要で潜在的に危険な用量の増加につながる可能性があります。タンパク質結合が低下している患者では、結合していない血清テオフィリン濃度の測定は、総血清テオフィリン濃度の測定よりも信頼性の高い投与量調整の手段を提供します。一般に、結合していないテオフィリンの濃度は 6 ~ 12 mcg/mL の範囲に維持する必要があります。
代謝
経口投与後、テオフィリンは測定可能な初回通過排泄を受けません。成人および 1 歳以上の子供では、投与量の約 90% が肝臓で代謝されます。生体内変化は、1-メチルキサンチンと 3-メチルキサンチンへの脱メチル化、および 1,3-ジメチル尿酸へのヒドロキシル化によって行われます。 1-メチルキサンチンは、キサンチンオキシダーゼによってさらにヒドロキシル化され、1-メチル尿酸になります。テオフィリン投与量の約 6% が N-メチル化されてカフェインになります。 3-メチルキサンチンへのテオフィリンの脱メチル化はシトクロム P-450 1A2 によって触媒され、シトクロム P-450 2E1 および P-450 3A3 は 1,3-ジメチル尿酸へのヒドロキシル化を触媒します。 1-メチルキサンチンへの脱メチル化は、シトクロム P-450 1A2 または密接に関連するシトクロムのいずれかによって触媒されるようです。新生児では、N-脱メチル化経路は存在しませんが、ヒドロキシル化経路の機能は著しく不足しています。これらの経路の活動は、1 歳までに最大レベルまでゆっくりと増加します。
カフェインと 3-メチルキサンチンは、薬理活性を持つ唯一のテオフィリン代謝産物です。 3-メチルキサンチンの薬理活性はテオフィリンの約 10 分の 1 であり、腎機能が正常な成人の血清濃度は 1 mcg/mL 未満です。末期腎不全の患者では、3-メチルキサンチンが代謝されていないテオフィリン濃度に近い濃度まで蓄積することがあります。カフェイン濃度は、腎機能に関係なく、成人では通常検出されません。新生児では、代謝されていないテオフィリン濃度に近い濃度までカフェインが蓄積し、薬理学的効果を発揮する可能性があります。
テオフィリン生体内変化の N-脱メチル化経路とヒドロキシル化経路はどちらも容量制限があります。テオフィリンの代謝率は被験者間で大きく変動するため、一部の患者では、血清テオフィリン濃度が 10 mcg/mL 未満で排泄の非線形性が始まる可能性があります。この非直線性は、用量の変化に比例した以上の血清テオフィリン濃度の変化をもたらすため、血清テオフィリン濃度の望ましい変化を達成するために、用量を少しずつ増減することが推奨されます ( 投与量および投与量、表 VI )。患者のテオフィリン代謝の用量依存性をアプリオリに正確に予測することは不可能ですが、初期クリアランス率が非常に高い患者 (つまり、平均用量を超えると定常状態の血清テオフィリン濃度が低い) の患者は、血清で大きな変化を経験する可能性が最も高くなります。投与量の変化に応じたテオフィリン濃度。
排泄
新生児では、テオフィリン投与量の約 50% が未変化のまま尿中に排泄されます。生後 3 か月を過ぎると、テオフィリン投与量の約 10% が変化せずに尿中に排泄されます。残りは、主に 1,3-ジメチル尿酸 (35-40%)、1-メチル尿酸 (20-25%)、3-メチルキサンチン (15-20%) として尿中に排泄されます。テオフィリンはほとんど変化せずに尿中に排泄され、テオフィリンの活性代謝物 (すなわち、カフェイン、3-メチルキサンチン) は末期の腎疾患に直面しても臨床的に有意なレベルまで蓄積しないため、腎不全のための用量調整は必要ありません。大人と生後3ヶ月以上の子供。対照的に、テオフィリン投与量の大部分は未変化のテオフィリンと新生児のカフェインとして尿中に排泄されるため、腎機能が低下した新生児では、投与量の減少と血清テオフィリン濃度の頻繁なモニタリングに注意を払う必要があります。 警告 )。
定常状態での血清濃度
テオフィリンを複数回投与した後、成人では 30 ~ 65 時間 (平均 40 時間) で定常状態に達します。定常状態では、24 時間間隔の投与レジメンで、テオフィリンの平均半減期を 8 時間と仮定すると、予想される平均トラフ濃度は平均ピーク濃度の約 50% です。ピーク濃度とトラフ濃度の差は、テオフィリンクリアランスがより速い患者ほど大きくなります。これらの患者では、Uniphyl (テオフィリン無水錠剤) ® の投与がより頻繁に必要になる場合があります (12 時間ごと)。
特別な集団(平均クリアランスと半減期については表 I を参照)
高齢者
テオフィリンのクリアランスは、健康な若年成人と比較して、健康な高齢者 (> 60 歳) では平均 30% 減少します。高齢患者では、減量と血清テオフィリン濃度の頻繁なモニタリングに注意が必要です( 警告 )。
小児科
新生児におけるテオフィリンのクリアランスは非常に低い( 警告 )。テオフィリンクリアランスは 1 歳までに最大値に達し、約 9 歳までは比較的一定のままで、その後ゆっくりと約 50% 減少し、約 16 歳で成人の値になります。生後 3 か月以上の小児および成人では約 10% です。小児患者では、投与量の選択と血清テオフィリン濃度のモニタリングに注意が必要です( 警告 と 投薬と管理 )。
性別
テオフィリンクリアランスの性差は比較的小さく、臨床的に重要であるとは考えにくい.しかし、テオフィリン クリアランスの大幅な減少は、月経周期の 20 日目と妊娠の第 3 期の女性で報告されています。
人種
人種によるテオフィリンクリアランスの薬物動態の違いは研究されていません。
腎不全
投与されたテオフィリン投与量のわずかな割合、例えば約 10% のみが、生後 3 ヶ月以上の小児および成人の尿中に変化せずに排泄されます。テオフィリンはほとんど変化せずに尿中に排泄され、テオフィリンの活性代謝物 (カフェイン、3-メチルキサンチンなど) は末期の腎疾患に直面しても臨床的に有意なレベルまで蓄積しないため、成人では腎不全のための用量調整は必要ありません。および生後3か月以上の子供。対照的に、投与されたテオフィリン用量の約 50% は、新生児の尿中に変化せずに排泄されます。腎機能が低下した新生児では、減量と血清テオフィリン濃度の頻繁なモニタリングに細心の注意を払う必要があります。 警告 )。
肝不全
肝不全(例,肝硬変,急性肝炎,胆汁うっ滞)の患者では,テオフィリンクリアランスが50%以上低下する。肝機能が低下している患者では、減量に細心の注意を払い、血清テオフィリン濃度を頻繁にモニタリングする必要があります。 警告 )。
うっ血性心不全(CHF)
CHF患者では、テオフィリンクリアランスが50%以上減少する。 CHF患者におけるテオフィリンクリアランスの低下の程度は、心疾患の重症度と直接相関しているようである。テオフィリンクリアランスは肝臓の血流とは無関係であるため、クリアランスの減少は、灌流の減少ではなく、肝細胞機能の障害によるものと思われます。 CHF患者では、減量と血清テオフィリン濃度の頻繁なモニタリングに注意が必要です( 警告 )。
喫煙者
タバコとマリファナの喫煙は、代謝経路の誘導によってテオフィリンのクリアランスを増加させるようです.テオフィリンクリアランスは、非喫煙者と比較して、若年喫煙者では約 50%、高齢喫煙者では約 80% 増加することが示されています。受動喫煙により、テオフィリンのクリアランスが最大 50% 増加することも示されています。 1 週間禁煙すると、テオフィリンクリアランスが約 40% 減少します。禁煙する患者では、減量と血清テオフィリン濃度の頻繁なモニタリングに注意が必要です( 警告 )。ニコチンガムの使用は、テオフィリンクリアランスに影響を与えないことが示されています.
熱
発熱は、その根本的な原因に関係なく、テオフィリンのクリアランスを低下させる可能性があります.発熱の大きさと持続時間は、テオフィリンクリアランスの低下の程度と直接相関しているようです。正確なデータはありませんが、血清テオフィリン濃度を臨床的に有意に上昇させるには、おそらく少なくとも 24 時間 39°C (102°F) の温度が必要です。テオフィリンクリアランスの速度が速い子供(すなわち、無熱時に血清テオフィリン濃度の治療的ピークを達成するために、平均よりも大幅に多い用量を必要とする子供[例:> 22mg/kg/日])は、中毒のリスクがより高い可能性があります。持続的な発熱中のクリアランスの減少による影響。発熱が持続する患者では、減量に注意を払い、血清テオフィリン濃度を頻繁にモニタリングする必要があります。 警告 )。
その他
テオフィリンクリアランスの減少に関連するその他の要因には、妊娠後期、多臓器不全を伴う敗血症、および甲状腺機能低下症が含まれます。これらの状態のいずれかの患者では、減量に注意を払い、血清テオフィリン濃度を頻繁にモニタリングする必要があります。 警告 )。テオフィリンクリアランスの増加に関連するその他の要因には、甲状腺機能亢進症および嚢胞性線維症が含まれます。
臨床研究
吸入コルチコステロイドまたは隔日経口コルチコステロイドを必要とする重度の喘息患者を含む慢性喘息患者では、テオフィリンが夜間増悪を含む症状の頻度と重症度を減らし、「必要に応じた」吸入薬の使用を減らすことが多くの臨床研究で示されています。 β-2 アゴニスト。テオフィリンは、喘息患者の気管支拡張剤に反応しない気道閉塞の悪化を緩和するために、毎日の経口プレドニゾンの短期コースの必要性を減らすことも示されています.
慢性閉塞性肺疾患 (COPD) の患者では、テオフィリンが呼吸困難、エアトラッピング、呼吸仕事量を減少させ、横隔膜筋の収縮性を改善し、肺機能測定値の改善がほとんどまたはまったくないことが臨床研究で示されています。
患者情報
他の原因が疑われる場合でも、テオフィリンによる治療中に吐き気、嘔吐、持続的な頭痛、不眠症、または急速な心拍が発生した場合はいつでも、患者(または親/介護者)に医師の診察を受けるように指示する必要があります.患者は、新しい病気を発症した場合、特に熱が持続する場合、慢性疾患の悪化を経験した場合、タバコやマリファナの喫煙を開始または停止した場合、または別の医療専門家が追加した場合は、医療専門家に連絡するように指示する必要があります。新しい薬を服用するか、以前に処方された薬を中止します。患者は、テオフィリンが多種多様な薬物と相互作用することを知らされるべきです (表 II を参照)。栄養補助食品のセントジョンズワート (Hypericum perforatum) は、テオフィリンのレベルが低下する可能性があるため、テオフィリンと同時に服用しないでください。患者がすでにセントジョーンズワートとテオフィリンを一緒に服用している場合は、セントジョーンズワートを中止する前に医療専門家に相談する必要があります.患者は、治療に関与するすべての医療従事者に、テオフィリンを服用していることを知らせるように指示する必要があります。患者は、最初に医療専門家に相談することなく、投与量、投与のタイミング、または投与頻度を変更しないように指示されるべきです.服用し忘れた場合は、通常予定されている時間に次の服用をするように患者に指示し、忘れた服用を補おうとしないように指示する必要があります。
ユニフィル(テオフィリン無水錠) ® 錠は、1日1回朝晩服用できます。ユニフィル(テオフィリン無水錠剤)は食事と一緒に服用することをお勧めします。 Uniphyl (テオフィリン無水錠剤) を食物と一緒に摂取することを選択した場合、一貫して食物と一緒に摂取する必要があり、絶食状態で摂取する場合は、定期的に絶食して摂取する必要があることを患者にアドバイスする必要があります。製品を服用するときはいつでも、食物の有無にかかわらず一貫して服用することが重要です.
ユニフィル(テオフィリン無水錠剤) テオフィリンが急速に放出され、毒性の可能性があるため、錠剤を噛んだり、つぶしたりしないでください。スコアリングされたタブレットは分割される場合があります。 Uniphyl (テオフィリン無水錠剤) 錠剤を服用している患者は、便中または人工肛門を介して無傷のマトリックス錠剤を通過する可能性があります。これらのマトリックス錠剤には通常、残留テオフィリンがほとんどまたはまったく含まれていません。
