Hydrea 500mg Hydroxyurea 使用法、副作用および投与量。 オンライン薬局の価格。 処方箋不要のジェネリック医薬品。
Hydrea 500mg とは何ですか?
Hydrea (ヒドロキシ尿素) は、メラノーマ、難治性慢性骨髄性白血病、卵巣の再発性、転移性、または手術不能な癌腫および頭頸部の原発性扁平上皮 (類表皮) 癌腫の治療に使用される抗腫瘍 (抗癌) 剤です。 Hydrea は一般的な形で入手できます。
ハイドレアの副作用は?
Hydrea の一般的な副作用は次のとおりです。
- 吐き気、
- 嘔吐、
- 胃のむかつき、
- 下痢、
- 便秘、
- はがれや変色などの皮膚の変化、
- 風邪のような症状、
- 脱毛、
- 発疹、
- 頭痛、
- めまい、
- 眠気、または
- 体重の増加。
Hydrea の深刻な副作用には次のようなものがあります。
- 貧血、
- 骨髄抑制、および
- 白血病。
説明
HYDREA (ヒドロキシ尿素カプセル、USP) は、500 mg のヒドロキシ尿素を含むカプセルとして経口使用できる代謝拮抗剤です。不活性成分には、クエン酸、着色料 (D&C 黄色 10 号、FD&C 青色 1 号、FD&C 赤色 40 号、および D&C 赤色 28 号)、ゼラチン、乳糖、ステアリン酸マグネシウム、リン酸ナトリウム、および二酸化チタンが含まれます。
ヒドロキシ尿素は白色からオフホワイトの結晶性粉末です。吸湿性があり水に溶けやすいが、アルコールにはほとんど溶けない。実験式は CH4N2O2 で、分子量は 76.05 です。その構造式は次のとおりです。
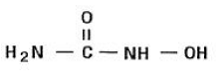
適応症
HYDREA 500mg は、以下の治療に適応されます。
- 抵抗性慢性骨髄性白血病。
- 頭頸部(口唇を除く)の局所進行扁平上皮がんと化学放射線療法の併用。
投薬と管理
投与情報
HYDREA は、腫瘍性疾患を治療するために、単独で、または他の抗腫瘍剤または放射線療法と組み合わせて使用されます。腫瘍の種類、病状、治療への反応、患者の危険因子、および現在の臨床診療基準に基づいて治療を個別化します。
すべての投与量は、患者の実際の体重または理想体重のいずれか少ない方に基づいてください。
HYDREA は細胞毒性薬です。該当する特別な取り扱いおよび廃棄手順に従ってください [参照 参考文献 ]。
HYDREA カプセルを丸ごと飲み込んでください。 HYDREA は細胞毒性薬であるため、カプセルを開けたり、壊したり、噛んだりしないでください。
葉酸の予防投与が推奨される[参照 警告と注意事項 ]。
HYDREA 500mg 治療中は、少なくとも週に 1 回は血球数をモニターしてください。 HYDREA による治療を開始する前に、重度の貧血を是正する必要があります。
毒性に対する用量変更
以下を監視し、それに応じて用量を減らすか、HYDREA 500mg を中止してください。
- 骨髄抑制 [参照 警告と注意事項 ]
- 皮膚血管炎 [参照 警告と注意事項 ]
他の毒性については用量変更を検討してください。
腎障害に対する用量変更
測定されたクレアチニンクリアランスが 60 mL/min 未満の患者、または末期腎疾患 (ESRD) の患者では、HYDREA の用量を 50% 減らします [参照 特定の集団での使用 と 臨床薬理学 ]。
これらの患者では、血液学的パラメーターの綿密なモニタリングが推奨されます。
供給方法
剤形と強度
カプセル
500mgの不透明な緑色のキャップと不透明なピンクのボディに「HYDREA」と「830」が刻印されています。
保管と取り扱い
HYDREA® (ヒドロキシ尿素カプセル、USP) 500 mg のカプセルで、プラスチック製の安全スクリュー キャップ付きの HDPE ボトルに入っています。各ボトルには100カプセルが含まれています。
キャップはオペークグリーン、ボディはオペークピンクです。カプセルは両方のセクションに「HYDREA」と「830」が黒インクで刻印されています ( NDC 0003-0830-50)。
保管所
20~25°C (68~77°F) で保管してください。 15°C ~ 30°C (59°F ~ 86°F) [USP Controlled RoomTemperature を参照] まで許容されます。密閉して保管してください。
取り扱いと廃棄
HYDREA 500mg は細胞毒性薬です。該当する特別な取り扱いおよび廃棄手順に従ってください [参照 参考文献 ]。
接触のリスクを減らすために、HYDREA または HYDREA を含むボトルを取り扱う際は、介護者に使い捨て手袋を着用するようにアドバイスしてください。 HYDREA を取り扱う際は、ボトルやカプセルに触れる前後に石けんと水で手を洗ってください。 HYDREA 500mg カプセルを開封しないでください。つぶれたカプセルや開いたカプセルに触れないようにしてください。つぶれたカプセルや開いたカプセルが皮膚に付着した場合は、直ちに患部を石鹸と水で十分に洗い流してください。つぶれたカプセルや開いたカプセルが目に入った場合は、患部を水または専用の等張性洗眼液で少なくとも 15 分間完全に洗い流す必要があります。カプセルから粉末がこぼれた場合は、すぐに湿らせた使い捨てタオルで拭き取り、ビニール袋などの密閉容器に捨ててください。空のカプセルと同様に。こぼれた場所は、洗剤溶液ときれいな水を使用して 3 回洗浄する必要があります。子供やペットから薬を遠ざけてください。古くなったカプセルの廃棄方法については、医師にご相談ください。
参考文献
OSHA。 http://www.osha.gov/SLTC/hazardousdrugs/index.html。
製造元: Bristol-Myers Squibb Company、プリンストン、ニュージャージー州 08543 米国。改訂: 2020 年 12 月
副作用
以下の臨床的に重大な副作用は、他のラベルのセクションで詳細に説明されています。
- 骨髄抑制 [参照 警告と注意事項 ]
- 悪性腫瘍 [参照 警告と注意事項 ]
- 血管毒性 [参照 警告と注意事項 ]
- 抗レトロウイルス薬の併用に伴うリスク[参照 警告と注意事項 ]
- 放射線リコール [参照 警告と注意事項 ]
- 大赤血球症 [参照 警告と注意事項 ]
- 肺毒性 [参照 警告と注意事項 ]
市販後の経験
HYDREAの承認後の使用中に、次の副作用が確認されました。これらの反応は、不確実な規模の集団から自発的に報告されるため、その頻度を確実に推定することは常に可能ではありません.
- 生殖器系および乳房障害: 無精子症、および乏精子症
- 胃腸障害: 口内炎、吐き気、嘔吐、下痢、便秘
- 代謝・栄養障害: 食欲不振、腫瘍崩壊症候群
- 皮膚および皮下組織の障害: 黄斑丘疹の発疹、皮膚潰瘍、皮膚紅斑性狼瘡、皮膚筋炎様の皮膚の変化、末梢および顔面の紅斑、色素沈着過剰、爪の色素沈着過剰、皮膚および爪の萎縮、落屑、紫色の丘疹、および脱毛症
- 腎および泌尿器疾患: 排尿障害、血清尿酸、血中尿素窒素(BUN)、およびクレアチニン値の上昇
- 神経系障害: 頭痛、めまい、眠気、見当識障害、幻覚、痙攣
- 一般的な障害: 発熱、悪寒、倦怠感、浮腫、無力症
- 肝胆道障害: 肝酵素の上昇、胆汁うっ滞、および肝炎
- 呼吸器疾患: びまん性肺浸潤、呼吸困難、および肺線維症、間質性肺疾患、肺炎、肺胞炎、アレルギー性肺胞炎および咳
- 免疫障害: 全身性エリテマトーデス
- 過敏症: 入院を必要とする薬物誘発性の発熱 (>39°C、>102°F) が、胃腸、肺、筋骨格、肝胆、皮膚、または心臓血管の症状と同時に報告されています。発症は通常、開始から 6 週間以内に発生し、ヒドロキシ尿素の中止により回復しました。再投与すると、典型的には 24 時間以内に発熱が再発した。
ヒドロキシ尿素と放射線治療の併用で観察される有害反応は、ヒドロキシ尿素または放射線治療単独で報告されたものと同様です。これらの影響には、主に骨髄抑制(貧血および白血球減少症)、胃の刺激、および粘膜炎が含まれます。ヒドロキシ尿素と放射線療法を組み合わせた適切なコースを受けているほとんどすべての患者は、同時に白血球減少症を示します。顕著な白血球減少症の存在下で、血小板減少 (
薬物相互作用
抗レトロウイルス薬の併用による毒性の増加
膵炎
スタブジンの有無にかかわらず、ヒドロキシ尿素とジダノシンによる治療中にHIV感染した患者では、致命的および非致命的な膵炎が発生しました。ヒドロキシ尿素は HIV 感染症の治療には適応されません。ただし、HIV感染患者がヒドロキシ尿素で治療されている場合、特にジダノシンおよび/またはスタブジンと組み合わせて、膵炎の徴候と症状を注意深く監視することをお勧めします.膵炎の徴候や症状が現れた患者では、ヒドロキシ尿素による治療を完全に中止してください。
肝毒性
ヒドロキシウレアおよび他の抗レトロウイルス薬で治療されたHIV感染患者の市販後調査中に、死に至る肝毒性および肝不全が報告されています。致命的な肝イベントは、ヒドロキシ尿素、ジダノシン、およびスタブジンの組み合わせで治療された患者で最も頻繁に報告されました.この組み合わせは避けてください。
末梢神経障害
スタブジンの有無にかかわらず、ジダノシンを含む抗レトロウイルス薬と組み合わせてヒドロキシ尿素を投与されたHIV感染患者で、場合によっては重篤な末梢神経障害が報告されています。
実験室試験干渉
尿酸、尿素、または乳酸アッセイへの干渉
研究では、尿素、尿酸、および乳酸の測定に使用される酵素 (ウレアーゼ、ウリカーゼ、および乳酸デヒドロゲナーゼ) に対するヒドロキシ尿素の分析的干渉があり、ヒドロキシ尿素で治療された患者でこれらの結果が誤って上昇することが示されています。
警告
の一部として含まれています "予防" セクション
予防
骨髄抑制
ヒドロキシ尿素は重度の骨髄抑制を引き起こします。骨髄機能が著しく低下している場合は、ヒドロキシ尿素による治療を開始しないでください。骨髄抑制が起こる可能性があり、白血球減少症は一般に最初の最も一般的な症状です。血小板減少症および貧血はあまり発生せず、先行する白血球減少症なしではめったに見られません。骨髄抑制は、以前に放射線療法または細胞傷害性癌化学療法剤を受けた患者で発生する可能性が高くなります。そのような患者には慎重にヒドロキシ尿素を使用してください。
HYDREA による治療前および治療中に血液学的状態を評価します。支持療法を提供し、必要に応じて用量を変更するか、HYDREA を中止してください。治療を中断すると、骨髄抑制からの回復は通常急速です。
悪性腫瘍
ヒドロキシ尿素はヒト発がん物質です。骨髄増殖性疾患のために長期ヒドロキシ尿素を投与されている患者では、続発性白血病が報告されています。ヒドロキシ尿素を長期投与している患者では、皮膚がんも報告されています。日光にさらされないように注意し、二次的な悪性腫瘍の発生を監視してください。
胚・胎児毒性
作用機序と動物での調査結果に基づいて、HYDREA 500mg は妊婦に投与すると胎児に害を及ぼす可能性があります。ヒドロキシ尿素は、mg/m2 に基づく最大推奨ヒト 1 日用量のそれぞれ 0.8 倍および 0.3 倍の用量で、ラットおよびウサギにおいて胎児毒性および催奇形性を示した。妊娠中の女性には、胎児への潜在的なリスクについて助言する [参照 特定の集団での使用 ]。
生殖能力のある女性には、HYDREA 500mg による治療中および治療後少なくとも 6 か月間は効果的な避妊法を使用するようにアドバイスしてください。治療後少なくとも 1 年間は HYDREA 500mg による治療中および治療後に効果的な避妊法を使用するよう、生殖能力のある男性に助言する [ 特定の集団での使用 ]。
血管毒性
血管炎性潰瘍および壊疽を含む皮膚血管毒性は、ヒドロキシ尿素による治療中に骨髄増殖性疾患の患者に発生しています。これらの血管毒性は、インターフェロン療法の既往または現在受けている患者で最も頻繁に報告されました。皮膚血管炎性潰瘍が発生した場合は、治療を開始し、HYDREA を中止してください。
生ワクチン接種
HYDREA を服用している患者では、生ワクチンの使用を避けてください。 HYDREA と生ウイルス ワクチンを併用すると、ウイルスの複製が促進されたり、HYDREA によって通常の防御機構が抑制される可能性があるため、ワクチンの有害反応が増加する可能性があります。 HYDREA 500mg を投与されている患者に生ワクチンを接種すると、重度の感染症を引き起こす可能性があります。ワクチンに対する患者の抗体反応が低下する可能性があります。専門家への相談を検討してください。
抗レトロウイルス薬の併用によるリスク
ジダノシンやスタブジンなどの抗レトロウイルス薬と併用してヒドロキシ尿素を投与すると、膵炎、肝毒性、および末梢神経障害が発生した[参照 薬物相互作用 ]。
放射線リコール
過去に放射線治療を受けた患者さんは、照射後の紅斑が悪化することがあります。以前に放射線を受けた患者の皮膚の紅斑を監視し、症状に応じて管理します。
大赤血球症
HYDREA 500mg は、自己制限的な大赤血球症を引き起こす可能性があり、治療過程の初期によく見られます。形態学的変化は悪性貧血に似ていますが、ビタミン B12 や葉酸欠乏症とは関係ありません。これは、悪性貧血の診断を覆い隠す可能性があります。葉酸の予防投与が推奨されます。
肺毒性
骨髄増殖性腫瘍の治療を受けた患者では、肺線維症、肺浸潤、肺炎、肺胞炎/アレルギー性肺胞炎 (致死例を含む) などの間質性肺疾患が報告されています。発熱、咳、呼吸困難、またはその他の呼吸器症状を発症している患者を頻繁に監視し、調査して迅速に治療します。 HYDREA 500mg を中止し、コルチコステロイドで管理する [参照 有害反応 ]。
実験室試験干渉
尿酸、尿素、または乳酸アッセイへの干渉が可能であり、ヒドロキシ尿素で治療された患者でこれらの結果が誤って上昇する[参照 薬物相互作用 ]。
非臨床毒性学
発がん、突然変異誘発、生殖能力の障害
ヒドロキシ尿素の発がん性を評価するための従来の長期試験は実施されていません。しかし、125 ~ 250 mg/kg のヒドロキシ尿素 (mg/m2 に基づいてヒトの最大推奨経口 1 日用量の約 0.6 ~ 1.2 倍) を週 3 回、6 か月間雌ラットに腹腔内投与すると、生存ラットの乳腺腫瘍の発生率が 18 に増加しました。コントロールと比較して月。ヒドロキシ尿素は、in vitro で細菌、真菌、原生動物、および哺乳類細胞に対して変異原性を示します。ヒドロキシ尿素は、in vitro (ハムスター細胞、ヒトリンパ芽球) および in vivo (げっ歯類の SCE アッセイ、マウス小核アッセイ) で染色体異常誘発性があります。ヒドロキシ尿素は、げっ歯類の胚細胞を腫瘍形成性の表現型に変換します。
ヒドロキシウレアを雄ラットに 60 mg/kg/日 (mg/m2 に基づいてヒトの 1 日最大推奨用量の約 0.3 倍) 投与すると、精巣の萎縮、精子形成の減少、雌の妊娠能力の大幅な低下が生じた。
特定の集団での使用
妊娠
リスクの概要
HYDREA は、動物実験から得られた知見と薬剤の作用機序に基づいて、胎児に害を及ぼす可能性があります [参照 臨床薬理学 ]。薬物関連のリスクを知らせるために、妊娠中の女性に HYDREA を使用したデータはありません。動物の繁殖研究では、器官形成期の妊娠中のラットとウサギにヒドロキシ尿素を投与すると、mg/m2 に基づく最大推奨ヒト 1 日用量のそれぞれ 0.8 倍と 0.3 倍の用量で胚毒性と催奇形性効果が生じた ( データ )。胎児への潜在的なリスクについて女性に助言し、HYDREA による治療中は妊娠を避けるようにしてください。
米国の一般集団では、臨床的に認識された妊娠における主要な先天異常および流産の推定背景リスクは、それぞれ 2% ~ 4% および 15% ~ 20% です。
データ
動物データ
ヒドロキシウレアは、マウス、ハムスター、ネコ、ミニブタ、イヌ、サルなどのさまざまな動物モデルにおいて、mg/m2 ベースで与えられるヒト用量の 1 倍以内の用量で、強力な催奇形物質であることが実証されています。ヒドロキシウレアは胚毒性があり、180 mg/kg/日 (mg/m2 に基づく最大推奨ヒト 1 日用量の約 0.8 倍) で胎児の奇形 (部分的に骨化した頭蓋骨、眼窩の欠如、水頭症、二部胸骨、腰椎の欠損) を引き起こします。ラットでは 30 mg/kg/日 (mg/m2 に基づく最大推奨ヒト 1 日用量の約 0.3 倍) でウサギに。胚毒性は、胎児生存率の低下、同腹子数の減少、および発育遅延を特徴としていました。ヒドロキシウレアは胎盤を通過します。 375 mg/kg 以上の単回投与 (mg/m2 に基づいてヒトの 1 日最大推奨量の約 1.7 倍) をラットに投与すると、成長遅延と学習能力の障害が引き起こされました。
授乳
リスクの概要
ヒドロキシ尿素は母乳中に排泄されます。発がん性を含む、ヒドロキシウレアによる母乳育児中の幼児への重篤な有害反応の可能性があるため、HYDREA による治療中は母乳育児を中止してください。
生殖能力のある雌と雄
妊娠検査
HYDREA 治療を開始する前に、生殖能力のある女性の妊娠状態を確認してください。
避妊
女性
HYDREA を妊婦に投与すると、胎児に害を及ぼす可能性があります [参照 妊娠 ]。生殖能力のある女性には、HYDREA による治療中および治療後少なくとも 6 か月間は効果的な避妊法を使用するようにアドバイスしてください。女性には、妊娠をすぐに報告するようにアドバイスしてください。
男性
HYDREA 500mg は、精子および精巣組織に損傷を与え、遺伝子異常を引き起こす可能性があります。生殖能力のある女性の性的パートナーを持つ男性は、HYDREA 500mg による治療中および治療後、治療後少なくとも 1 年間は効果的な避妊法を使用する必要があります。 非臨床毒性学 ]。
不妊
男性
動物およびヒトでの調査結果に基づくと、男性の生殖能力は HYDREA による治療によって損なわれる可能性があります。無精子症または乏精子症は、時には可逆的であり、男性で観察されています.治療開始前に精子保存の可能性について患者に説明する[参照 有害反応 と 非臨床毒性学 ]。
小児用
小児患者における安全性と有効性は確立されていません。
高齢者の使用
高齢の患者は、ヒドロキシ尿素の影響に対してより敏感である可能性があり、より低い用量レジメンが必要になる場合があります.ヒドロキシウレアは腎臓から排泄されるため、腎機能が低下している患者では、この薬に対する副作用のリスクが高くなる可能性があります。高齢患者は腎機能が低下している可能性が高いため、用量の選択には注意が必要であり、腎機能のモニタリングが有用な場合があります [参照 投薬と管理 ]。
腎障害
ヒドロキシ尿素への曝露は、クレアチニンクリアランスが 60 mL/min 未満の患者、または末期腎疾患 (ESRD) の患者で高くなります。これらの患者に HYDREA 500mg を投与する場合は、投与量を減らし、血液学的パラメータを注意深く監視してください [ 投薬と管理 と 臨床薬理学 ]。
肝障害
肝機能障害のある患者の用量調整に関する具体的なガイダンスを裏付けるデータはありません。これらの患者では、血液学的パラメーターの綿密なモニタリングが推奨されます。
過剰摂取
ヒドロキシ尿素を治療用量の数倍の用量で投与されている患者では、急性の皮膚粘膜毒性が報告されています。痛み、紫色の紅斑、手のひらと足の裏の浮腫、それに続く手足の鱗屑、皮膚の重度の全身性色素沈着、口内炎も観察されています。
禁忌
HYDREA 500mg は、ヒドロキシ尿素または製剤の他の成分に対して以前に過敏症を示したことのある患者には禁忌です。
臨床薬理学
作用機序
ヒドロキシ尿素がその抗腫瘍効果を生み出す正確なメカニズムは、現時点では説明できません。しかし、ラットとヒトの組織培養におけるさまざまな研究の報告は、ヒドロキシ尿素がリボ核酸またはタンパク質の合成を妨げることなく、リボヌクレオチドレダクターゼ阻害剤として作用することにより、DNA 合成の即時阻害を引き起こすという仮説を支持しています。この仮説は、特定の条件下でヒドロキシ尿素が催奇形性効果を誘発する理由を説明しています。
頭頸部の扁平上皮(類表皮)癌に対するヒドロキシウレア療法と放射線照射の併用による有効性の増加について、3 つの作用機序が仮定されています。チャイニーズハムスター細胞を利用した in vitro 研究では、ヒドロキシ尿素は (1) 通常は放射線抵抗性の S 期細胞に対して致死的であり、(2) 細胞周期の他の細胞を G1 または DNA 合成前の段階で保持し、そこで最も影響を受けやすいことを示唆しています。照射の効果。 3 番目の作用機序は、HeLa 細胞の in vitro 研究に基づいて理論化されています。ヒドロキシウレアは、DNA 合成を阻害することにより、照射によって損傷されたが殺されなかった細胞の正常な修復プロセスを妨げ、それによって細胞の生存率を低下させるようです。 RNA とタンパク質の合成は変化を示していません。
薬物動態
吸収
HYDREA の経口投与後、ヒドロキシ尿素は 1 ~ 4 時間で最高血漿濃度に達します。平均ピーク血漿濃度と AUC は、用量の増加に比例して増加します。
ヒドロキシ尿素の吸収に対する食物の影響に関するデータはありません。
分布
ヒドロキシウレアは、全身の水分量に近い量で全身に分布します。
ヒドロキシ尿素は白血球と赤血球に濃縮されます。
代謝
経口投与量の最大 60% は、飽和肝代謝と、腸内細菌に見られるウレアーゼによるマイナーな分解経路を介して変換されます。
排泄
鎌状赤血球貧血の患者では、ヒドロキシ尿素の平均累積尿回収率は投与量の約 40% でした。
特定の集団
腎障害
鎌状赤血球症および腎障害を有する成人患者において、ヒドロキシ尿素の薬物動態に対する腎障害の影響を評価した。正常な腎機能 (クレアチニン クリアランス [CrCl] >80 mL/min)、軽度 (CrCl 50-80 mL/min)、中等度 (CrCl = 30- 60 mL/min) よりも 64% 高かった。クレアチニンクリアランスが 60 mL/min 未満の患者、または血液透析後の ESRD の患者に投与する場合は、HYDREA 500mg の用量を減らしてください [ 投薬と管理 と 特定の集団での使用 ]。
患者情報
- 骨髄抑制のリスクがあります。 HYDREA を服用している患者には、治療期間中毎週血球数をモニタリングすることを強調する必要があります。 警告と注意事項 ]。感染や出血の徴候や症状を直ちに報告するよう患者に助言する。
- 皮膚血管毒性および白血病や皮膚がんなどの二次性悪性腫瘍のリスクがあることを患者に助言する[参照 警告と注意事項 ]。
- 妊娠の可能性がある女性には、胎児への潜在的なリスクについて助言し、妊娠が判明している、または妊娠の疑いがあることを医療従事者に知らせるようにしてください。 HYDREA による治療中および治療後に避妊を行うよう、生殖能力のある女性と男性に助言する [参照 警告と注意事項 と 特定の集団での使用 ]。
- HYDREA 500mg の服用中にワクチン接種を受けたことがある場合、または受ける予定がある場合は、重度の感染症を引き起こす可能性があるため、医療提供者に知らせるように患者に助言してください。 警告と注意事項 ]。
- HYDREA による治療中は授乳を中止するよう女性に助言する [参照 特定の集団での使用 ]。
- HIV 感染患者は、膵炎、肝イベント、および末梢神経障害の徴候と症状について医師に連絡する必要があります。 警告と注意事項 ]。
- 照射後の紅斑は、以前に放射線療法を受けた患者に発生する可能性があります[を参照してください。 警告と注意事項 ]。
- 潜在的な肺毒性の症状について患者に助言し、発熱、咳、呼吸困難、またはその他の呼吸器症状が発生した場合は、速やかに医師の診察を受けるように指示する[参照 警告と注意事項 ]。
