Furadantin 100mg Nitrofurantoin 使用法、副作用および投与量。 オンライン薬局の価格。 処方箋不要のジェネリック医薬品。
フラダンチン100mgとは?
フラダンチン(ニトロフラントイン経口懸濁液)は、尿路感染症の治療に使用される抗生物質です。フラダンチンは一般的な形で入手できます。
フラダンチンの副作用は何ですか?
フラダンチンの一般的な副作用は次のとおりです。
- 吐き気、
- 嘔吐、
- 食欲減少、
- 胃のむかつき、
- 下痢、
- 頭痛、
- めまい、
- 眠気、
- さび色または茶色がかった尿、または
- 膣のかゆみまたは分泌物。
以下を含むフラダンチンのまれではあるが非常に深刻な副作用がある場合は、医師に相談してください。
- 眼の痛み、
- 視界の変化、
- 精神/気分の変化、
- 持続性または重度の頭痛、
- 感染の新たな徴候(例、発熱、持続性の喉の痛み)、または
- あざや出血が起こりやすい。
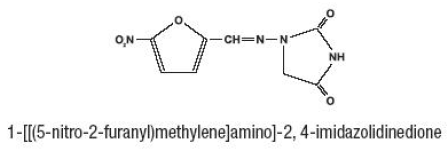
説明
合成化学物質であるフラダンチン(ニトロフラントイン)は、安定した黄色の結晶性化合物です。フラダンチンは、特定の尿路感染症に対する抗菌剤です。フラダンチンは、経口投与用に 25mg/5mL 液体懸濁液で入手できます。
不活性成分
フラダンチン経口懸濁液には、カルボキシメチルセルロースナトリウム、クエン酸、香料、グリセリン、ケイ酸アルミニウムマグネシウム、メチルパラベン、プロピルパラベン、精製水、クエン酸ナトリウム、およびソルビトールが含まれています。
適応症
フラダンチン Escherichia coli、enterococci、Staphylococcus aureus の感受性株、および Klebsiella および Enterobacter 種の特定の感受性株による尿路感染症の治療に特に適応されます。
ニトロフラントインは、腎盂腎炎または腎周囲膿瘍の治療には適応されません。
ニトロフラントインは、尿路感染症に対して承認されている他の治療薬のように組織に広く分布していません。そのため、治療を受ける患者さんの多くは フラダンチン 細菌尿が持続または再発する傾向があります。培養および感受性試験のための尿検体は、治療終了の前後に採取する必要があります。治療後に細菌尿が持続または再発した場合 フラダンチン 、より広い組織分布を持つ他の治療薬を選択する必要があります。の利用を考えると フラダンチン より低い根絶率は、全身毒性の可能性の増加と、より広い組織分布を持つ薬剤が利用される場合の抗菌薬耐性の発生とのバランスを取る必要があります。
投薬と管理
フラダンチン 薬物の吸収を改善し、一部の患者では耐性を改善するために、食物と一緒に投与する必要があります。
大人
50-100 mg を 1 日 4 回 - 合併症のない尿路感染症には、より低い用量レベルが推奨されます。
小児患者
24 時間あたり 5 ~ 7 mg/kg 体重を 4 回に分けて投与します (生後 1 か月未満は禁忌)。
次の表は、24 時間あたり 5 ~ 6 mg/kg 体重を 4 回に分けて投与した各範囲の平均体重に基づいています。の平均線量を計算するために使用できます。 フラダンチン 小児患者用の経口懸濁液 (25 mg/5 mL)。
治療は、尿の無菌性が得られた後、1 週間または少なくとも 3 日間継続する必要があります。継続的な感染は、再評価の必要性を示しています。
成人における長期の抑制療法では、就寝時に 50 ~ 100 mg に減量するのが適切な場合があります。小児患者の長期抑制療法では、1 回または 2 回に分けて 24 時間あたり 1 mg/kg という低用量で十分な場合があります。見る 長期治療に伴うリスクに関する警告セクション .
供給方法
フラダンチン 経口懸濁液は、次の製品で利用できます。
NDC 70199-006-32 230mL PET琥珀瓶
薬が黒ずむ可能性がある強い光にさらさないでください。 20°~25°C (68°~77°F) で保管すると安定します。 15°-30°C (59°-86°F) まで許容されるエクスカーション [参照 USP制御の室温 ]。凍結から保護してください。激しく揺する。密封された耐光性のあるプラスチック (PET) またはガラス容器に分注してください。
30日以内にご利用ください。
小児の手の届かない場所に保管。
製造元: Casper Pharma LLC, East Brunswick NJ 08816. 改訂: 2020 年 12 月
副作用
呼吸器
慢性、亜急性、または急性の肺過敏症反応が起こることがあります。
慢性肺反応は、通常、6 か月以上の継続的な治療を受けた患者に発生する可能性があります。倦怠感、運動時の呼吸困難、咳、および肺機能の変化は、知らず知らずに発生する可能性がある一般的な症状です。びまん性間質性肺炎または線維症、またはその両方の放射線学的および組織学的所見も、慢性肺反応の一般的な症状です。発熱が目立つことはめったにありません。
慢性肺反応の重症度とその回復度は、最初の臨床症状が現れた後の治療期間に関連しているようです。治療を中止した後でも、肺機能が永久に損なわれる可能性があります。慢性肺反応が早期に認識されない場合、リスクは大きくなります。
亜急性肺反応では、発熱と好酸球増加症は急性型よりも発生頻度が低くなります。治療を中止すると、回復には数か月かかる場合があります。症状が薬物関連であると認識されず、ニトロフラントイン療法が中止されない場合、症状がより深刻になる可能性があります.
急性肺反応は、一般に、発熱、悪寒、咳、胸痛、呼吸困難、X 線での胸水の硬化を伴う肺浸潤、および好酸球増多によって現れます。
急性反応は通常、治療の最初の 1 週間以内に発生し、治療を中止すると元に戻ります。多くの場合、解像度は劇的です。 (見る 警告 )
EKG の変化 (例えば、非特異的な ST/T 波の変化、脚ブロック) は、肺反応に関連して報告されています。
まれにチアノーゼが報告されています。
肝臓
肝炎、胆汁うっ滞性黄疸、慢性活動性肝炎、肝神経症などの肝反応はめったに起こりません。 (見る 警告 )
神経学的
重度または不可逆になる可能性のある末梢神経障害が発生しています。死亡者が報告されています。腎障害(クレアチニンクリアランスが毎分 60 mL 未満または臨床的に有意な血清クレアチニンの上昇)、貧血、真性糖尿病、電解質の不均衡、ビタミン B 欠乏症、衰弱性疾患などの状態は、末梢神経障害の可能性を高める可能性があります( 警告 )
ニトロフラントインの使用により、無力症、めまい、眼振、めまい、頭痛、および眠気も報告されています。
良性頭蓋内圧亢進症(偽大脳腫瘍)、錯乱、抑うつ、視神経炎、および精神病反応がまれに報告されています。乳児の良性頭蓋内圧亢進症の徴候としての泉門の隆起は、めったに報告されていません。
皮膚科
剥脱性皮膚炎および多形紅斑(スティーブンス・ジョンソン症候群を含む)はまれに報告されています。一過性脱毛症も報告されています。
アレルギー
ニトロフラントインに対する肺反応に関連する狼瘡様症候群が報告されています。また、血管性浮腫;黄斑丘疹、紅斑性、または湿疹性発疹;かゆみ;蕁麻疹;アナフィラキシー;関節痛;筋肉痛;薬物熱;および血管炎(肺反応を伴うこともある)が報告されています。過敏症反応は、ニトロフラントイン製剤の世界的な市販後経験において、自発的に報告される最も頻繁な有害事象を示します。
胃腸
吐き気、嘔吐、食欲不振が最も頻繁に発生します。腹痛と下痢は、あまり一般的でない胃腸反応です。これらの用量関連反応は、用量を減らすことで最小限に抑えることができます。唾液腺炎および膵炎が報告されています。ニトロフラントインの使用による偽膜性大腸炎の散発的な報告があります。偽膜性大腸炎の症状の発症は、抗菌薬治療中または治療後に発生する可能性があります。 (見る 警告 )
血液学
メトヘモグロビン血症に続発するチアノーゼはめったに報告されていません。
その他
他の抗菌剤と同様に、耐性生物、例えばシュードモナス種またはカンジダ種によって引き起こされる重複感染が発生する可能性があります。ニトロフラントインの使用による、クロストリジウム・ディフィシル重複感染、または偽膜性大腸炎の散発的な報告があります。
実験室の有害事象
ニトロフラントインの使用により、以下の実験室での有害事象が報告されています。 AST(SGOT)の増加、ALT(SGPT)の増加、ヘモグロビンの減少、血清リンの増加、好酸球増加症、グルコース-6-リン酸脱水素酵素欠乏性貧血( 警告 )、無顆粒球症、白血球減少症、顆粒球減少症、溶血性貧血、血小板減少症、巨赤芽球性貧血。ほとんどの場合、これらの血液学的異常は、治療の中止後に解消されました。再生不良性貧血はまれに報告されています。
疑わしい有害反応を報告するには、Casper Pharma LLC に連絡してください。 1-844-5-CASPER (1-844-522-7737) または FDA では 1-800-FDA-1088 または www.fda.gov/medwatch。
薬物相互作用
三ケイ酸マグネシウムを含む制酸剤は、ニトロフラントインと同時に投与すると、吸収の速度と程度の両方を低下させます。この相互作用のメカニズムは、おそらく三ケイ酸マグネシウムの表面へのニトロフラントインの吸着です。
プロベネシドやスルフィンピラゾンなどの尿酸減少薬は、ニトロフラントインの尿細管分泌を阻害する可能性があります。結果として生じるニトロフラントインの血清レベルの上昇は毒性を高める可能性があり、尿中レベルの低下は尿路抗菌剤としての有効性を低下させる可能性があります.
薬物/実験室試験の相互作用
ニトロフラントインの存在の結果として、尿中のグルコースに対する偽陽性反応が起こることがあります。これは、ベネディクトとフェーリングの溶液で観察されましたが、グルコース酵素テストでは観察されませんでした.
警告
肺反応
急性、亜急性、または慢性の肺反応が、ニトロフラントインで治療された患者で観察されています。これらの反応が生じた場合は、フラダンチン 100mg の使用を中止し、適切な処置を行うこと。報告では、死亡の一因として肺反応が挙げられています。
慢性肺反応 (びまん性間質性肺炎または肺線維症、またはその両方) は、潜行的に発症する可能性があります。これらの反応は、6 か月以上治療を受けている患者ではまれに、そして一般的に発生します。長期治療を受けている患者の肺の状態を綿密に監視することは保証されており、潜在的なリスクと治療の利点を比較検討する必要があります。 (呼吸器反応を参照してください。)
肝毒性
肝炎、胆汁うっ滞性黄疸、慢性活動性肝炎、肝壊死などの肝反応はめったに起こりません。死亡者が報告されています。慢性活動性肝炎の発症は潜行性である可能性があり、肝障害を示す生化学的検査の変化について患者を定期的に監視する必要があります。肝炎が発生した場合は、直ちに薬を中止し、適切な処置を講じる必要があります。
神経障害
重度または不可逆になる可能性のある末梢神経障害が発生しています。死亡者が報告されています。腎機能障害 (クレアチニンクリアランスが毎分 60 mL 未満または臨床的に有意な血清クレアチニンの上昇)、貧血、真性糖尿病、電解質の不均衡、ビタミン B 欠乏症、衰弱性疾患などの状態は、末梢神経障害の発生を促進する可能性があります。長期治療を受けている患者は、腎機能の変化を定期的に監視する必要があります。
ニトロフラントイン製剤の市販後の経験では、視神経炎はめったに報告されていません。
溶血性貧血
プリマキン感受性型の溶血性貧血の症例は、ニトロフラントインによって誘発されています。溶血は、罹患患者の赤血球におけるグルコース-6-リン酸デヒドロゲナーゼ欠乏に関連しているようです。この欠乏症は、黒人の 10% と、地中海および近東起源の少数の民族グループに見られます。溶血は中止の目安です フラダンチン ;薬を中止すると溶血が止まります。
クロストリジウム・ディフィシル関連下痢症
クロストリジウム・ディフィシル関連下痢症 (CDAD) は、以下を含むほぼすべての抗菌剤の使用で報告されています。 フラダンチン 経口懸濁液であり、重症度は軽度の下痢から致命的な大腸炎までさまざまです。抗菌剤による治療は、結腸の正常な細菌叢を変化させ、C. difficile の異常増殖を引き起こします。
C. difficile は、CDAD の発症に寄与する毒素 A および B を産生します。 C. difficile の高毒素産生株は、これらの感染症が抗菌療法に抵抗性である可能性があり、結腸切除術を必要とする可能性があるため、罹患率と死亡率の増加を引き起こします。抗生物質の使用後に下痢を呈するすべての患者で、CDAD を考慮する必要があります。 CDADは抗菌薬投与後2か月以上経過すると報告されているため、病歴には注意が必要です。
CDAD が疑われるか確認された場合、C. difficile に対するものではない継続的な抗生物質の使用を中止する必要があるかもしれません。適切な体液と電解質の管理、タンパク質の補給、C. difficile の抗生物質治療、および外科的評価を、臨床的に必要な場合に開始する必要があります。
予防
非臨床毒性学
発がん、突然変異誘発、生殖能力の障害
ニトロフラントインは、メスの Holtzman ラットに 44.5 週間、またはメスの Sprague-Dawley ラットに 75 週間与えた場合、発がん性はありませんでした。雄と雌の Sprague-Dawley ラットを利用した 2 つの長期げっ歯類生物検定と、Swiss マウスと BDF1 マウスでの 2 つの長期生物検定では、発がん性の証拠は明らかにされなかった。
ニトロフラントインは、雌の B6C3F1 マウスにおける発がん活性の証拠を提示し、これは、管状腺腫、良性混合腫瘍、および卵巣の顆粒膜細胞腫瘍の発生率の増加によって示されます。雄の F344/N ラットでは、まれな腎尿細管細胞腫瘍、骨の骨肉腫、および皮下組織の腫瘍の発生率が増加しました。 75 mg/kg のニトロフラントインを妊娠雌マウスに皮下投与したある研究では、F1 世代で未知の重要性の肺乳頭腺腫が観察された。
ニトロフラントインは、ネズミチフス菌の特定の株に点突然変異を誘発し、L5178Y マウスリンパ腫細胞に前方突然変異を誘発することが示されています。ニトロフラントインは、チャイニーズハムスター卵巣細胞で姉妹染色分体交換および染色体異常の数の増加を誘発したが、培養中のヒト細胞では誘発しなかった.ショウジョウバエにおける伴性劣性致死試験の結果は、摂食または注射によるニトロフラントインの投与後に陰性であった。ニトロフラントインは、調べたげっ歯類モデルで遺伝性の突然変異を誘発しませんでした。
ヒトにおけるニトロフラントインの治療的使用に関連する発がん性および変異原性の所見の重要性は不明です。
ラットに高用量のニトロフラントインを投与すると、一時的な精子形成停止が引き起こされます。これは、薬を中止すると元に戻ります。健康な人間の男性に 10 mg/kg/日以上の用量を投与すると、特定の予測不可能な場合に、精子数の減少を伴う軽度から中等度の精子形成停止を引き起こす可能性があります。
妊娠
催奇形性効果
ヒトの用量の最大6倍の用量でウサギとラットでいくつかの繁殖研究が行われ、ニトロフラントインによる生殖能力の障害や胎児への害の証拠は明らかにされていません.ヒト用量の 68 倍のマウスで実施された 1 件の発表された研究 (母親に投与された mg/kg に基づく) では、成長遅延と軽度および一般的な奇形の発生率の低下が観察されました。しかし、人間の用量の 25 倍では、胎児の奇形は観察されませんでした。これらの発見と人間との関連性は不明です。しかし、妊娠中の女性を対象とした十分に管理された研究はありません。動物の繁殖研究は常に人間の反応を予測できるわけではないため、この薬は明らかに必要な場合にのみ妊娠中に使用する必要があります.
非催奇形効果
ニトロフラントインは、1 つの公開された経胎盤発がん性研究で、mg/kg ベースでヒト用量の 19 倍の用量で F1 世代のマウスに肺乳頭腺腫を誘発することが示されています。この所見と潜在的なヒトの発がんとの関係は、現在のところ不明です。これらの動物データの人間への影響に関する不確実性のため、この薬は明らかに必要な場合にのみ妊娠中に使用する必要があります.
労働と配達
見る 禁忌 .
授乳中の母親
ニトロフラントインは、ヒトの母乳中に微量検出されています。ニトロフラントインは、生後 1 か月未満の乳児に深刻な副作用を引き起こす可能性があるため、母親にとっての薬物の重要性を考慮して、授乳を中止するか、薬物を中止するかを決定する必要があります。 (見る 禁忌 )
小児用
安全性と有効性 フラダンチン 生後 1 か月未満の新生児では確立されていません。 (見る 禁忌 )
過剰摂取
の急性過剰摂取の時折の事件 フラダンチン 嘔吐以外の特別な症状はありません。嘔吐の誘導が推奨されます。特定の解毒剤はありませんが、薬物の尿中排泄を促進するために、水分摂取量を多く維持する必要があります。透析可能です。
禁忌
無尿、乏尿、または腎機能の重大な障害 (クレアチニンクリアランスが毎分 60 mL 未満または臨床的に有意な血清クレアチニンの上昇) は禁忌です。このタイプの患者の治療では、薬物の排泄が損なわれるため、毒性のリスクが高くなります。
未熟な赤血球酵素系 (グルタチオン不安定性) による溶血性貧血の可能性があるため、満期産 (妊娠 38 ~ 42 週)、陣痛および分娩中、または陣痛の開始が差し迫っている妊娠中の患者には禁忌です。同じ理由で、この薬は生後 1 か月未満の新生児には禁忌です。
フラダンチン ニトロフラントインに関連する胆汁うっ滞性黄疸/肝機能障害の既往歴のある患者には禁忌です。 フラダンチン また、ニトロフラントインに対する既知の過敏症のある患者には禁忌です。
臨床薬理学
経口投与 フラダンチン 吸収されやすく、尿中に速やかに排泄されます。通常、治療用量での血中濃度は低いです。尿への溶解性が高く、褐色を呈することがある。
100 mg を 1 日 1 回、7 日間投与した後、1 日目と 7 日目の平均尿中薬物回収率 (0 ~ 24 時間) は 42.7% と 43.6% でした。
多くの薬とは異なり、胃内容排出を遅らせる食物または薬剤の存在は、 フラダンチン 、おそらく胃液への溶解を改善することによって.
微生物学
作用機序
ニトロフラントインは、細菌のフラビンタンパク質を含む広範囲の酵素によって、DNA やタンパク質などの高分子に損傷を与える反応性中間体に還元されます。
交差抵抗
他の抗菌剤との交差耐性が発生する可能性がありますが、スルホンアミドとの交差耐性は観察されていません。
他の抗菌剤との相互作用
拮抗作用は、ニトロフラントインとキノロン抗菌剤の間で in vitro で実証されています。ニトロフラントイン経口懸濁液の形態のニトロフラントインは、in vitro および臨床感染の両方で、以下の細菌のほとんどに対して活性であることが示されています。 適応症と使用法 )。
グラム陽性菌
黄色ブドウ球菌Enterococcus種
グラム陰性菌
大腸菌
注: エンテロバクター種とクレブシエラ種の一部の株は、ニトロフラントインに耐性があります。
以下の in vitro データが利用可能ですが、それらの臨床的意義は不明です。ニトロフラントインは、以下の細菌に対して in vitro 活性を示します。しかし、これらの細菌による臨床感染症の治療におけるニトロフラントインの安全性と有効性は、十分に管理された臨床試験では確立されていません。
グラム陽性菌
コアグラーゼ陰性ブドウ球菌(Staphylococcus epidermidis および Staphylococcus saprophyticus を含む)Streptococcus agalactiaeViridans group streptococci
グラム陰性菌
Citrobacter koseriCitrobacter freundiiKlebsiella oxytoca
ニトロフラントインは、プロテウス種またはセラチア種のほとんどの菌株に対して活性がありません。シュードモナス属菌に対する活性はありません。
感受性試験
感受性試験の解釈基準、関連する試験方法、FDA が承認したこの薬剤の品質管理基準に関する具体的な情報については、http://www.fda.gov/STIC を参照してください。
患者情報
患者は摂取するように助言されるべきである フラダンチン 耐性をさらに強化し、薬物吸収を改善するために食物と一緒に。患者は治療の全過程を完了するように指示されるべきです。ただし、治療中に異常な症状が発生した場合は、医師に連絡するようアドバイスする必要があります。
下痢は抗生物質によって引き起こされる一般的な問題であり、通常は抗生物質の使用を中止すると終了します。抗生物質による治療を開始した後、患者は、抗生物質の最後の用量を服用してから2か月以上経っても、水様便や血便(胃痙攣や発熱の有無にかかわらず)を発症することがあります.これが発生した場合、患者はできるだけ早く医師に連絡する必要があります。
患者は、服用中は三ケイ酸マグネシウムを含む制酸剤を使用しないようにアドバイスする必要があります。 フラダンチン .
