Feldene 10mg, 20mg Piroxicam 使用法、副作用および投与量。 オンライン薬局の価格。 処方箋不要のジェネリック医薬品。
フェルデン 20mg とは何ですか?
ピロキシカムは、関節リウマチ(若年性関節炎を含む)または変形性関節症の痛みまたは炎症を治療するために使用される処方薬です。ピロキシカムは、単独で使用することも、他の薬と併用することもできます。
ピロキシカムは、非ステロイド性抗炎症薬 (NSAID) です。
ピロキシカムが 12 歳未満の子供に安全で効果があるかどうかはわかっていません。
フェルデンの可能な副作用は何ですか?
フェルデン 10mg は、次のような重大な副作用を引き起こす可能性があります。
- 首や耳がドキドキする
- 眠気、
- ぼやけた視界、
- 腫れ、
- 急激な体重増加、
- 呼吸困難、
- 食欲減少、
- 胃痛、
- 疲れ、
- かゆみ、
- 暗い尿 ,
- 粘土色のスツール、
- 皮膚や目の黄変(黄疸)、
- 血便またはタール便
- コーヒーかすのような吐血や吐血、
- 排尿がほとんどまたはまったくない、
- 足や足首のむくみ、
- ふらつき感、
- 手や足の冷え、
- 青白い肌と、
- 激しい頭痛、
上記の症状がある場合は、すぐに医療機関を受診してください。
フェルデンの最も一般的な副作用は次のとおりです。
- 異常な肝機能検査、
- 排尿困難、
- 胃のむかつき、
- 胸焼け、
- 食欲減少、
- 胃痛、
- 吐き気、
- 嘔吐、
- ガス、
- 下痢 、
- 便秘、
- めまい、
- 頭痛、
- かゆみやかぶれ、
- 耳鳴り、
気になる副作用や治らない副作用がある場合は、医師に相談してください。
これらは、フェルデンの考えられるすべての副作用ではありません.詳細については、医師または薬剤師にお尋ねください。
副作用に関する医学的アドバイスについては、医師に連絡してください。 1-800-FDA-1088 で副作用を FDA に報告できます。
警告
重篤な心血管および胃腸イベントのリスク
心血管血栓性イベント
- 非ステロイド性抗炎症薬 (NSAID) は、心筋梗塞や脳卒中などの重篤な心血管血栓性イベントのリスクを高め、致命的になる可能性があります。このリスクは治療の初期に発生する可能性があり、使用期間とともに増加する可能性があります。 [見る 警告と注意事項 ]。
- フェルデン 20 mg は、冠動脈バイパス移植 (CABG) 手術の設定では禁忌です [参照 禁忌 と 警告と注意事項 ]。
消化管出血、潰瘍、および穿孔
- NSAID は、胃や腸の出血、潰瘍、穿孔など、致命的な可能性がある重篤な胃腸 (GI) の有害事象のリスクを高めます。これらのイベントは、使用中にいつでも発生する可能性があり、警告の症状はありません。高齢患者および消化性潰瘍疾患および/または消化管出血の既往歴のある患者は、重篤な消化管イベントのリスクが高くなります[参照 警告と注意事項 ]。
説明
FELDENE (ピロキシカム) カプセルは、非ステロイド性抗炎症薬で、経口投与用の栗色および青色の #322 10 mg カプセルおよび栗色の #323 20 mg カプセルとして入手できます。化学名は、4-ヒドロキシル-2-メチル-N-2-ピリジニル-2H-1,2,-ベンゾチアジン-3-カルボキサミド 1,1-ジオキシドです。分子量は331.35です。その分子式は C15H13N3O4S で、次の化学構造を持っています。
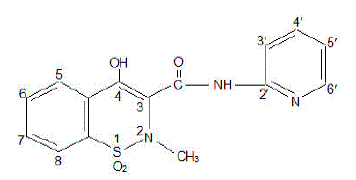
ピロキシカムは白色の結晶性固体として発生し、水、希酸、およびほとんどの有機溶媒にわずかに溶けます。アルコールや水溶液にわずかに溶けます。弱酸性の 4-ヒドロキシ プロトン (pKa 5.1) と弱塩基性のピリジル窒素 (pKa 1.8) を示します。
フェルデン 10mg の不活性成分には、青 1、赤 3、乳糖、ステアリン酸マグネシウム、ラウリル硫酸ナトリウム、デンプンが含まれます。
適応症
フェルデンが示されています:
- 変形性関節症の徴候と症状の緩和に。
- 関節リウマチの徴候と症状の緩和に。
投薬と管理
FELDENE の使用を決定する前に、FELDENE 20mg およびその他の治療オプションの潜在的な利点とリスクを慎重に検討してください。個々の患者の治療目標に一致する最短の期間で最低の有効用量を使用する [参照 警告と注意事項 ]。
FELDENE 20mg による初期治療に対する反応を観察した後、個々の患者のニーズに合わせて用量と頻度を調整する必要があります。
関節リウマチおよび変形性関節症の緩和には、1 日 1 回 20 mg を経口投与します。必要に応じて、1 日量を分割することもできます。 FELDENE の半減期が長いため、7 ~ 12 日間は定常状態の血中濃度に達しません。したがって、FELDENE の治療効果は治療の早い段階で明らかですが、数週間にわたって反応が徐々に増加するため、治療の効果は 2 週間評価されるべきではありません。
供給方法
剤形と強度
フェルデン(ピロキシカム)カプセル
10mg マルーン&ブルー #322 20mg マルーン #323
保管と取り扱い
FELDENE® (ピロキシカム) 10 mg カプセル 栗色と青色の #322 で、次のように提供されます。
FELDENE® (ピロキシカム) 20 mg カプセル マルーン #323 で、次のように提供されます。
保管所
室温 20°C ~ 25°C (68°F ~ 77°F) で保管してください。 15°C から 30°C (59°F から 86°F) の間で許容される逸脱 [USP 制御室温を参照]。
配布元: Pfizer Labs, Division of Pfizer Inc., 235 East 42nd Street, New York, NY 10017. 改訂: 2017 年 4 月.
副作用
次の副作用については、ラベルの他のセクションで詳しく説明しています。
- 心血管血栓性イベント [参照 警告と注意事項 ]
- 消化管出血、潰瘍および穿孔 [参照 警告と注意事項 ]
- 肝毒性 [参照 警告と注意事項 ]
- 高血圧 [参照 警告と注意事項 ]
- 心不全および浮腫 [参照 警告と注意事項 ]
- 腎毒性および高カリウム血症 [参照 警告と注意事項 ]
- アナフィラキシー反応 [参照 警告と注意事項 ]
- 深刻な皮膚反応 [参照 警告と注意事項 ]
- 血液毒性 [参照 警告と注意事項 ]
臨床試験の経験
臨床試験はさまざまな条件下で実施されるため、ある医薬品の臨床試験で観察された副作用率を別の医薬品の臨床試験で観察された率と直接比較することはできず、実際に観察された率を反映していない可能性があります。
FELDENE 10mg または他の NSAID を服用している患者において、患者の約 1 ~ 10% で発生する最も頻繁に報告されている有害事象は次のとおりです。
心臓血管系: 浮腫
消化器系: 食欲不振、腹痛、便秘、下痢、鼓腸、吐き気、嘔吐
神経系 :めまい、頭痛、めまい
皮膚と付属物: かゆみ、かぶれ
特別な感覚: 耳鳴り
時折報告される追加の有害な経験には、次のものがあります。
心臓血管系: 動悸
消化器系: 口内炎
神経系: 眠気
特別な感覚: ぼやけた視界
市販後の経験
FELDENEの承認後の使用中に、次の副作用が確認されています。これらの反応は不確かな規模の集団から自発的に報告されるため、その頻度を確実に推定したり、薬物曝露との因果関係を確立したりすることは常に可能ではありません.
全身: 発熱、感染症、敗血症、アナフィラキシー反応、食欲の変化、死亡、インフルエンザ様症候群、痛み(疝痛)、血清病
心臓血管系: うっ血性心不全、高血圧、頻脈、失神、不整脈、狭心症の増悪、低血圧、心筋梗塞、血管炎
消化器系: 消化不良、肝臓酵素の上昇、総出血/穿孔、胸やけ、潰瘍(胃/十二指腸)、口渇、食道炎、胃炎、舌炎、吐血、肝炎、黄疸、下血、直腸出血、おくび、肝不全、膵炎
血液およびリンパ系: 貧血、出血時間の増加、 e 斑状出血、好酸球増加症、鼻出血、白血球減少症、紫斑病、点状出血、血小板減少症、無顆粒球症、溶血性貧血、再生不良性貧血、リンパ節腫脹、汎血球減少症
過敏症: 正ANA
代謝と栄養: 体重変化、体液貯留、高血糖、低血糖
神経系: 不安、無力症、錯乱、うつ病、夢異常、不眠症、倦怠感、神経過敏、感覚異常、傾眠、振戦、アカシジア、痙攣、昏睡、幻覚、髄膜炎、気分の変化
呼吸器系: 喘息、呼吸困難、呼吸抑制、肺炎
皮膚と付属物: 脱毛症、あざ、落屑、紅斑、光線過敏症、発汗、血管性浮腫、中毒性表皮壊死症、多形紅斑、剥離性皮膚炎、爪甲剥離症、スティーブンス・ジョンソン症候群、蕁麻疹、水泡性反応
特別な感覚: 結膜炎、難聴、目の腫れ
泌尿生殖器系: 腎機能異常、 c 膀胱炎、排尿障害、血尿、高カリウム血症、間質性腎炎、ネフローゼ症候群、乏尿・多尿、タンパク尿、腎不全、糸球体腎炎
生殖器系および乳房障害: 女性の生殖能力の低下
薬物相互作用
ピロキシカムとの臨床的に重要な薬物相互作用については、表 1 を参照してください。
警告
の一部として含まれています "予防" セクション
予防
心血管血栓性イベント
いくつかの COX-2 選択的および非選択的 NSAID の最大 3 年間の臨床試験では、心筋梗塞 (MI) や脳卒中などの重篤な心血管 (CV) 血栓性イベントのリスクが高くなり、致命的な可能性があることが示されています。利用可能なデータに基づくと、CV 血栓イベントのリスクがすべての NSAID で同様であることは明らかではありません。 NSAID の使用によってもたらされるベースラインを超える重篤な心血管血栓性イベントの相対的な増加は、既知の心血管疾患または心血管疾患の危険因子がある場合とない場合で同様であるように思われます。しかし、既知の心血管疾患または危険因子を持つ患者は、ベースライン率が高いため、過剰な重篤な心血管血栓イベントの絶対発生率が高くなりました。いくつかの観察研究では、深刻な CV 血栓症のリスクの増加は、治療の最初の数週間で始まったことがわかりました。 CV 血栓リスクの増加は、高用量で最も一貫して観察されています。
NSAID 治療を受けている患者の有害な CV イベントの潜在的なリスクを最小限に抑えるために、可能な限り短い期間で最小の有効用量を使用してください。医師と患者は、以前の心血管症状がなくても、治療過程全体を通して、そのような事象の発生に注意を払う必要があります。重篤な心血管イベントの症状と、発生した場合の対処法について、患者に説明する必要があります。
アスピリンの同時使用が、NSAID の使用に関連する重篤な CV 血栓イベントのリスク増加を軽減するという一貫した証拠はありません。アスピリンとピロキシカムなどの NSAID の同時使用は、重篤な胃腸(GI)イベントのリスクを高めます。 消化管出血、潰瘍、および穿孔 ]。
冠動脈バイパス移植(CABG)手術後の状態
CABG 手術後の最初の 10 ~ 14 日間の痛みを治療するための COX-2 選択的 NSAID に関する 2 つの大規模な対照臨床試験では、心筋梗塞と脳卒中の発生率が増加することがわかりました。 NSAIDs は、CABG の状況では禁忌です [参照 禁忌 ]。
MI後の患者
デンマーク国民登録簿で実施された観察研究では、MI 後の期間に NSAID で治療された患者は、治療の最初の週から、再梗塞、心血管関連死、および全死因死亡のリスクが高いことが示されました。この同じコホートでは、MI 後 1 年間の死亡率は、非 NSAID 曝露患者では 100 人年あたり 12 であるのに対し、NSAID 治療患者では 100 人年あたり 20 でした。絶対死亡率は MI 後 1 年目から幾分低下したが、NSAID 使用者の死亡の相対リスクの増加は、少なくともその後 4 年間の追跡調査で持続した。
最近の心筋梗塞患者へのフェルデン 10mg の使用は、CV 血栓性イベントの再発のリスクを上回ると予想される場合を除き、避けてください。 FELDENE を心筋梗塞を発症したばかりの患者に使用する場合は、心虚血の徴候がないか患者を監視してください。
消化管出血、潰瘍、および穿孔
FELDENE を含む NSAID は、食道、胃、小腸、または大腸の炎症、出血、潰瘍、穿孔など、致命的な可能性がある重篤な胃腸 (GI) 有害事象を引き起こします。これらの重篤な有害事象は、NSAID で治療されている患者において、警告症状の有無にかかわらず、いつでも発生する可能性があります。 NSAID 療法で重篤な上部消化管の有害事象を発症した患者の 5 人に 1 人のみが症状を示します。 NSAID による上部消化管潰瘍、肉眼的出血、または穿孔は、3 ~ 6 か月間治療を受けた患者の約 1%、1 年間治療を受けた患者の約 2% ~ 4% で発生しました。ただし、短期間の NSAID 治療でもリスクがないわけではありません。
消化管出血、潰瘍、および穿孔の危険因子
消化性潰瘍疾患および/または消化管出血の既往歴があり、NSAID を使用した患者は、これらの危険因子のない患者と比較して、消化管出血を発症するリスクが 10 倍以上高くなりました。 NSAID で治療された患者の消化管出血のリスクを高めるその他の要因には、NSAID 治療の長期化が含まれます。経口コルチコステロイド、アスピリン、抗凝固薬、または選択的セロトニン再取り込み阻害薬(SSRI)の併用。喫煙;アルコールの使用;高齢;および一般的な健康状態が悪い。致命的な消化管イベントに関する市販後の報告のほとんどは、高齢者または衰弱した患者で発生しました。さらに、進行した肝疾患および/または凝固障害のある患者は、消化管出血のリスクが高くなります。
NSAID 治療患者の消化管リスクを最小限に抑えるための戦略
- 可能な限り短い期間で最低の有効量を使用してください。
- 一度に複数の NSAID を投与することは避けてください。
- 利点が出血のリスクの増加を上回ると予想される場合を除き、リスクの高い患者への使用は避けてください。そのような患者、および活動性消化管出血のある患者については、NSAIDs 以外の代替療法を検討してください。
- NSAID 治療中は、消化管潰瘍や出血の徴候や症状に注意してください。
- 重篤な胃腸の有害事象が疑われる場合は、直ちに評価と治療を開始し、重篤な胃腸の有害事象が除外されるまで FELDENE の使用を中止してください。
- 心臓予防のために低用量アスピリンを併用している状況では、消化管出血の証拠について患者をより綿密に監視する[参照 薬物相互作用 ]。
肝毒性
ALT または AST の上昇 (正常 [ULN] の上限の 3 倍以上) が、臨床試験で NSAID 治療を受けた患者の約 1% で報告されています。さらに、劇症肝炎、肝壊死、肝不全などのまれな、時には致命的な重度の肝障害の症例が報告されています。
ALT または AST の上昇 (ULN の 3 倍未満) は、ピロキシカムを含む NSAID で治療された患者の最大 15% で発生する可能性があります。
肝毒性の兆候と症状(吐き気、疲労、嗜眠、下痢、かゆみ、黄疸、右上腹部圧痛、「インフルエンザ様」症状など)について患者に知らせる。肝疾患に一致する臨床徴候や症状が現れた場合、または全身症状が現れた場合 (例えば、好酸球増加症、発疹など)、直ちにフェルデンの服用を中止し、患者の臨床評価を行ってください。
高血圧症
FELDENE を含む NSAID は、高血圧の新たな発症または既存の高血圧の悪化につながる可能性があり、いずれも CV イベントの発生率の増加に寄与する可能性があります。アンギオテンシン変換酵素 (ACE) 阻害薬、サイアザイド利尿薬、またはループ利尿薬を服用している患者は、NSAID を服用すると、これらの治療に対する反応が損なわれる可能性があります [参照 薬物相互作用 ]。
NSAID 治療の開始時および治療中は、血圧 (BP) を監視します。
心不全と浮腫
Coxib と従来の NSAID Trialists のコラボレーションによるランダム化比較試験のメタ分析では、COX-2 選択的治療を受けた患者および非選択的 NSAID 治療を受けた患者では、プラセボ治療を受けた患者と比較して、心不全による入院が約 2 倍増加したことが示されました。心不全患者を対象としたデンマーク国立登録簿の研究では、NSAID の使用により心筋梗塞、心不全による入院、および死亡のリスクが増加しました。
さらに、体液貯留と浮腫は、NSAID で治療された一部の患者で観察されています。ピロキシカムの使用は、これらの病状の治療に使用されるいくつかの治療薬(利尿薬、ACE 阻害薬、またはアンギオテンシン受容体遮断薬 [ARB] など)の CV 効果を鈍らせる可能性がある [参照 薬物相互作用 ]。
ベネフィットが心不全の悪化のリスクを上回ると予想される場合を除き、重度の心不全患者への FELDENE 10mg の使用は避けてください。重度の心不全患者に FELDENE を使用する場合は、心不全の悪化の徴候がないか患者を監視してください。
腎毒性と高カリウム血症
腎毒性
NSAIDs の長期投与は、腎乳頭壊死およびその他の腎損傷をもたらしました。
腎毒性は、腎プロスタグランジンが腎灌流の維持において代償的役割を果たしている患者にも見られます。これらの患者では、NSAID の投与によりプロスタグランジン生成が用量依存的に減少し、二次的に腎血流が減少し、明らかな腎代償不全が引き起こされる可能性があります。この反応のリスクが最も高い患者は、腎機能障害、脱水、循環血液量減少、心不全、肝機能障害、利尿薬および ACE 阻害薬または ARB を服用している患者、および高齢者です。通常、NSAID 療法を中止すると、治療前の状態に戻ります。
進行性腎疾患患者における FELDENE 20mg の使用に関する対照臨床試験からの情報は入手できません。 FELDENE 20mgの腎臓への影響は、既存の腎疾患を持つ患者の腎機能障害の進行を早める可能性があります.
FELDENE を開始する前に、脱水症または血液量減少症の患者の体液量の状態を修正します。 FELDENE 使用中は、腎機能障害、肝機能障害、心不全、脱水症、循環血液量減少症の患者の腎機能をモニタリングする [参照 薬物相互作用 ]。有益性が腎機能の悪化のリスクを上回ると予想される場合を除き、進行した腎疾患のある患者への FELDENE の使用は避けてください。進行した腎疾患の患者に FELDENE を使用する場合は、腎機能の悪化の徴候がないか患者を監視してください。
高カリウム血症
高カリウム血症を含む血清カリウム濃度の上昇は、腎機能障害のない一部の患者でさえ、NSAID の使用で報告されています。腎機能が正常な患者では、これらの影響は低レニン血症-低アルドステロン症状態に起因するとされています。
アナフィラキシー反応
ピロキシカムは、ピロキシカムに対する既知の過敏症の有無にかかわらず、アスピリン感受性喘息患者のアナフィラキシー反応と関連している[参照 禁忌 と アスピリン感受性に関連する喘息の増悪 ]。
アナフィラキシー反応が発生した場合は、緊急の助けを求めてください。
アスピリン感受性に関連する喘息の増悪
喘息患者の亜集団は、鼻ポリープを合併した慢性副鼻腔炎を含む可能性があるアスピリン感受性喘息を有する可能性があります。重度の致命的な気管支痙攣;および/またはアスピリンやその他の NSAID に対する不耐性。このようなアスピリン感受性患者では、アスピリンと他の NSAID との交差反応性が報告されているため、フェルデン 20mg は、この形態のアスピリン感受性を持つ患者には禁忌です [ 禁忌 ]。喘息の既往がある患者(アスピリン感受性がない)に FELDENE を使用する場合は、喘息の徴候や症状の変化について患者を監視してください。
深刻な皮膚反応
ピロキシカムを含む NSAID は、剥脱性皮膚炎、スティーブンス・ジョンソン症候群 (SJS)、中毒性表皮壊死症 (TEN) などの重篤な皮膚有害反応を引き起こす可能性があり、致命的となる可能性があります。これらの重大なイベントは、予告なしに発生する可能性があります。重篤な皮膚反応の兆候と症状について患者に知らせ、皮膚発疹または過敏症の他の兆候が最初に現れた場合は、フェルデン 10mg の使用を中止してください。 FELDENE 20mg は、以前に NSAIDs に対して重篤な皮膚反応を示した患者には禁忌です [参照 禁忌 ]。
胎児動脈管の早期閉鎖
ピロキシカムは、胎児の動脈管の早期閉鎖を引き起こす可能性があります。妊娠 30 週(第 3 トリメスター)以降の妊婦には、FELDENE 20mg を含む NSAID の使用を避けてください。 特定の集団での使用 ]。
血液毒性
NSAID治療を受けた患者に貧血が発生しました。これは、潜在的または総失血、体液貯留、または不完全に記述された赤血球生成への影響が原因である可能性があります。 FELDENE で治療された患者に貧血の徴候や症状がある場合は、ヘモグロビンまたはヘマトクリットを監視してください。
FELDENE を含む NSAID は、出血イベントのリスクを高める可能性があります。凝固障害、ワルファリンの併用、他の抗凝固薬、抗血小板薬(アスピリンなど)、セロトニン再取り込み阻害薬(SSRI)、セロトニン・ノルエピネフリン再取り込み阻害薬(SNRI)などの併存疾患は、このリスクを高める可能性があります。これらの患者の出血の徴候を監視します [参照 薬物相互作用 ]。
炎症と発熱のマスキング
フェルデン 10mg の炎症とおそらく発熱を抑える薬理学的活性は、感染を検出する際の診断的兆候の有用性を低下させる可能性があります。
ラボモニタリング
深刻な消化管出血、肝毒性、および腎障害は、警告の症状や徴候なしに発生する可能性があるため、長期の NSAID 治療を受けている患者を定期的に CBC および化学的プロファイルでモニタリングすることを検討してください。 消化管出血、潰瘍、穿孔、肝毒性、腎毒性、高カリウム血症 ] .
眼科効果
非ステロイド性抗炎症剤による有害な眼所見の報告があるため、フェルデンによる治療中に視覚障害を発症した患者には眼科的評価を受けることをお勧めします。

患者相談情報
患者に、FDA 承認の患者ラベル ( 投薬ガイド ) 調剤される各処方箋に添付されます。フェルデンによる治療を開始する前に、また進行中の治療中に定期的に、患者、家族、またはその介護者に次の情報を知らせてください。
心血管血栓性イベント
胸痛、息切れ、脱力感、ろれつが回らないなどの心血管血栓性イベントの症状に注意し、これらの症状があればすぐに医療提供者に報告するように患者に助言する[参照 警告と注意事項 ]。
消化管出血、潰瘍、および穿孔
心窩部痛、消化不良、下血、吐血などの潰瘍や出血の症状を医療提供者に報告するよう患者に助言します。心臓予防のために低用量アスピリンを併用する状況では、患者に消化管出血のリスクの増加とその徴候と症状を知らせる[参照 警告と注意事項 ]。
肝毒性
肝毒性の兆候と症状(吐き気、疲労、無気力、かゆみ、下痢、黄疸、右上腹部圧痛、「インフルエンザ様」症状など)について患者に知らせる。これらが発生した場合は、患者に FELDENE を中止し、直ちに医学的治療を受けるように指示します [参照] 警告と注意事項 ]。
心不全と浮腫
息切れ、原因不明の体重増加、または浮腫などのうっ血性心不全の症状に注意し、そのような症状が発生した場合は医療提供者に連絡するよう患者に助言する[参照 警告と注意事項 ]。
アナフィラキシー反応
アナフィラキシー反応の徴候(例、呼吸困難、顔や喉の腫れ)を患者に知らせてください。これらが発生した場合は、直ちに緊急の助けを求めるように患者に指示します[参照 禁忌 と 警告と注意事項 ]。
深刻な皮膚反応
何らかの発疹が現れた場合は、直ちに FELDENE を中止し、できるだけ早く医療提供者に連絡するよう患者に助言してください [ 警告と注意事項 ]。
女性の生殖能力
妊娠を希望する生殖能力のある女性には、フェルデン 20mg を含む NSAIDs が排卵の可逆的遅延と関連している可能性があることをアドバイスする [ 特定の集団での使用 ]。
胎児毒性
妊娠中の女性には、胎児の動脈管が早期に閉鎖するリスクがあるため、妊娠 30 週から FELDENE やその他の NSAID の使用を避けるように伝えてください。 警告と注意事項 と 特定の集団での使用 ]。
NSAIDの併用を避ける
FELDENE と他の NSAIDs またはサリチル酸塩(例、ジフルニサル、サルサレート)との併用は、胃腸毒性のリスクが高く、有効性がほとんどまたはまったく増加しないため、推奨されないことを患者に知らせる [参照 警告と注意事項 と 薬物相互作用 ]。風邪、発熱、または不眠症の治療のための「市販薬」に NSAIDs が含まれている可能性があることを患者に警告します。
NSAID と低用量アスピリンの使用
医療提供者に相談するまで、フェルデンと併用して低用量アスピリンを使用しないように患者に伝えます[ 薬物相互作用 ]。
非臨床毒性学
発がん、突然変異誘発、生殖能力の障害
発がん
ピロキシカムの発がん性を特徴付ける長期の動物実験は行われていません。
突然変異誘発
ピロキシカムは、Ames 細菌復帰突然変異試験またはマウスの優性致死突然変異試験で変異原性を示さず、マウスの in vivo 染色体異常試験で染色体異常誘発性を示さなかった。
生殖能力の障害
ラットにピロキシカムを 2、5、または 10 mg/kg/日の用量で投与した生殖研究 (mg/m2 体表面積 [BSA] に基づく 20 mg の最大推奨ヒト用量 [MRHD] の 5 倍まで)男性または女性の生殖能力に障害がないことを明らかにしました。
特定の集団での使用
妊娠
リスクの概要
妊娠後期に FELDENE 20mg を含む NSAID を使用すると、胎児の動脈管が早期に閉鎖するリスクが高まります。妊娠 30 週(第 3 トリメスター)以降の妊婦には、FELDENE 10mg を含む NSAID の使用を避けてください。
妊娠中の女性における FELDENE 20mg の十分に管理された研究はありません。
妊娠第 1 期または第 2 期の女性における NSAID 使用の潜在的な胎児リスクに関する観察研究のデータは決定的ではありません。米国の一般集団では、臨床的に認められたすべての妊娠は、薬物曝露に関係なく、重大な奇形の背景率が 2 ~ 4%、流産の背景率が 15 ~ 20% です。
ラットとウサギの動物繁殖試験では、それぞれ MRHD の 5 倍と 10 倍までの曝露で催奇形性の証拠はありませんでした。ピロキシカムを用いたラットの研究では、MRHD の 2 倍の暴露で胎仔毒性 (着床後損失) が観察され、ピロキシカムの MRHD と同等の用量で分娩の遅延と死産の発生率の増加が認められました。動物データに基づいて、プロスタグランジンは子宮内膜の血管透過性、胚盤胞着床、および脱落膜化において重要な役割を果たしていることが示されています。動物実験では、ピロキシカムなどのプロスタグランジン合成阻害剤の投与により、着床前および着床後の損失が増加しました。
臨床上の考慮事項
労働または配達
分娩中のフェルデンの影響に関する研究はありません。動物実験では、ピロキシカムを含む NSAIDS はプロスタグランジン合成を阻害し、分娩を遅らせ、死産の発生率を高めます。
データ
動物データ
器官形成期 (妊娠 6 日目から 15 日目) に 2、5、または 10 mg/kg/日でピロキシカムを投与された妊娠ラットは、5 および 10 mg/kg/日のピロキシカム (2 およびmg/m2 体表面積 [BSA] に基づいて、それぞれ 20 mg の最大推奨ヒト用量 [MRHD] の 5 倍)。子孫に認められた薬物関連の発達異常はありませんでした。胃腸管毒性は、妊娠していないラットまたは妊娠初期のラットと比較して、妊娠後期の妊娠ラットで増加した。器官形成期 (妊娠 7 日目から 18 日目) に 2、5、または 10 mg/kg/日でピロキシカムを投与された妊娠ウサギは、子孫に薬物関連の発達異常を示さなかった (mg/m2 に基づく MRHD の最大 10 倍)。 BSA)。
妊娠ラットにピロキシカムを妊娠 15 日目に 2、5、または 10 mg/kg/日で分娩および子孫の離乳を経て投与した出生前および出生後の発育試験では、体重増加の減少および死亡が母動物で観察されました。 10 mg/kg/日 (mg/m2 BSA に基づく MRHD の 5 倍) を妊娠 20 日目から開始。処置した母動物は、腹膜炎、癒着、胃出血、出血性腸炎、および子宮内胎児死亡を明らかにした。すべてのピロキシカム治療群(MRHD と同等の用量)で分娩が遅れ、死産の発生率が増加しました。重度の母体毒性に続発する母体のケアがないため、生後の発達を確実に評価することはできませんでした。
授乳
リスクの概要
合計 6 人の授乳中の女性と 2 人の乳児を含む 2 つの公開されたレポートからの限られたデータは、ピロキシカムが母親の濃度の約 1% から 3% で母乳中に排泄されることを示しました。治療中、母体の血漿中のピロキシカムと比較して、乳中のピロキシカムの蓄積は発生しませんでした。母乳育児の発達上および健康上の利点は、フェルデン 20mg に対する母親の臨床的必要性、およびフェルデンまたは基礎となる母体の状態による母乳育児への潜在的な悪影響とともに考慮されるべきです。
生殖能力のある雌と雄
不妊
女性
作用機序に基づいて、FELDENE を含むプロスタグランジンを介した NSAID の使用は、一部の女性の可逆的不妊症に関連している卵胞の破裂を遅らせたり、予防したりする可能性があります。発表された動物研究は、プロスタグランジン合成阻害剤の投与が、排卵に必要なプロスタグランジン媒介卵胞破裂を妨害する可能性があることを示しています. NSAIDs で治療された女性を対象とした小規模な研究でも、可逆的な排卵遅延が示されています。妊娠困難な女性や不妊症の調査を受けている女性では、FELDENE を含む NSAID の中止を検討してください。
小児用
FELDENE 20mg は、小児患者では調査されていません。フェルデン 10mg の安全性と有効性は確立されていません。
高齢者の使用
高齢の患者は、若い患者と比較して、NSAID に関連する重篤な心血管、胃腸、および/または腎臓の副作用のリスクが高くなります。高齢患者にとって予想される利益がこれらの潜在的なリスクを上回る場合は、投与範囲の下限から投与を開始し、副作用について患者を監視します[参照 警告と注意事項 ]。
過剰摂取
急性 NSAID 過剰摂取後の症状は、通常、無気力、眠気、吐き気、嘔吐、心窩部痛に限定されており、一般に支持療法で元に戻すことができます。消化管出血が発生しました。高血圧、急性腎不全、呼吸抑制、および昏睡が発生しましたが、まれでした [ 警告と注意事項 ]。
NSAID の過剰摂取後は、対症療法と支持療法で患者を管理します。特定の解毒剤はありません。嘔吐および/または活性炭 (成人で 60 ~ 100 グラム、小児患者では体重 1 kg あたり 1 ~ 2 グラム) および/または摂取後 4 時間以内に見られる症状のある患者または大量の過剰摂取 (推奨用量の 5 ~ 10 倍)。
ピロキシカムの過剰摂取を治療する場合、ピロキシカムの長い血漿中半減期を考慮する必要があります。強制利尿、尿のアルカリ化、血液透析、または血液灌流は、タンパク質結合が高いため役に立たない場合があります。
過剰摂取の治療に関する追加情報については、毒物管理センター (1-800-222-1222) にお問い合わせください。
禁忌
フェルデン 10mg は、次の患者には禁忌です。
- -ピロキシカムまたは医薬品の成分に対する既知の過敏症(例、アナフィラキシー反応および重篤な皮膚反応)[参照 警告と注意事項 ]
- -アスピリンまたは他のNSAIDを服用した後の喘息、蕁麻疹、またはその他のアレルギー型反応の病歴。そのような患者では、NSAIDsに対する重度の、時には致命的なアナフィラキシー反応が報告されています[ 警告と注意事項 ]
- 冠動脈バイパス移植 (CABG) 手術の状況 [参照 警告と注意事項 ]
臨床薬理学
作用機序
ピロキシカムには、鎮痛、抗炎症、および解熱特性があります。
FELDENE 20mg の作用機序は、他の NSAIDs と同様に完全には解明されていませんが、シクロオキシゲナーゼ (COX-1 および COX-2) の阻害が関与しています。
ピロキシカムは、in vitro でのプロスタグランジン (PG) 合成の強力な阻害剤です。治療中に到達したピロキシカム濃度は、in vivo 効果を生み出しました。プロスタグランジンは求心性神経を敏感にし、動物モデルで痛みを誘発するブラジキニンの作用を増強します。プロスタグランジンは炎症のメディエーターです。ピロキシカムはプロスタグランジン合成の阻害剤であるため、その作用機序は末梢組織におけるプロスタグランジンの減少によるものと考えられます。
薬物動態
一般的な薬物動態特性
ピロキシカムの薬物動態は、健康な被験者、特別な集団、および患者で特徴付けられています。ピロキシカムの薬物動態は線形です。線量の増加に比例して暴露量が増加することが観察されます。長い半減期 (50 時間) により、1 日 1 回の投与で 1 日を通して比較的安定した血漿濃度が維持され、複数回の投与でかなり蓄積されます。ほとんどの患者は、7 ~ 12 日以内に定常状態の血漿レベルに近づきます。ピロキシカムの血漿半減期がより長い患者では、2 ~ 3 週間で定常状態に近い高レベルが観察されています。
吸収
ピロキシカムは、経口投与後によく吸収されます。薬物の血漿中濃度は 10 mg と 20 mg の用量で比例し、一般に投与後 3 ~ 5 時間以内にピークに達します。通常、20 mg の単回投与では、ピロキシカムのピーク血漿レベルは 1.5 ~ 2 mcg/mL になりますが、20 mg のピロキシカムを毎日繰り返し投与した後の最大薬物血漿濃度は、通常 3 ~ 8 mcg/mL で安定します。
食事の場合、吸収率はわずかに遅れますが、経口投与後の吸収の程度は遅くありません。制酸剤 (水酸化アルミニウムまたは水酸化マグネシウムと水酸化アルミニウム) の同時投与は、経口投与されたピロキシカムの血漿レベルに影響を与えないことが示されています。
分布
ピロキシカムの見かけの分布体積は、約 0.14 L/kg です。血漿ピロキシカムの 99% は血漿タンパク質に結合しています。ピロキシカムは母乳中に排泄されます。母乳中の存在は、初期および長期の状態 (52 日間) で測定されています。ピロキシカムは、母体濃度の約 1% から 3% で母乳中に現れました。ピロキシカムの蓄積は、治療中の血漿と比較して乳に発生しませんでした。
排除
代謝
ピロキシカムの代謝は、ピリジル側鎖の 5 位でのヒドロキシル化とこの生成物の抱合によって起こります。脱水環化による;アミド結合の加水分解、脱炭酸、環の収縮、および N-脱メチル化を含む一連の反応によって。インビトロ研究では、シトクロム P4502C9 (CYP2C9) が、主要な代謝産物である 5'-ヒドロキシピロキシカムの形成に関与する主要な酵素であることを示しています [ ファーマコゲノミクス ]。ピロキシカム代謝の生体内変換産物には、抗炎症活性がないと報告されています。
CYP2C9 多型を持つ被験者では、正常な代謝タイプの被験者と比較して、ピロキシカムのより高い全身曝露が認められています [ ファーマコゲノミクス ]。
排泄
ピロキシカムとその生体内変化生成物は、尿と糞便中に排泄され、糞便中の約 2 倍が尿中に現れます。フェルデン 10mg の投与量の約 5% が変化せずに排泄されます。ピロキシカムの血漿半減期 (t½ ) は約 50 時間です。
特定の集団
小児科
ピロキシカムは、小児患者では調査されていません。
人種
人種による薬物動態の違いは確認されていません。
肝障害
ピロキシカムの薬物動態に対する肝疾患の影響は確立されていません。しかし、ピロキシカムの排泄のかなりの部分は肝代謝によって行われます。その結果、肝疾患の患者は、正常な肝機能の患者と比較して、ピロキシカムの投与量を減らす必要がある場合があります。
腎障害
ピロキシカムの薬物動態は、腎不全の患者で調査されています。研究によると、軽度から中等度の腎障害を持つ患者は、投与量の調整を必要としない場合があります。しかし、重度の腎不全患者または血液透析を受けている患者におけるピロキシカムの薬物動態特性は知られていません。
薬物相互作用研究
制酸剤
制酸剤の同時投与は、ピロキシカムの血漿レベルに影響を与えませんでした。
アスピリン
ピロキシカムをアスピリンと一緒に投与すると、そのタンパク質結合が減少しましたが、遊離フェルデン 20mg のクリアランスは変化しませんでした。アスピリン (3900 mg/日) と併用してフェルデン (20 mg/日) を投与した場合、ピロキシカムの血漿レベルは正常値の約 80% に減少しました。この相互作用の臨床的重要性は知られていない[参照 薬物相互作用 ]。
ファーマコゲノミクス
CYP2C9 * 2 および CYP2C9 * 3 多型などの遺伝子多型を持つ個人では、CYP2C9 活性が低下します。公開された 2 つのレポートからの限られたデータは、ヘテロ接合 CYP2C9*1/*2 (n=9)、ヘテロ接合 CYP2C9*1/*3 (n=9)、およびホモ接合 CYP2C9*3/*3 (n=1) 遺伝子型を持つ被験者を示しました。ピロキシカムの全身レベルは、単回経口投与後の CYP2C9*1/*1 (n=17、正常代謝遺伝子型) の被験者よりも、それぞれ 1.7 倍、1.7 倍、5.3 倍高かった。 CYP2C9*1/*3 (n=9) および CYP2C9*3/*3 (n=1) 遺伝子型の被験者のピロキシカムの平均消失半減期値は、CYP2C9*1 の被験者よりも 1.7 倍および 8.8 倍高かった/*1 (n=17)。ホモ接合*3/*3 遺伝子型の頻度は、一般集団の 0% から 1% であると推定されています。ただし、特定の民族グループでは 5.7% もの高い頻度が報告されています。
CYP2C9 基質の代謝不良者
遺伝子型または他の CYP2C9 基質 (ワルファリンやフェニトインなど) の使用歴/経験に基づいて CYP2C9 代謝不良であることが知られている、または疑われる患者では、代謝クリアランスの低下により血漿レベルが異常に高くなる可能性があるため、用量の減量を検討してください。
臨床研究
制御された臨床試験では、関節リウマチと変形性関節症の急性増悪と長期管理の両方に対するフェルデンの有効性が確立されています。
FELDENE 20mg の治療効果は、両方の疾患の治療の早い段階で明らかであり、数週間 (8 ~ 12 週間) にわたって反応が徐々に増加します。有効性は、痛みの軽減、および存在する場合は炎症の沈静という点で見られます。
FELDENE 20mg/日 20 mg の用量は、アスピリンの治療用量に匹敵する治療効果を示し、マイナーな胃腸への影響と耳鳴りの発生率が低くなります。
FELDENE 10mg は、固定用量の金およびコルチコステロイドと同時に投与されています。 「ステロイド節約」効果の存在は、今日まで十分に研究されていません。
患者情報
非ステロイド性抗炎症薬 (NSAIDs) と呼ばれる薬について知っておくべき最も重要な情報は何ですか?
NSAID は、次のような重大な副作用を引き起こす可能性があります。
- 死に至る可能性のある心臓発作や脳卒中のリスクが高まります。 このリスクは治療の初期に発生する可能性があり、次のように増加する可能性があります。
- NSAIDsの増量に伴い
- NSAIDの長期使用
- 食道(口から胃につながる管)、胃、腸の出血、潰瘍、裂傷(穿孔)のリスクの増加:
- 使用中いつでも
- 警告症状なし
- 死に至る可能性があるもの
潰瘍または出血のリスクは、次の場合に増加します。
- 胃潰瘍、またはNSAIDの使用による胃または腸の出血の過去の病歴
- 「コルチコステロイド」、「抗凝固剤」、「SSRI」または「SNRI」と呼ばれる薬の服用
- NSAIDの増量
- NSAIDの長期使用
- 喫煙
- アルコールを飲む
- 高齢
- 病弱
- 進行した肝疾患
- 出血の問題
NSAID は次の場合にのみ使用してください。
- 規定どおり
- あなたの治療のために可能な限り低い用量で
- 必要最小限の時間で
「冠動脈バイパス移植 (CABG)」と呼ばれる心臓手術の直前または直後に NSAID を服用しないでください。
最近心臓発作を起こした後は、医療提供者が指示しない限り、NSAID の服用を避けてください。最近の心臓発作の後にNSAIDを服用すると、別の心臓発作のリスクが高まる可能性があります
NSAIDとは何ですか?
NSAID は、さまざまな種類の関節炎、月経痛、およびその他の種類の短期的な痛みなどの病状による痛みや発赤、腫れ、および熱 (炎症) を治療するために使用されます。
NSAIDsを服用してはいけない人は?
NSAID を服用しないでください。
- 喘息発作、蕁麻疹、またはアスピリンやその他の NSAID によるその他のアレルギー反応を起こしたことがある場合。
- 心臓バイパス手術の直前または直後。
NSAIDS を服用する前に、次の場合を含め、すべての病状について医療提供者に伝えてください。
- 肝臓または腎臓に問題がある
- 高血圧がある
- 喘息がある
- 妊娠している、または妊娠する予定がある。妊娠中にNSAIDsの服用を検討している場合は、医療提供者に相談してください. 妊娠29週以降はNSAIDsを服用してはいけません
- 授乳中または授乳を計画している。
処方薬や市販薬、ビタミン、ハーブのサプリメントなど、服用しているすべての薬について医療提供者に伝えてください。 NSAIDs と他のいくつかの薬は相互に作用し、深刻な副作用を引き起こす可能性があります。 最初に医療提供者に相談せずに、新しい薬の服用を開始しないでください。
NSAIDsの考えられる副作用は何ですか?
NSAID は、次のような重大な副作用を引き起こす可能性があります。
「非ステロイド系抗炎症薬(NSAID)と呼ばれる薬について知っておくべき最も重要な情報は何ですか?」を参照してください。
- 新しいまたは悪化した高血圧
- 心不全
- 肝不全を含む肝臓の問題
- 腎不全を含む腎臓の問題
- 低赤血球(貧血)
- 生命を脅かす皮膚反応
- 生命を脅かすアレルギー反応
- NSAID のその他の副作用には次のようなものがあります。 胃痛、便秘、下痢、ガス、胸やけ、吐き気、嘔吐、めまい。
次のいずれかの症状が現れた場合は、すぐに緊急援助を受けてください。
- 息切れまたは呼吸困難
- 胸痛
- 体の一部または側面の脱力
- ろれつが回らない
- 顔や喉の腫れ
次のいずれかの症状が現れた場合は、NSAID の使用を中止し、すぐに医療提供者に連絡してください。
- 吐き気
- いつもより疲れている、または弱っている
- 下痢
- かゆみ
- 肌や目が黄色く見える
- 消化不良または胃痛
- 風邪のような症状
- 血を吐く
- 便に血が混じっている、またはタールのように黒くてねばねばしている
- 異常な体重増加
- 発熱を伴う皮膚発疹または水ぶくれ
- 腕、脚、手、足のむくみ
NSAID の服用量が多すぎる場合は、すぐに医療提供者に連絡するか、医師の診察を受けてください。
これらは、NSAIDs の考えられるすべての副作用ではありません。詳細については、NSAID について医療提供者または薬剤師にお尋ねください。
副作用に関する医学的アドバイスについては、医師に連絡してください。 1-800-FDA-1088 で副作用を FDA に報告できます。
NSAID に関するその他の情報
- アスピリンは NSAID ですが、心臓発作の可能性を高めることはありません。アスピリンは、脳、胃、腸で出血を引き起こす可能性があります。アスピリンは、胃や腸に潰瘍を引き起こすこともあります。
- 一部の NSAID は、処方箋なしで低用量で販売されています (店頭)。市販の NSAID を 10 日以上使用する前に、医療提供者に相談してください。
NSAID の安全で効果的な使用に関する一般情報
医薬品は、医薬品ガイドに記載されている以外の目的で処方されることがあります。処方されていない状態に NSAID を使用しないでください。他の人があなたと同じ症状を持っていても、NSAID を他の人に与えないでください。それらに害を及ぼす可能性があります。
NSAID についてさらに詳しい情報が必要な場合は、医療提供者に相談してください。医療専門家向けに書かれた NSAID に関する情報については、薬剤師または医療提供者に尋ねることができます。
この医薬品ガイドは、米国食品医薬品局によって承認されています。
